下列实验操作完全正确的是
| A.酸碱中和滴定曲线绘制实验:测试和记录pH的间隔时间要相同 |
| B.配置一定浓度的氯化钾溶液0.1mol/L:准确称取氯化钾固体,量筒量取1000ml水倒入容量瓶中,溶解,震荡摇匀,定容 |
| C.排除碱式滴定管尖嘴部分的气泡:将胶管弯曲使玻璃尖嘴断向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| D.取出分液漏斗中所需的上层液体:下层液体从分液漏斗下端尖口放出,关闭活塞,换一个接受容器,上层液体继续从分液漏斗下端管口放出 |
在常温下,将一定体积的某 NaOH 溶液分成两等分,与pH 均为2的一元酸 HA、HB恰好中和,消耗两种酸溶液的体积分别为V1、V2(V1≠V2)。则下列叙述中正确的是
A.若 Vl>V2,则说明 HA 的酸性比 HB的酸性强
B.中和后得到的两种溶液的 pH 均为 7
C.分别将两种酸溶液稀释10 倍后溶液的 pH 均为3
D.分别往等体积的两种酸溶液中加人足量锌粉,充分反应后产生的 H2的体积相等
常温下有浓度为0.1mol/L、体积为VL的氨水,向其中逐滴加入一定浓度的盐酸,得到如图的滴定曲线,其中d点时两种溶液恰好完全反应。根据图像回答下列问题:
(1)上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH如下表,请将表格补充完整:
| 离子浓度大小顺序 |
溶质化学式 |
溶液的pH |
| c (NH4+)>c (OH-)>c (CI-)>c (H+) |
① |
>7 |
| ② |
③ |
=7 |
| ④ |
NH4Cl |
⑤ |
(2)该温度时氨水的电离平衡常数K数值约为____________。滴定过程中所用盐酸的pH=____________。
(3)若取该实验中恰好完全反应的d点溶液,向其中滴加0.1VL某浓度的氨水后溶液呈中性,依(2)中计算结果计算所滴加氨水的浓度为____________ moI/L。
室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是
A.HA为强酸
B.a、b两点所示溶液中水的电离程度相同
C.b点所示溶液中c(A—)> c(HA)
D.pH=7时,c(Na+)=c(A—)+ c(HA)
用pH试纸测定某溶液的pH,如果先将pH试纸用蒸馏水润湿后,再把待测液滴到pH试纸上,跟比色卡对照,溶液的pH测得值为8,则该溶液的实际pH
| A.大于8 | B.小于8 | C.等于8 | D.小于7 |
室温下向10 mL 0.1 mol/L NaOH 溶液中加入0.1 mol/L 的一元酸HA 溶液pH 的变化曲线如图所示。下列说法正确的是
A.a 点所示溶液中c(A-)+c(HA)= 0.1mol/L
B.a、b 两点所示溶液中水的电离程度不同
C.pH="7" 时,c(Na+)=c(A-)+c(HA)
D.b 点所示溶液中c(HA) >c(A-)
某温度下水的离子积常数为KW,该温度下,将a mol/L的一元酸HA与b mol/L一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.a=b |
| B.混合溶液的pH=7 |
C.混合溶液中,c(H+)=  mol/L mol/L |
| D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-) |
某同学用中和滴定法去测定某烧碱的纯度,实验过程如下:
(1)配制待测液称取得 5.0g 固体烧碱样品(杂质不与酸反应)配制成 250 mL 溶液,
(2)用 0.2000 mol·L-1标准盐酸滴定待测烧碱溶液,实验操作如下
| A.用碱式滴定管取上述烧碱溶液10.00 mL,注入锥形瓶中,加入指示剂。 | B.用待测定 的溶液润洗碱式滴定管。 | C.用蒸馏水洗干净滴定管。 | D.取下酸式滴定管用标准的盐酸 溶液润洗后,将标准液注入酸式滴定管刻度“0”以上2~ 3 cm处,再把酸式滴定管固定好, 调节液面至刻度“0”或“0”刻度以下。E.检查滴定管是否漏水。F.另取锥形瓶,再重复 操作一次。G.把锥形瓶放在滴定管下面,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面的刻度。 |
①滴定操作的正确顺序是(用序号填写):________________
②该滴定操作中应选用的指示剂是:________________
③在G操作中如何确定终点?________________
(3)数据处理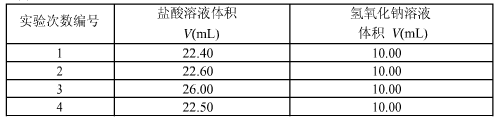
根据上述各数据,选取合适的三组,计算待测烧碱溶液的浓度为__________,烧碱的纯度为_________。
(4)下列操作,会导致实验结果偏低的是________(填序号)。
①碱式滴管用蒸馏水洗净后没有用待测液润洗 ②锥形瓶用蒸馏水洗净后没有用待测液润洗 ③终点读数时俯视(滴定前读数准确) ④酸式滴定管尖端气泡没有排除,滴定后消失 ⑤振荡时锥形瓶中液滴飞溅出来 ⑥酸式滴定管用蒸馏水洗净后没有用标准液润洗
欲用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,下列有关说法正确的是
| A.滴定管在装溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| B.锥形瓶在装待测溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| C.滴定过程中,两眼注视滴定管装液面的变化 |
| D.装标准液的滴定管中有气泡而滴定前未排出,则滴定结果将偏低 |
已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB- H++B2- ,则下列说法中一定正确的是
H++B2- ,则下列说法中一定正确的是
A、在Na2B溶液中一定有:c(OH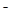 )=c(H
)=c(H )+c(HB
)+c(HB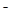 )+2c(H2B)
)+2c(H2B)
B、NaHB溶液可能存在以下关系:c(Na )>c(HB
)>c(HB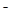 )>c(OH
)>c(OH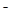 )>c(H
)>c(H )
)
C、NaHB水溶液中一定有:c(Na )+c(H
)+c(H )=c(HB
)=c(HB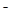 )+c(OH
)+c(OH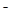 )+c(B
)+c(B )
)
D、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
25℃时,水的电离达到平衡:H2O H++OH-;DH>0,则下列叙述正确的是
H++OH-;DH>0,则下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,KW增大,pH不变 |
用0.1000mol·L-1标准NaOH溶液测定食醋中醋酸的含量,下列说法正确的是( )
| A.酸式滴定管、碱式滴定管及锥形瓶均需洗净后再润洗内壁2~3次 |
| B.应该选择酚酞作指示剂 |
| C.滴定过程中眼睛应始终注视滴定管内液面变化 |
| D.读取标准液的刻度时,滴定前平视,滴定后仰视,测定结果偏低 |
某温度下,水的离子积约为10-12,将Va L pH=2的硫酸溶液与Vb L pH=11的NaOH溶液混合,若混合溶液的pH=10,体积是(Va+Vb) L,则Va∶Vb为( )
| A.2∶11 | B.11∶2 | C.9∶2 | D.2∶9 |