下列说法正确的是
| A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以,HClO4的氧化性强 |
| B.已知①Fe + Cu2+ = Fe2+ + Cu;②2Fe3+ + Cu = 2Fe2+ + Cu2+,则氧化性强弱顺序为: Fe3+ > Cu2+> Fe2+ |
| C.已知还原性:B-> C-> D-,反应 2C-+ D2 = 2D-+C2和反应 2C-+ B2 =2B-+C2都能发生 |
| D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |
根据下列反应判断有关物质还原性由强到弱的顺序是
H2SO3+I2+H2O=H2SO4+2HI
2FeCl3+2HI=2FeCl2+2HCl+I2
3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3
| A.I->Fe2+ >H2SO3>NO |
| B.H2SO3>I->Fe2+>NO |
| C.Fe2+>I->H2SO3>NO |
| D.NO>Fe2+>H2SO3>I- |
下列有关说法正确的是
| A.电解精炼铜时,粗铜与外接电源的负极相连 |
| B.2Na2O2 + 2CO2 = 2Na2CO3 + O2在常温下能自发进行,则该反应的△H>0 |
| C.由PbO2 +4HCl(浓)= PbCl2 + Cl2↑+2H2O 可确定氧化性:PbO2>Cl2 |
| D.常温下,用蒸馏水不断稀释醋酸,溶液中c(CH3COO-)/c(CH3COOH)的值不变 |
在淀粉—碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,在上述溶液中加入足量的亚硫酸钠溶液,蓝色逐渐消失。下列判断不正确的是
A.氧化性:ClO->I2> |
| B.漂白粉溶液可使淀粉碘化钾试纸变蓝 |
| C.次氯酸钠可以与亚硫酸钠共存 |
| D.向氯水中加入亚硫酸钠溶液,氯水褪色 |
根据反应:2H2S+O2===2S↓+2H2O,Na2S+I2===2NaI+S↓,4NaI+O2+2H2SO4===2I2+2Na2SO4
+2H2O,下列物质的氧化性强弱判断正确的是
| A.O2>I2>S | B.H2S>NaI>H2O | C.S>I2>O2 | D.H2O>NaI>H2S |
(13分)某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示: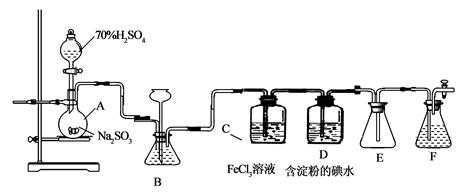
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若
,则整个装置气密性良好。装置E的作用是 。装置F中为 溶液。
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
| A.蒸馏水 | B.饱和Na2SO3溶液 |
| C.饱和NaHSO3溶液 | D.饱和NaHCO3溶液 |
(3)SO2气体还原Fe3+反应的产物是________________(填离子符号)。
(4)在上述装置中通入过量的SO2为了验证C中SO2与Fe3+发生了氧化还原反应,他们取C中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是____,原因是_______________________________________。
(5)能表明I-的还原性弱于SO2的现象是_________________,写出有关离子方程式:_____________。
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性是顺序为SO2 > I- > Fe2+ > H2O2> Cl-,则下列反应不可能发生的是
| A.2Fe2++Cl2=2Fe3++2Cl- |
| B.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| C.H2O2+H2SO4=SO2↑+O2↑+2H2O |
| D.SO2+I2+2H2O=H2SO4+2HI |
为了探究H2O2、H2SO3和Br2氧化性的相对强弱,设计如下实验(夹持仪器已略去)。请回答下列问题: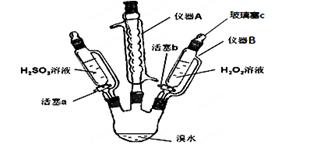
(1)仪器A的名称_________,其作用是___________。
(2)用仪器B滴加液体并不需要打开玻璃塞c,原因是____________________________。
(3)实验记录如下(请补全空白):
| 步骤 |
实验操作 |
实验现象 |
实验结论 |
| Ⅰ |
打开活塞a,逐滴加入H2SO3溶液至过量 |
________________ |
__________________________ |
| Ⅱ |
向步骤Ⅰ所得溶液中逐滴加入H2O2溶液 |
刚开始溶液颜色无明显变化,继续滴加,溶液变为橙黄色 |
__________________________ |
(4)步骤Ⅱ中,开始时颜色无明显变化的原因是(写出一条)_______________________,
步骤Ⅰ中反应的离子方程式_________________________________________________,
步骤Ⅱ中主要反应的离子方程式_____________________________________________。
某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置:(部分夹持装置已略去) 
(1)写出A中反应的离子方程式 。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式 。
(3)试从原子结构角度解释氯的氧化性大于硫原因 。
(4)D中干燥管中出现的现象及化学方程式 ; 。
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,该洗气装置中盛装 试剂。
(6)还有什么方法能证明氧化性Cl2 > S,用一种相关事实说明 。
已知:(1)2Fe3++2I-=2Fe2++I2 (2)Br2+2Fe2+=2Br-+2Fe3+,由此可判断有关离子的还原性从强到弱的顺序是
| A.Br->Fe2+>I- | B.I->Fe2+>Br- |
| C.Br->I->Fe2+ | D.Fe2+>I->Br- |
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++H2O2=2Fe2++O2↑+2H+ ,由此说明:
,由此说明:
(1)H2O2的氧化性比Fe3+ ,其还原性比Fe2+ (填“强”或“弱”) (2)
(2) 在H2O2分解过程中,FeSO4溶液 的作用是
在H2O2分解过程中,FeSO4溶液 的作用是
已知常温下在溶液里可发生如下两个离子反应:
Ce4++Fe2+===Fe3++Ce3+
Sn2++2Fe3+===2Fe2++Sn4+
由此可以确定Fe3+、Ce4+、Sn4+三种离子的氧化性由强到弱的顺序
| A.Sn4+、Fe3+、Ce4+ | B.Ce4+、Fe3+、Sn4+ |
| C.Sn4+、Ce4+、Fe3+ | D.Fe3+、Sn4+、Ce4+ |
(1)写出下列反应的离子方程式:
①氯化铵溶液和氢氧化钠溶液反应 ;
②少量二氧化碳通入澄清石灰水 ;
③三氧化二铁和盐酸反应 。
(2)铜和浓硫酸发生反应的化学方程式为:Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
下列说法正确的是
| A.金属原子失电子越多,其还原性越强 |
| B.CH4的摩尔质量为16g |
| C.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% |
| D.电解质物质本身可能导电 |