江苏省盐城市高三上学期期中考试化学试卷
最近美国化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是
| A.NH3是电解质 |
| B.该合成氨过程不属于氮的固定 |
| C.空气、水、太阳能均为可再生资源 |
| D.断裂N2中的N≡N键会释放出能量 |
下列有关化学用语表示正确的是
A.过氧化氢电子式: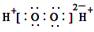 |
B.中子数为28的钙原子: Ca Ca |
C.铝离子结构示意图: |
D.2,4,6-三溴苯酚: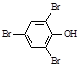 |
25℃时,下列各组离子在指定溶液中一定能大量共存的是
| A.能使甲基橙变红的溶液中:Na+、NH4+、MnO4-、SO32- |
| B.pH=14的溶液中:Mg2+、K+、Cl-、HCO3- |
| C.0.1mol·L-1 NH4I溶液中:Ca2+、Fe3+、SO42-、Br- |
| D.0.1mol·L-1 CuCl2溶液中:Mg2+、Al3+、NO3-、SO42- |
下列有关物质性质与应用对应关系不正确的是
| A.氧化镁是一种电解质,可直接用于工业上电解制镁 |
| B.熟石灰具有碱性,可用于治理被酸雨污染的湖泊和土壤 |
| C.Al(OH)3受热分解生成H2O并吸收大量的热量,可用作阻燃剂 |
| D.KMnO4能氧化乙烯,可用浸泡过高锰酸钾溶液的硅藻土作水果保鲜剂 |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.7.8gNa2O2中阴、阳离子总数为0.4NA |
| B.4.4gCO2和C3H8的混合气体中含有的分子总数为0.1NA |
| C.0.1mol苯乙烯中含碳碳双键总数为0.4NA |
| D.标准状况下,1.12L乙酸中含有氢原子总数为0.2NA |
实验室从含溴化氢的废液中提取溴单质,下列说法中能达到实验目的的是
| A.用装置甲氧化废液中的溴化氢 |
| B.用装置乙分离CCl4层和水层 |
| C.用装置丙分离CCl4和液溴 |
| D.用仪器丁长期贮存液溴 |
下列指定反应的离子方程式正确的是
| A.NaHCO3溶液中加入醋酸溶液:HCO3-+ H+ = CO2↑+ H2O |
| B.NaAlO2溶液中通入过量CO2气体:2AlO2-+ CO2 +3H2O = 2Al(OH)3↓+CO32- |
| C.Fe(OH)2溶于足量稀硝酸:Fe(OH)2 + 2H+ = Fe2+ + 2H2O |
D.乙醛与含有NaOH的Cu(OH)2悬浊液共热:CH3CHO + OH-+2Cu(OH)2 CH3COO-+ Cu2O↓+3H2O CH3COO-+ Cu2O↓+3H2O |
常温下,甲组中的某种物质能与乙组中的所有物质发生反应,甲组中的该物质是
| 甲组 |
①Al(OH)3 ②SiO2 ③ FeCl3溶液 ④ SO2 |
| 乙组 |
a.NaOH溶液 b.浓HNO3 c.氨水 d.氯水 e.H2O2溶液 |
A.① B.② C.③ D.④
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如下图所示。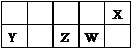
已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是
| A.原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X) |
| B.Z的最高价氧化物的水化物酸性比W的强 |
| C.X的简单气态氢化物的稳定性比W的弱 |
| D.X分别与Y、Z形成的化合物中化学键类型相同 |
建构数学模型来研究化学问题,既直观又简洁。下列建构的数轴模型正确的是
A.钠在氧气中燃烧,钠的氧化产物: |
B.铁在Cl2中燃烧,铁的氧化产物: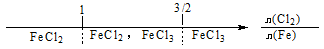 |
C.NH3与Cl2反应,反应产物: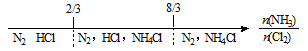 |
D.FeBr2溶液中通入Cl2,铁元素存在形式: |
下列有关说法正确的是
| A.电解精炼铜时,粗铜与外接电源的负极相连 |
| B.2Na2O2 + 2CO2 = 2Na2CO3 + O2在常温下能自发进行,则该反应的△H>0 |
| C.由PbO2 +4HCl(浓)= PbCl2 + Cl2↑+2H2O 可确定氧化性:PbO2>Cl2 |
| D.常温下,用蒸馏水不断稀释醋酸,溶液中c(CH3COO-)/c(CH3COOH)的值不变 |
一种瑞香素的衍生物的结构简式如图,下列有关该有机物性质的说法正确的是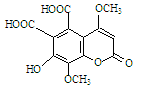
| A.能与FeCl3溶液发生显色反应 |
| B.1mol该有机物最多可与3molH2加成 |
| C.1mol该有机物最多可与含5molNaOH的溶液反应 |
| D.1mol该有机物与足量NaHCO3溶液反应可放出3molCO2 |
25℃时,0.1mol·L-1下列溶液的pH如下表,有关比较错误的是
| 序号 |
① |
② |
③ |
④ |
| 溶液 |
NaCl |
CH3COONH4 |
NaF |
NaHCO3 |
| pH |
7.0 |
7.0 |
8.1 |
8.4 |
A.酸的强度:HF>H2CO3
B.由水电离产生的c(H+):①=②
C.溶液中酸根离子浓度:c(F-)>c(HCO3-)
D.序号④中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol·L-1
在恒容密闭容器中进行的反应:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H 。在某压强下起始时按不同氢碳比[n(H2)/n(CO2)]投料(见右图中曲线①②③),测得CO2的平衡转化率与温度关系如下图所示,
C2H5OH(g)+3H2O(g) △H 。在某压强下起始时按不同氢碳比[n(H2)/n(CO2)]投料(见右图中曲线①②③),测得CO2的平衡转化率与温度关系如下图所示,
下列有关说法正确的是
| A.该反应:△H >0 |
| B.氢碳比:①<②<③ |
| C.其它条件不变的情况下,缩小容器的体积可提高CO2的转化率 |
| D.若起始CO2浓度为2mol·L-1、H2为4mol·L-1,在图中曲线③氢碳比条件下进行,则400K时该反应的平衡常数数值约为1.7 |
实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的主要实验流程如下。
(1)滤渣Ⅰ的成分为MnO2、单质S和 (写化学式);硫酸浸取时,Cu2S被MnO2氧化的化学方程式为 。
(2)浸取时,Fe2O3溶于硫酸的离子方程式为 ;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是 。
(3)“赶氨”时,最适宜的操作方法是 。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是 (写化学式)。
长托宁是一种选择性抗胆碱药,可通过以下方法合成(部分反应条件略去):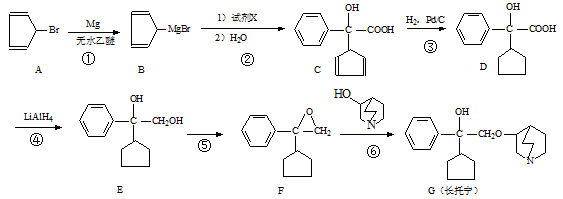
(1)长托宁中的含氧官能团为_________和_________(填名称)
(2)反应②中加入试剂X的分子式为C8H6O3 ,X的结构简式为_________
(3)反应③的反应类型为_______________
(4)S的同分异构体满足下列条件:
①.能与FeCl3溶液发生显色反应。
②.核磁共振氢谱有5个峰且峰的面积比为2:4:4:1:1;分子中含有两个苯环。写出该同分异构体的结构简式_________________
(5)根据已有知识并结合相关信息,写出以 和
和 为原料制备
为原料制备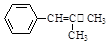 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: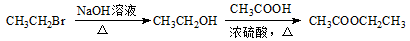
Co2(OH)2CO3和Co(CH3COO)2·nH2O均是生产高比能锂电池正极材料的前驱体。
(1)这两种钴的化合物中钴的化合价为 。
(2)Co2(OH)2CO3在空气中充分加热生成四氧化三钴,该反应的化学方程式为 。
(3)为确定Co(CH3COO)2·nH2O中的n值及其热分解过程,取一定量的样品在氮气氛围中加热,样品的固体残留率( )随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
)随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
①Co(CH3COO)2·nH2O晶体中n= (填自然数)。
②A→B点反应释放的气体为纯净物(由两种元素组成),该气体的结构简式为 。
③B→C点反应释放CO、CO2两种气体,n(CO)∶n(CO2)= 。
④D点残留固体的化学式为 。(列出上述计算过程)
某合作学习小组的同学拟用硼砂制取硼酸并测定硼酸样品的纯度。制备硼酸的实验流程如下: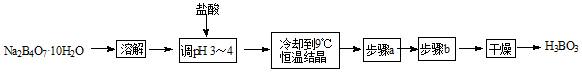
(1)溶解硼砂时需要的玻璃仪器有:烧杯和 。
(2)用pH试纸测定溶液pH的操作方法为 。
(3)用盐酸酸化硼砂溶液生成硼酸的离子方程式为 。
(4)实验流程中缺少的步骤a、步骤b操作分别为 、 。
(5)硼酸酸性太弱不能用碱的标准溶液直接滴定,实验室常采用间接滴定法,其原理为: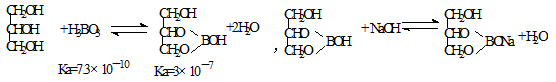
滴定步骤为:
①定到终点时溶液颜色变化是 。
②若滴定到终点时消耗NaOH标准溶液22.00mL,则本次滴定测得的硼酸样品中硼酸的质量分数为 (假定杂质不反应)。
③若滴定时滴定管尖嘴部分有气泡,滴定过程中消失,将导致测得的结果 (选填:“偏大”、“偏小”或“不变”)。
磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质。已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解。
(1)已知:①SO2 (g) +Cl2 (g)+ SCl2 (g) 2SOCl2 (g) △H="a" kJ·mol-1
2SOCl2 (g) △H="a" kJ·mol-1
②SO2Cl2(g)+ SCl2 (g)  2SOCl2(g) △H="b" kJ·mol-1
2SOCl2(g) △H="b" kJ·mol-1
则反应:SO2(g) + Cl2(g) SO2Cl2(g) △H = kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = 。
SO2Cl2(g) △H = kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = 。
(2)磺酰氯可与白磷发生反应为:P4+ 10SO2Cl2= 4PCl5 + 10SO2↑,若生成1molSO2,则转移电子的物质的量为 mol。
(3)某学习小组的同学依据反应:SO2(g)+ Cl2(g) SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图-1。
SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图-1。
①若用浓盐酸与二氧化锰为原料制取Cl2,其反应的化学方程式为 。
②有关图-1所示的装置说法正确的是 (不定项选择)。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为 。
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如图-2所示,已知电池反应为:2Li + SO2Cl2 =" 2LiCl" + SO2↑;则电池工作时,正极的电极反应式为 。
[物质结构与性质]磷化硼是一种高折射率红棕色晶体,可通过单质B与Zn3P2(或PH3)反应,也可热解PCl3·BCl3制得。
(1)锌离子基态时核外电子排布式为 。
(2)PH3中磷原子的杂化轨道类型为 ,BCl3空间形状为 (用文字描述)。
(3)PCl3能够与配合物Ni(CO)4发生配体置换反应:Ni(CO)4 +4PCl3 = Ni(PCl3)4 +4CO。
①与CO互为等电子体且带1个单位负电荷的阴离子化学式为 。
②1molNi(PCl3)4中含 键数目为 。
键数目为 。
(4)立方BP的晶胞结构如图所示,晶胞中含B原子数目为 。
[实验化学]铝镁加(Almagate)是一种制酸药,其组成为Al2Mg6(OH)14(CO3)2·4H2O,实验室可通过下列实验制备铝镁加。
步骤1.称取63.5gMgSO4·7H2O(0.26mol),30.5gAl2(SO4)3·18H2O(0.046mol) 溶于400mL水中得到混合溶液A,另称取无水Na2CO352g溶于400mL水得到溶液B。
步骤2.将A、B两溶液同时等速滴加到盛有400mL90℃水的2L三颈烧瓶中,维持90℃,不断搅拌。
步骤3.抽滤,并用蒸馏水洗涤沉淀3~4次,100℃下干燥5h,得白色疏松固体24.3g。
(1)步骤2需缓慢滴加两种溶液并不断搅拌,其主要原因是 。
(2)①步骤3抽滤时用到的硅酸盐质仪器有 、 。
②如何证明沉淀已洗涤干净 。
(3)本次实验所得产品产率为 。
(4)铝镁加中和胃酸的离子方程式为 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号