某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式
(2)实验②中化学反应转移电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是________________
(1)观察如下反应,总结规律,然后完成下列问题:
①Al(OH)3+H2O Al(OH)4- +H+ ②NH3+H2O
Al(OH)4- +H+ ②NH3+H2O NH4++OH-
NH4++OH-
(A)已知B(OH)3是一元弱酸,试写出其电离方程式
(B)已知N2H4是二元弱碱,试写出其二步电离方程式
。
(2)将a mol Cl2通入含 b mol FeBr2的溶液中,若0<a/b≤1/2时,反应的离子方程式为2Fe2+ +Cl2 = 2Fe3+ +2 Cl-,写出另2个可能发生的离子方程式。
①当1/2< a/b<3/2时 。
②当a/b≥3/2时 。
由amolFe+bmolFe2O3组成的混和物,用足量的盐酸溶解。随着a/b的不同,反应产物各不相同。按照a/b的不同比值,结合有关氧化还原的反应竞争顺序,填写下列表格内容。表格可不填满,若不足可添加表格。
| a/b |
氧化还原反应主要产物 |
有关的离子方程式 |
| |
|
|
| |
|
|
| |
|
|
| |
|
|
| |
|
|
氧化还原是常见的反应类型,根据信息回答以下问题: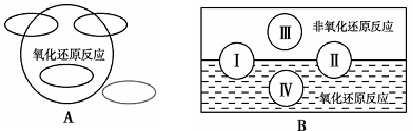
1、A图是“四种基本反应类型与氧化还原反应的关系”图,请在A图中用阴影部分表示反应:Cl2 + 2NaBr —→ 2NaCl + Br2 所属的区域。
2、“四种基本反应类型与氧化还原反应的关系”也可用B图表达。①其中Ⅰ为化合反应,则Ⅱ为 反应。②写出一个有水生成的符合反应类型Ⅲ的化学方程式: 。③写出一个有水参加的符合反应类型Ⅳ的化学方程式 ,
其中水作为 剂。(填氧化剂、还原剂等)
3、用“单线桥”分析下列氧化还原反应的电子转移方向及数目,并填空。
(1)2HClO —光→ 2HCl + O2↑ 氧化产物 被还原的元素
(2)2NaCl + 2H2O —电解→ 2NaOH + Cl2↑ + H2↑
4、有F-、Cl-、I-、Br2、I2五种粒子,其中氧化性最强的是 ,还原性最强的是 ,用离子方程式表示氧化性强弱的事实:
。
过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填空:
| A.Na2O2 +2HCl= 2NaCl+H2O2 | B.Ag2O+ H2O2=2Ag+O2+ H2O |
| C.2 H2O2="2" H2O+O2 | D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O |
(1)H2O2仅体现氧化性的反应是(填代号) 。
(2)H2O2既体现氧化性又体现还原性的反应是(填代号) 。
(3)上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是: 。
将 分别含有MnO4—、Fe3+、Fe2+、I—的四种溶液混合,调节溶液的pH值,使pH=1,充分反应后:
分别含有MnO4—、Fe3+、Fe2+、I—的四种溶液混合,调节溶液的pH值,使pH=1,充分反应后:
(1)若I—离子有剩余,则上述四种离子在溶液中还存在的有 ,一定不存在的是 ;
(2)若所得混合液呈紫色,则上述四种离子在溶液中一定存在的有 ,一定不存在的离子有 ;
铜跟稀硝酸可发生反应:3Cu + 8HNO3(稀)=3Cu(NO3)2 + 2NO↑+ 4H2O。在该反应中,铜元素的化合价 (填“升高”或“降低”),被 (填“氧化”或“还 原”);硝酸体现_____________性,若反应中生成转移0.6mole,则生成___ L NO(标况)。
原”);硝酸体现_____________性,若反应中生成转移0.6mole,则生成___ L NO(标况)。
在酸性条件下:
①KBrO3能将KI氧化成I2或KIO3,其本身被还原成Br2;
②KIO3能将I-氧化为I2,也能将Br-氧化成Br2,其本身被还原成I2。
(1)上述反应所涉及到的粒子氧化性最强的是 (填离子符号);
(2)写出一个能证明氧化性Br2>I2的离子方程式 ;
(3)向含有KI、H2SO4的溶液中加入KBrO3溶液,若氧化产物、还原产物只有I2和Br2,写出反应的化学方程式,并标明电子转移方向和数目。
_______________________________________________________;
其中被氧化的元素是_________,要得到1mol还原产物转移电子数目为____________。
已知①氯水和溴水能将Fe2+氧化成Fe3+,而碘水不能;②Fe3+可以使KI-淀粉试液变蓝色。
⑴向100mL FeBr2溶液中通入标况下体积为3.36L的Cl2,充分反应后测得溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为 ;
⑵向含1 molFeI2和2mol FeBr2溶液中通入3 mol Cl2后,溶液中所含各种离子的个数之比是 ;
⑶向含a molFeI2和bmol FeBr2溶液中通入c mol Cl2,若要保证溶液中含有两种阳离子,c的取值范围是 。
在高温时,水蒸气与灼热的炭发生氧化还原反应的化学方程式是H2O+C H2+CO,其中水是 剂。硫在氧气中燃烧的化学方程式是 ,其中硫是 剂。
H2+CO,其中水是 剂。硫在氧气中燃烧的化学方程式是 ,其中硫是 剂。
氧化一还原反应实际上是含氧化反应和还原反应二个过程,一个还原反应过程如下:NO3—+4H++ 3e— NO+ 2H2O
下列四种物质:KMnO4,Na2CO3,KI,Fe2(SO4)3中的一种物质甲,滴加少量稀硝酸,能使上述反应过程发生。
(1)被还原元素是______ ;还原剂是 ;
(2)写出并配平该氧化还原反应的化学方程式并用双线桥注明其电子转移的方向和数目: ;
(3)反应生成0.4mol H20,则转移电子的数目为 个;
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂物质的量之比将 (填“增大”、“不变”、“减小”或“不能确定”)
在盛有淀粉KI溶液的试管中,滴加少量的NaClO溶液和稀H2SO4,会立即看到溶液变为蓝色,这是因为______________________________,相应的离子方程式为__________在盛有淀粉和碘水的混合液中,滴加Na2SO3溶液,发现__________________现象,这是因为________________________,其离子方程式为______________________________,对于上述两组实验的结果,可得出:ClO-、I2、SO42-的氧化性强弱顺序为___________________。
21在Fe + 2HCl ="=" FeCl2(氯化亚铁) + H2↑ 反应中。
② 此反应若转移了12mol的电子,则生成氢气 L(标准状况下).