下列各物质转化关系如图所示,A是一种高熔点固体,D是一种红棕色固体。
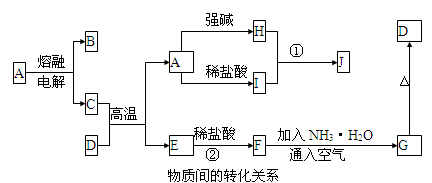
根据上述一系列关系回答:
(1)填写物质的化学式:B , G 。
(2)写出D物质中金属元素基态原子的核外电子排布图 。
(3)写出下列反应的离子方程式:
①H溶液和I溶液混合生成J___________ 。
②E和盐酸反应 。
(4)在电解熔融状态A的过程中,当电路中通过1mol电子时,阳极上产生的气体体积为 L。(标准状况下)
在如图所示的一些常见单质,化合物等物质之间的转化关系中(有些反应过程中的水,部分产物和反应条件未全部列出),已知反应①是氯碱工业的最基础的反应,A、B、F、H、J的焰色反应均为黄色,热的F溶液可以去除物品表面的油污,I为地壳中含量最多的金属元素的单质,L是典型的两性氧化物,在常温常压下C、D、G均为气体,D呈黄绿色,G是形成温室效应的主要气体.
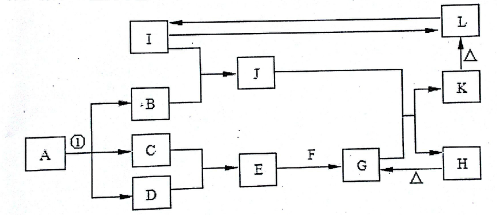
(1)反应①进行的条件为 .
(2)化合物F的化学式为 .
(3)I与氧化铁反应的化学方程式为 .
(4)J的水溶液与G反应生成K和H的离子方程式为 .
已知A、B、C、D四种强电解质溶液,分别含有下列阴阳离子中的各一种,且互不重复:Ba2+、H+、Na+、NH4+、CO32﹣、NO3﹣、SO42﹣、OH﹣.已知:①A和B反应生成的气体能被D吸收,而A和D反应生成的气体能被B吸收;②向A或D中滴入C,均有白色沉淀产生.另有晶体E的摩尔质量为474g/mol,可用于自来水的净水剂.试判断:
(1)晶体E的名称为 ,用离子方程式和必要的文字说明E可用作净水剂的原理 .
(2)写出A、B、C的化学式:A ,B ,C .
(3)写出A与D反应的离子方程式 .
(4)将200mL0.5mol/L的B溶液加入到150mL0.2mol/L的E溶液中,最终生成的白色沉淀质量为 g.
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
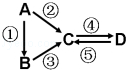
(1)若B是淡黄色固体,②③反应均用到同一种液态氢化物.D物质常用于食品工业.写出④反应的化学方程式 .
(2)若B是气态氢化物.C、D是氧化物且会造成光化学烟雾污染.写出③反应的化学方程式 .
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体.写出④反应离子方程式 .
(4)若A是太阳能电池用的光伏材料.C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性.写出②反应的化学方程式 .
(5)若A是应用最广泛的金属.④反应用到A,②⑤反应均用到同一种非金属单质.写出④反应的离子方程式 .
下列框图所示的转化关系中,甲为生活中常见的金属单质,乙、丙、丁为气体单质,D为家庭中常用物质(部分反应物和生成物及溶剂水已略去).
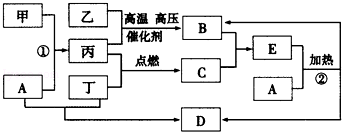
请回答:
(1)E的化学式为 ;甲的原子结构示意图为 ;
(2)反应①的离子方程式为 ;反应②的化学方程式为 ;
(3)实验室制取并收集B的操作中,用 法收集B,验证B已收集满的方法是 (限答一种).
(4)实验室制备丁的方程式为 ,工业上输送丁的管道出现气体泄漏,如何查漏(用方程式表示) .
A、B、C、D为可溶于水的四种固体,B的水溶液呈浅绿色,D为含氧酸盐,组成它们的离子有:
| 阳离子 |
Fe2+、Na+、Ba2+、Al3+ |
| 阴离子 |
Cl-、SO42-、NO3-、OH- |
Ⅰ.将四种固体溶于水,分别取它们的水溶液进行实验,结果如下:
(1)A溶液的颜色反应为黄色,则A溶液中含有的金属离子是___________(填离子序号)。
(2)将A的水溶液逐滴加入C中,先生成白色沉淀,后白色沉淀逐渐溶解,请写出白色沉淀逐渐溶解的离子方程式___________________。
(3)B溶液与D溶液反应生成不溶于稀硝酸的白色沉淀,请写出该反应的离子方程式_____________。
Ⅱ.(4)据此推断它们是(写化学式)A______________;D_____________。
(5)A溶液与B溶液反应的现象为________________________。
有一包白色粉末状混合物,可能含有K2CO3、CuSO4、AlCl3、NaOH中的某几种,现进行如下实验:
① 将混合物溶于水,得到无色透明溶液。
② 取少量上述溶液两份:
第一份中加入稀硝酸,开始出现白色沉淀,有气泡产生,继续加入稀硝酸,沉淀全部溶解,再加入AgNO3溶液,又出现白色沉淀;
第二份进行焰色反应,直接观察,火焰呈黄色。
根据上述实验现象回答:
(1)原混合物中肯定有 。
(2)第一份中,继续加入稀硝酸,沉淀全部溶解的离子方程式为 。
(3)第一份中,再加入AgNO3溶液,又出现白色沉淀的离子方程式为 。
(4)第二份进行焰色反应,为什么观察不到K+的焰色反应 。
无机推断题组(一题多变题组)
已知:A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出E中含有的化学键类型 ;已知1molA与水反应放出283.5kJ的热量,试写出A与水反应的热化学反应方程式 ;
(2)若A 为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则单质A与H2O反应的离子方程式 。
(3)若A 为淡黄色粉末,回答下列问题:
①1molA与足量的H2O充分反应时,转移电子总数为 。
②若X为非金属单质,通常为黑色粉末,写出D的结构式 ;
(4)若A为氧化物,X是Fe,溶液D加入KSCN溶液变红。
①A与H2O反应的离子方程式 。
②请用离子方程式表示D盐的净水原理 。
A→J有如图所示的转化关系(反应条件、部分反应物和产物已忽略):其中A、D为银白色金属单质;B为淡黄色粉末,C为红棕色粉末,E为黑色晶体;H久置于空气中,由白色固体变为灰绿色,最终变成红褐色Ⅰ;B和I在一定条件下反应生成J,J的化学式为Na2FeO4,它能够杀菌消毒,是一种优良的净水剂。
(1)物质C俗称__________;物质B的一种用途________
(2)写出下列反应的化学反应方程式:
⑤ ____________________________
⑧ _____________________________
(3)写出反应的离子方程式:⑦______________________
(4)在①-⑧的所有反应中,属于非氧化还原反应的有(填序号)_________
(5)根据Na2FeO4元素的价态及反应前后的产物推测Na2FeO4杀菌消毒做净水剂的原因________
有一包白色固体粉末,可能含有K2SO4、Na2CO3、NH4Cl、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
①取少量固体粉末加到足量水中,得到无色溶液;
②取①中溶液少量继续往其中加入足量稀硫酸,有气泡产生;
③继续向②中的溶液加Ba(NO3)2溶液,有白色沉淀生成;
④取①中溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝。
根据以上事实判断:
(1)肯定存在的是______________。
(2)肯定不存在的是____________。
(3)不能确定是否存在的是_____________。请简述证明该物质是否存在的实验方案(实验方法、现象、结论)__________________________。
(4)写出上述实验④中产生刺激性气味反应的离子方程式:_____________________。
中学化学常见物质A、B、C、D、X、Y,存在如下图转化关系(部分物质和条件略去)
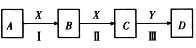
(1)若A为NaOH溶液,X为CO2,D是沉淀,则Y可为___________(填序号)。
A.SO3 B.Ba(OH)2 C.H2SO4 D.CaO
(2)若A为黄铁矿(FeS2),D是H2SO4,则反应Ⅱ的化学方程式为_________________________。
(3)若A为碱性气体,A与D反应生成一种化肥,则反应Ⅲ的化学方程式为__________________。
(4)若A和X均为单质,反应Ⅲ的现象是白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,则反应II的离子方程式为__________________________。
有关物质的转化关系如下图所示(部分物质和条件已略去)。A、D是常见金属,B、C是它们的氧化物,B是红棕色固体,D是年产量最高的金属,I、J是氯碱工业的主要产品,H是一种常见强酸,可由氯碱工业的产品为原料制得。请回答下列问题:

(1) B的化学式为 。
(2) H的电子式为 。
(3) 写出E与I反应的离子方程式: 。
(4) 写出A与J反应的化学方程式: 。
已知A是用途最广泛的金属单质,B是常温下呈液态的化合物,E是一种黄绿色的气体。(图中部分产物未标出)。

回答下列问题:
(1)写出F的化学式 。
(2)写出下列反应的化学反应方程式:
反应① ;
反应⑧ 。
(3)写出反应③的离子方程式: 。
(4)鉴别G溶液中阳离子的方法 。
(5)将H溶液滴加到沸水中,继续加热煮沸,得到的液体颜色为 。
Ⅰ.现有Al3+、NH4+、CO32—、HCO3— 等离子,回答下例问题:
①在强酸性条件下能够存在的离子是 ;
②在强碱性条件下能够存在的离子是 ;
③在强酸性和强碱性条件下都不能存在的离子是 。
Ⅱ.由Na+、NH4+、 Ba2+、 Cu2+、 OH—、 Fe3+、 SO42—、 Cl— 等八种离子中的六种两两组成的A、B、C三种化合物(它们不含有共同离子,已知NH4+与OH— 反应有碱性气体生成)。
A.A、B、C均易溶于水,形成无色溶液;
B.将A、B、C三种物质的溶液相互作用时,发现A与B混合后产生有刺激性气味的气体,此气体使湿润红色石蕊试纸变蓝,B与C混合产生白色沉淀,则:
①A、B、C的化学式为:
A、 ;
B、 ;
C、 。
②B+C反应的离子方程式为: 。
若四种溶液,分别含有: ①Al3+ ②Mg2+ ③Fe2+ ④Fe3+ 离子。请回答下列问题:
(1)遇KSCN溶液呈红色的是 。
(2)加铁粉溶液质量增重的是 。
(3)加入过量NaOH溶液中最终无沉淀的是 。
(4)加入新制Cl2水溶液变黄色的是 ,反应的离子方程式是 。