化学与生产、生活密切相关。从化学视角回答下列问题:
(1)节日焰火利用的是 反应,城市射灯在夜空形成五颜六色的光柱,属于____效应,工业上制造光导纤维的基本原料是 。
(2)pH< 的雨水称为酸雨,我国形成酸雨的主要污染物是 。
(3)化工厂曾用浓氨水来检验氯气管道是否漏气,反应原理为(在有水蒸气存在时):2NH3+3Cl2==6HCl+N2。如果氯气管道某处漏气,用该方法检查时的现象是___________。
(4)碳酸氢铵俗称碳铵,是一种廉价氮肥,它的最大缺点是 。如果向碳酸氢铵溶液中滴加NaOH溶液至过量,反应的离子方程式是_____________________。
(现有以下物质:①NaOH溶液 ②液氨 ③BaCO3固体 ④熔融KHSO4 ⑤Fe(OH)3胶体 ⑥铜⑦CO2 ⑧CH3COOH
(1)以上物质中属于混合物的是____________(填序号)
以上物质中属于非电解质的是____________(填序号)
(2)对物质⑤进行通电,观察到阴阳两极的现象是____________
以上纯净物中能导电的是___________(填序号)
(3)写出①和⑧的水溶液反应的离子方程式____________
(4)写出④的电离方程式____________
(5)在足量④的水溶液中加入少量③,发生反应的离子方程式为____________
(6)在含0.4mol①的溶液中缓慢通入标准状况下6.72LCO2,气体被完全吸收,则反应后的溶质有___________(填化学式),该过程总的离子反应方程式为____________
钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧可获得钛酸钡粉体。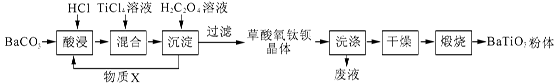
(1)酸浸时发生的反应的离子方程式为 ;为提高BaCO3的酸浸率,可采取的措施为 (任答一点)。
(2)配制TiCl4溶液时,通常将TiCl4溶于浓盐酸,目的是 。
(3)加入H2C2O4溶液时,发生反应的化学方程式为 ;
可循环使用的物质X是 。
(4)煅烧得到BaTiO3的同时,生成高温下的气体产物有CO、 和 。
某课题组研究以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺,其设计的流程如下:

回答下列问题:
(1)已知在焙烧硫铁矿石过程中铁元素转化成了Fe3O4,则该反应的化学方程式是 ;
(2)“酸溶”中反应的离子方程式是 ;
(3)“过滤”后滤液中金属阳离子有 ;
(4)“氧化”中使用的氧化剂最好是 ;
用一种试剂除去下列各物质中的杂质(括号内的物质)。写出所用试剂及反应的离子方程式。
(1)BaCl2(HCl):试剂 ,离子方程式 。
(2)O2(CO2):试剂 ,离子方程式 。
(3)SO42-(CO32-):试剂 ,离子方程式 。
(4)Cu粉(Al粉):试剂 ,离子方程式 。
在烧杯中盛有半杯的Ba(OH)2溶液,然后用滴管向烧杯中滴加H2SO4(装置如图)。随着硫酸的滴入,电灯会逐渐变暗,当两者恰好完全反应时,电灯完全熄灭。
(1)该实验说明溶液的导电性与_________________有关。
(2)上述反应的离子方程式为_________________________________________。
(3)可以利用上述原理进行溶液浓度的测定。若烧杯中装有75mL 0.1mol/L Ba(OH)2溶液,当滴入25mL H2SO4时,电灯完全熄灭。试求该硫酸溶液的物质的量浓度为
在Cl-浓度为0.5 mol·L-1的某无色澄清溶液中,还可能含有下表中的若干种离子。
| 阳离子 |
K+Al3+Mg2+Ba2+ Fe3+ |
| 阴离子 |
NO3-CO32-SiO32-SO42- OH- |
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
| 序号 |
实验内容 |
实验结果 |
| Ⅰ |
向该溶液中加入足量稀盐酸 |
产生白色沉淀并放出标准状况下0.56 L气体 |
| Ⅱ |
将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 |
固体质量为2.4 g |
| Ⅲ |
向Ⅱ的滤液中滴加BaCl2溶液 |
无明显现象 |
请回答下列问题。
(1)通过以上实验能确定一定不存在的离子是____ ____。
(2)实验Ⅰ中生成沉淀的离子方程式为___________________________。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满)。
| |
阴离子 |
浓度c/(mol·L-1) |
| ① |
|
|
| ② |
|
|
| ③ |
|
|
| ④ |
|
|
(4)判断K+是否存在,若存在,求出其最小浓度,若不存在说明理由:_____________。
写出下列反应的离子方程式。
(1)用稀硫酸清洗铁锈(Fe2O3)_____________________________________
(2)碳酸钠溶液与盐酸混合___________________________________________
(3)硫酸铜溶液和氢氧化钡溶液混合_____________________________
(4)向足量澄清石灰水中通入二氧化碳________________________
某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀CuI。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
已知:I2+2S2O32-=S4O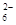 +2I-
+2I-
①可选用_____作滴定指示剂,滴定终点的现象是_______________________________ 。
②CuCl2溶液与KI反应的离子方程式为_______________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
按要求写出下列反应的方程式
(1)工业用石英制取粗硅的反应方程式:_______________________________;
(2)工业用赤铁矿做原料炼铁的反应方程式: ;
(3)金属铝与NaOH溶液反应的离子方程式:_______________________________;
(4)FeSO4溶液中滴加双氧水的离子方程式: ;
(5)酸性条件下, MnO4—被SO2还原为Mn2+的离子方程式:___________________________;
除去下列物质中的杂质,写出发生反应的离子方程式:
(1)硝酸钾中混有溴化钾___________
(2)碳酸氢钾溶液中混有碳酸钾___________,
(3)二氧化碳气体中混有氯化氢气体___________。
有四种物质:①Al2O3、②HNO3、③NaHCO3、④Ba(OH)2。根据要求,回答下列问题:
(1)写出物质④的电离方程式_______________________________。
(2)写出物质②和③反应的离子方程式_______________________________。
(3)既能与强酸反应,又能与强碱反应的物质是____________(填序号)。
按要求填空
(1)硫酸铝(写出电离方程式)
(2)稀硫酸跟氧化镁反应(写出离子方程式)
(3)盐酸跟碳酸氢钠溶液反应(写出离子方程式)
(4)Cu2+ + 2OH—= Cu(OH)2↓(写出化学方程式)
(5)氢氧化铁胶体制备(写出化学方程式)
为建设美丽浙江,浙江省政府开展“五水共治”。
(1)城市饮用水处理时可用二氧化氯(ClO2)替代传统的净水剂Cl2。工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:_______________。
(2)某地污水中的有机污染物主要成分是三氯乙烯 (C2HCl3),向此污水中加入KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式_________________。