在盛有AgNO3、HCl、Na2CO3、CaCl2、NaCl、KCl六种无色溶液的试剂瓶上分别贴有①~⑥的编号,分别取它们两两混合,产生的现象如下表所列(其中“↑”表示产生气体,“↓”表示生成沉淀,“—”表示无现象):
| |
① |
② |
③ |
④ |
⑤ |
⑥ |
| ① |
|
— |
— |
↓ |
↓ |
↑ |
| ② |
— |
|
— |
— |
↓ |
— |
| ③ |
— |
— |
|
— |
↓ |
— |
| ④ |
↓ |
— |
— |
|
↓ |
— |
| ⑤ |
↓ |
↓ |
↓ |
↓ |
|
↓ |
| ⑥ |
↑ |
— |
— |
— |
↓ |
|
(1)推断下列编号对应的溶液(写溶质的化学式):
①_______,④_______,⑤________,⑥________。
(2)向①与⑤反应后的生成物中加入足量HNO3溶液,反应的离子方程式为__________________。
(3)通过以上实验,还有两种溶液不能确定,若要进一步确定它们,必须进行的实验是________________
按要求写出下列反应的方程式
(1)工业用石英制取粗硅的反应方程式:_______________________________;
(2)工业用赤铁矿做原料炼铁的反应方程式: ;
(3)金属铝与NaOH溶液反应的离子方程式:_______________________________;
(4)FeSO4溶液中滴加双氧水的离子方程式: ;
(5)酸性条件下, MnO4—被SO2还原为Mn2+的离子方程式:___________________________;
四只试剂瓶中分别盛有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,可用于检验的试剂有Ba(NO3)2溶液、AgNO3溶液、稀HNO3,就如何检验这四种溶液分别回答下列各题。在四支试管中分别取四种溶液各1mL,按一定的实验顺序完成下列实验。
(1)在四支试管中分别滴入___________,出现的现象是____________,可以确定试管中的溶液是___________离子方程式是_____________________________________。
(2)在剩余三支试管中分别滴入___________,出现的现象是_________,可以确定试管中的溶液是___________离子方程式是_____________________________________。
(3)在剩余两支试管中分别滴入___________,出现的现象是__________,可以确定试管中的溶液是___________离子方程式是_____________________________________。
(4)三次实验中都没有明显变化的是_______________。
写出下列离子方程式:
(1)泡沫灭火器原理:__________________________________________________________________
(2)胃舒平治疗胃酸过多:____________________________________________________________
(3)FeS除去废水中铅离子:_____________________________________________________
亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3 H+ + H2PO3-。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
H+ + H2PO3-。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
(1)①写出亚磷酸与少量NaOH溶液反应的离子方程式 。
②根据亚磷酸(H3PO3)的性质可推测Na2HPO3稀溶液的pH 7(填“>”、 “<” 或“=”)。
(2)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式 。
(3)电解Na2HPO3溶液也可得到亚磷酸,装置示意图如下:

说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过。
①阴极的电极反应式为 。
②产品室中生成亚磷酸的离子方程式为 。
取来两份等浓度的NaOH溶液A和B,每份10ml,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,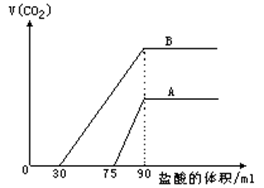
试回答下列问题:
(1)原NaOH溶液的物质的量浓度为 _______________mol/L
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质为(写化学式)___________________;其物质的量之比为_____________。
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸产生CO2气体体积(标准状况)的最大值为________________ml。
在Cl-浓度为0.5 mol·L-1的某无色澄清溶液中,还可能含有下表中的若干种离子。
| 阳离子 |
K+Al3+Mg2+Ba2+ Fe3+ |
| 阴离子 |
NO3-CO32-SiO32-SO42- OH- |
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
| 序号 |
实验内容 |
实验结果 |
| Ⅰ |
向该溶液中加入足量稀盐酸 |
产生白色沉淀并放出标准状况下0.56 L气体 |
| Ⅱ |
将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 |
固体质量为2.4 g |
| Ⅲ |
向Ⅱ的滤液中滴加BaCl2溶液 |
无明显现象 |
请回答下列问题。
(1)通过以上实验能确定一定不存在的离子是____ ____。
(2)实验Ⅰ中生成沉淀的离子方程式为___________________________。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满)。
| |
阴离子 |
浓度c/(mol·L-1) |
| ① |
|
|
| ② |
|
|
| ③ |
|
|
| ④ |
|
|
(4)判断K+是否存在,若存在,求出其最小浓度,若不存在说明理由:_____________。
某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、盐酸和Na2CO3溶液将这三种离子逐一沉淀分离。其流程图如所示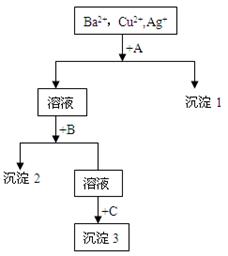
(1)沉淀的化学式(写出最佳答案):
沉淀1 ,沉淀3 ;
(2)写出溶液+B的离子方程式: 。
研究工业废弃物的处理和防治具有重要的意义。
(1)利用反应CH4+2NO2 N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是____,当消耗CH4的体积是11.2 L(标准状况下)时,理论上可处理____molNO2。
N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是____,当消耗CH4的体积是11.2 L(标准状况下)时,理论上可处理____molNO2。
(2)治理汽车尾气中CO和NO的一种方法是:在汽车排气管中安装一个催化转化装置,该装置能将CO和NO转化为参与大气循环的无毒气体。该反应的化学方程式为________________.
(3)某无色废水中可能含有Fe3+、Al3+、Na+、Cl-、OH-、SO42-、中的几种离子。分别取三份废水进行如下实验:
I.进行焰色反应实验,火焰为无色。
Ⅱ.取100 mL废水,加入足量的BaCl2溶液,生成2.33g白色沉淀。
Ⅲ.取100 mL废水,逐滴加入1.0 mol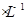 的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如下图所示。
的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如下图所示。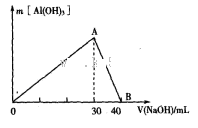
请根据上述信息回答下列问题:、
①该废水中一定不含有的离子是__________.
②实验中需配制1.0 mol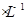 的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有_______。
的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有_______。
③写出图中A→B反应的离子方程式:_______________________。
④通过计算,该废水中______Cl-(填“含有”或“不含有”);若含有,则c(Cl-)=________(若不含有,此问不必作答)。
(10分)霞石是一种硅酸盐,其组成可表示为K2O·3Na2O·4Al2O3·8SiO2,某小组同学设计以霞石为原料制备Al2O3的方案如下:
请回答下列问题:
(1)沉淀1的主要成分的化学式为 。
(2)向滤液1中加入过量NaOH溶液的有关反应离子方程式为 。
(3)由溶液2生成Al(OH)3的离子方程式为 。
(4)某同学提出上述流程较繁琐,可简化流程,其方法是向滤液1中加入足量的试剂X即可得到Al(OH)3,则试剂X为 。
(12分)某无色溶液中只含有下列8种离子中的某几种:Mg2+、H+、Ag+、Na+、Cl-、HCO3-、OH-、NO3-,已知该溶液能与铝反应且放出的气体只有氢气。试回答下列问题:
(1)若反应后生成Al3+,反应的离子方程式为________________,则原溶液中一定大量存在的离子有________________,一定不能大量存在的离子有__________________。
(2)若反应后生成AlO2-,反应的离子方程式为 ,则溶液中一定大量存在的离子有 ,一定不能大量存在的离子有 。
有四种物质:①Al2O3、②HNO3、③NaHCO3、④Ba(OH)2。根据要求,回答下列问题:
(1)写出物质④的电离方程式_______________________________。
(2)写出物质②和③反应的离子方程式_______________________________。
(3)既能与强酸反应,又能与强碱反应的物质是____________(填序号)。
按要求填空
(1)硫酸铝(写出电离方程式)
(2)稀硫酸跟氧化镁反应(写出离子方程式)
(3)盐酸跟碳酸氢钠溶液反应(写出离子方程式)
(4)Cu2+ + 2OH—= Cu(OH)2↓(写出化学方程式)
(5)氢氧化铁胶体制备(写出化学方程式)
为建设美丽浙江,浙江省政府开展“五水共治”。
(1)城市饮用水处理时可用二氧化氯(ClO2)替代传统的净水剂Cl2。工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:_______________。
(2)某地污水中的有机污染物主要成分是三氯乙烯 (C2HCl3),向此污水中加入KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式_________________。