短周期元素形成的常见非金属固体单质 A 与常见金属单质 B,在加热条件下反应生成化合物 C,C 与水反应生成白色沉淀 D 和气体 E,D 既能溶于强酸,又能溶于强碱。E 在足量空气中燃烧产生刺激性气味的气体 G,G 在大气中能导致酸雨的形成。E 被足量氢氧化钠溶液吸收得到无色溶液 F。溶液 F 在空气中长期放置发生反应,生成物之一为 H。H 与过氧化钠的结构和化学性质相似,其溶液显黄色。请回答下列问题:
(1)组成单质 A 的元素位于周期表中第__________ 周期,第___________ 族。
(2)B 与氢氧化钠溶液反应的化学方程式为:_____________________。
(3)G 与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为__________,当生成 2mol 二氧化氯时,转移电子___________mol。
(4)溶液 F 在空气中长期放置生成 H 的化学方程式为:________________________。
(5)H 的溶液与稀硫酸反应产生的现象为_______________________。
A、B、C属于周期表前4周期的元素,它们的原子序数依次增大。A、B属于同一周期,C是生活中常见的金属元素。A的氧化物是沙子的主要成分,B的单质常温下为黄色粉末。
(1)C在周期表中位于___________周期____________族。
(2)在加热条件下B单质与C单质反应的化学方程式是_____________________________。
(3)A的氧化物用NaOH溶液处理,使A元素变为可溶性盐,该反应的离子方程式是____________。
(4)B与C形成的化合物CB2,在有水存在的条件下用氧气氧化该化合物,得到强酸性溶液和低价盐,该氧化还原反应的化学方程式是_____________________________________。
A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,B与D形成的化合物BD与C的单质C2电子总数相等,CA3分子结构为三角锥形,D与E可形成E2D与E2D2两种离子化合物,D与F是同族元素。
根据以上信息,回答下列有关问题:
(1)写出基态时D的电子排布图 。
(2)写出化合物E2F2的电子式 ,化合物ABC的结构式 。
(3)根据题目要求完成以下填空:
BF32-中心原子杂化方式 ;D3中心原子杂化方式 ;
FD42-微粒中的键角 ;FD3分子的立体构型 。
(4)根据等电子原理,指出与BD2互为等电子体且含有C原子的微粒有 、 (要求写一种分子和一种离子)。
下表为元素周期表的一部分,根据表中所列出的元素回答下列问题
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
|
|
|
C |
N |
O |
F |
|
| 3 |
Na |
Mg |
Al |
Si |
|
S |
Cl |
Ar |
(1)最不活泼的元素是 (填元素符号,下同),最活泼的非金属元素是
(2)可做半导体材料的元素是 (填元素名称)
(3)氧离子结构示意图为 ,C、N、O原子半径从大到小的顺序是
(4)与水反应最剧烈的金属单质是 ,其反应的化学方程式是
(5)既能与强酸又能与强碱反应的金属单质是
(6)最高价氧化物的水化物中酸性最强的酸是 (写化学式)
(7)气态氢化物的稳定性:H2S HCl(填“>”、“=”或“<”);
(8)Al2O3中铝元素与氧元素的质量比是 ,氧元素质量分数为
X~R是元素周期表中的短周期元素,其性质或结构信息如下表:
| 元素 |
X |
Y |
Z |
W |
R |
| 性质 信息 |
能形成+7价的化合物 |
日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 |
通常状况下能形成短周期中最稳定的双原子分子 |
焰色反应为黄色 |
位于第IVA,是形成化合物种类最多的元素 |
请用化学用语回答下列问题:
(1)X在元素周期表中的位置是_______。
(2)元素W的离子结构示意图为_________。
(3)元素R的最高价氧化物的电子式为_________。
(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型为_____,_____。
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是 。(用离子方程式表示)
(6)W的氢氧化物是重要的基本化工原料。写出工业上制取该氢氧化物的离子反应方程式_____。
短周期元素Q、R、T、W在元素周期表中的位置如图所示,期中T所处的周期序数与主族序数相等,请回答下列问题:
(1)T的原子结构示意图为_______。
(2)元素的非金属性为(原子的得电子能力):Q______W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_____。
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氯气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是__________。
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的 =________(注:题中所设单质均为最稳定单质)。
=________(注:题中所设单质均为最稳定单质)。
(15分)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 |
IA |
|
0 |
|||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
|
|
|
② |
③ |
④ |
|
|
| 3 |
⑤ |
|
⑥ |
⑦ |
|
⑧ |
⑨ |
|
(1)画出元素⑦的原子结构示意图_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是____________(填化学式)
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:___________。
(4)写出元素③的气态氢化物与其最高价含氧酸的离子方程式_______________
写出元素②的单质与元素⑧最高价含氧酸浓溶液的反应化学反应方程式__________
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为_____________________________,
(选考)【化学——物质结构与性质】
W、Q、R、X、Y、Z六种元素的原子序数逐渐增大。已知W原子1s轨道上只有一个电子,Q、X原子p轨道的电子数分别为2和4,Z的原子序数为29,除Z外均为短周期主族元素,Y原子的价电子排布为(n+1)sn(n+1)pn。请回答下列问题:
(1)Q和W能形成一种化合物的相对分子质量为28,则该化合物的中心原子采取的杂化轨道类型是 ,该分子中含有____个 键。
键。
(2)Z原子的核外电子排布式为 ;向Z的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中Z的离子与NH3之间的化学键为 。
(3)这六种元素中,电负性最大与最小的两种非金属元素形成的晶体属于____晶体;W、Q、X三种元素之间可以形成多种化合物,其中邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,理由是 。邻甲基苯甲醛分子中碳原子轨道的杂化类型为 。1 mol 苯甲醛分子中σ键为 mol。
(4)元素X的阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。
该晶体中阳离子和阴离子个数比为____,晶体中每个Xn-被 个等距离的C+离子包围。
Ⅰ.下表为元素周期表的一部分:
| 族 周期 |
|
|
|
|||||
| 1 |
① |
|
|
|
|
|
|
|
| 2 |
|
|
|
|
|
② |
|
|
| 3 |
③ |
|
|
④ |
|
⑤ |
⑥ |
|
用化学用语回答下列问题:
(1)写出元素④在周期表中的位置____________________。
(2)②、③、⑤的原子半径由大到小的顺序为____________________。
(3)②与⑤元素氢化物的沸点由高到低_____________________。
(4)①、②、③、⑥中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:____________________。
Ⅱ.已知下图是常见元素形成的单质或化合物A、B、C、D、E、X转化关系(部分生成物和反应条件略去)
(1)若E为氧化物
①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为 。
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为 。
(2)若E为单质气体,D为白色沉淀,A的化学式可能是 。
X、Y、Z、R、W是原子序数依次增大的五种短周期主族元素。X的单质为密度最小的气体,Y是地壳中含量最多的元素,Y和R同主族,可组成共价化合物RY2,Z能与冷水剧烈反应生成一种可燃性气体,X在W中燃烧,产物溶于水得到一种强酸。请回答下列问题:
(1)R在周期表中的位置是________,Z、R、W三种元素最高价氧化物对应的水化物中,酸性最强的是________。(填化学式)
(2)X、Y、Z两种或三种元素组成的化合物中,既含有共价键又含有离子键的有 、 。(填化学式)
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是____________(填化学式)。此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为_______________________________。
(4)Y、Z、R三种元素组成的盐,R的质量分数为40.5%,其水溶液与W单质反应的离子反应方程式为____________________________________________。
W、X、Y、Z四种元素的原子序数依次增大。其中Y原子的L电子层中,成对电子与未成对电子占据的轨道数相等,且无空轨道;X原子的L电子层中未成对电子数与Y相同,但还有空轨道;W、Z的原子序数相差10,且Z原子的第一电离能在同周期中最低。
(1)写出下列元素的元素符号:W ,X ,Y ,Z 。
(2)XW4分子中,中心原子属于 杂化,分子的空间构型为 ;
根据电子云重叠方式的不同,分子里共价键的主要类型为 。
(3)写出Y原子价层电子的排布图
(4)X的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
【化学-选修3:物质结构与性质】
(1)I.短周期某主族元素M的电离能情况如图(A)所示,则M元素位于周期表的第____族;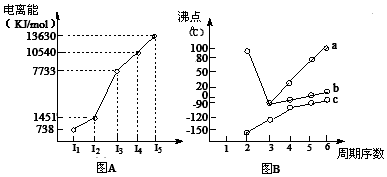
II.图B折线c可以表达出第_________族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:__________(填“a”或“b”);
III.部分有机物的熔沸点见下表: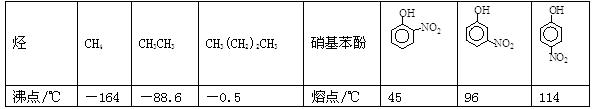
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):____________________;
(2)COCl2俗称光气,分子中C原子采取________杂化成键;其中碳氧原子之间共价键含有______(填字母):
a.2个σ键
b.2个π键
c.1个σ键.1个π键;
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为________________________________;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的2/3,
则绿色晶体配合物的化学式为_________________________。
X、Y、Z、W是四种常见的短周期主族元素,核电荷数依次增大。X有三种同位数,其中有两种常用于制造氢弹。Y、Z是同周期相邻元素,Y的最简单氢化物常用作致冷剂,Z的一种氢化物分子呈V型结构,其沸点远高于同族其它稳定的氢化物,Z的另一种氢化物M分子中两种元素的原子个数比为1︰1;W的最高正价与最低负价的代数和与Z原子的L层电子数相等。请回答下列问题:
(1)X在周期表中的位置_____________________;
(2)写出X、Y、W形成离子化合物的电子式_________,Y的最简单氢化物分子呈____________型;
(3)Y的最简单氢化物与最高价氧化物对应的水化物形成的盐R,R是一种常见的化肥和炸药,R可以促进水的电离,水溶液显_______性(填“酸”或“碱”),溶液中各种离子浓度的大小顺序是_________________;
(4)XYZ3溶液和XWZ4溶液均有强氧化性,写出
①铜与XYZ3浓溶液反应的离子方程式__________________________。
②XWZ4溶液与适量SO2反应的离子方程式______________________________。
(5)由Y、W两种元素组成的一种化合物Q分子中,每个原子最外层均达到8电子稳定结构,该物质在工业生产中被用于面粉的漂白和杀菌,写出Q与水初步反应的化学方程式:__________________。
(12分)食盐是重要调味品,随着对饮食健康的重视,出现了各种类型的特种食盐。
(1)常说“饮食过咸会伤骨”,长期摄入食盐过多可能导致骨骼脱钙,下列物质中,可以作为补钙药品主要成分的是 (填标号)。
| A.CaCO3 | B.CaO | C.Ca(OH)2 | D.Ca |
(2)低钠盐因含有氯化钾和硫酸镁可防治高血压和心血管病,往其溶液中滴入氨水,发生反应的化学方程式是 。
(3)加硒盐中含有的硒元素是人体微量元素中的“抗癌之王”,写出证明硒元素非金属性比硫元素弱的一个实验事实: 。
(4)加碘盐可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,1mol KIO3被还原时,转移电子 mol,该反应的离子方程式为 。
(11分)元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素。Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,其空间构型为v形,W的基态原子3d轨道有8种运动状态不同的电子。请回答下列问题:
(1)Z在周期表中的位置 ;W基态原于的价电子排布图 。
(2)X、Y、Z、Q中,基态原子第一电离能最大的是 (填元素符号)。
(3)在XQ—中Q的杂化类型为 X的氧化物(X2O)晶体结构示意图如下,则1molX2O晶体含有 mol氢键。
(4)ZY3有较强的还原性,遇到NaClO溶液时有无污染的气体生成,其化学方程式为