(9分)下表是元素周期表的一部分。表中所列的数分别代表某一种化学元素。
| |
|
|
|||||||||||||||
| |
|
|
|
① |
② |
|
③ |
|
|||||||||
| |
④ |
⑤ |
|
|
⑥ |
⑦ |
⑧ |
||||||||||
| ⑨ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑩ |
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)表中①-⑩化学性质最不活泼的元素,其原子结构示意图为 。
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的氧化物与⑨最高价氧化物的水化物反应的离子方程式 。
(3)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填化学式)。
(4)③、⑦、⑩的氢化物沸点最低的是 (填化学式)。③元素与⑩元素两者核电荷数之差是 。
(5)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。
可供选择的试剂:氯水、溴水、酒精、淀粉、CCl4、NaCl溶液、NaBr溶液。
| 实验步骤 |
实验现象与结论 |
| |
|
A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质。它们之间的转化关系如图②所示。
请回答下列问题:
(1)Z的化学式为___________。乙的结构式为 。
(2)B的最高价氧化物的电子式为 。
(3)用电子式表示A元素和E元素形成化合物的过程:____________________________。
(4)G的单质与水反应的离子方程式的________________________________________。
(5)F的单质与E的最高价氧化物的水化物反应的离子方程式为 。
(6)W空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。W空气燃料电池放电时负极反应式为________________________________。
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第___________周期第___________族。
(2)E元素形成的氧化物对应的水化物的化学式为________________。
(3)元素C、D、E形成的离子半径大小关系是________>________>__________(用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程________________________。C、D还可形成化合物D2C2,D2C2含有的化学键是__________________。
(5)由A、B、C三种元素形成的离子化合物的化学式为______________,它与强碱溶液共热,发生反应的离子方程式是____________________。
(6)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为______________________(化学式用具体的元素符号表示)。
(6分)现代科技的高度快速发展离不开C和Si元素。
(1)写出Si的基态原子核外电子排布式__________________。
(2)从电负性角度分析,C、Si、O元素的非金属活泼性由强至弱的顺序为______。
(3)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为_____,微粒间存在的作用力是_______。
(4)C、Si为同一主族的元素,CO2、SiO2的化学式相似,但结构和性质有很大的不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成上述π键,而Si、O原子间不能形成上述π键:_________________________
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍。下列说法正确的是
| A.X的氢化物溶于水显酸性且稳定性弱于HF |
| B.Y的氧化物是离子化合物,Y的氢氧化物碱性比氢氧化钠弱 |
| C.Z的氢化物的水溶液在空气中存放不易变质 |
| D.X和Z的最高价氧化物对应的水化物都是弱酸 |
短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等。它们的最高价氧化物的水化物依次为甲、乙、丙、丁。下列叙述不正确的是: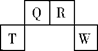
| A.R的氧化物在空气中与其它物质作用可形成光化学烟雾 |
| B.常温下丁的浓溶液可用T单质所制的容器来盛装 |
| C.丁的浓溶液与Q的单质加热发生反应,可生成体积比为1:2的两种气体 |
| D.甲、乙、丙、丁受热均易分解 |
如下表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是: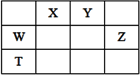
| A.X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B.由X、Y和氢三种元素形成的化合物中一定只有共价键 |
| C.W、X、Z三种元素最高价氧化物对应水化物的酸性逐渐减弱 |
| D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
下表是元素周期表中的一部分,表中所列字母分别表示一种元素。(选项中的物质都由下表中的元素组成)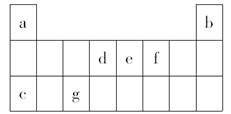
由以上信息可推断下列说法正确的是:
| A.宇航员在飞船活动舱内会产生d和f组成的气体,吸收这种气体的化合物应该由e和f组成 |
| B.活动舱内还要营造一种适合宇航员生存的人工生态环境,即充入a和f的常见单质 |
| C.c和f以原子个数之比为1:1组成的化合物可用作宇航员所需f单质的来源 |
| D.《阿凡达》中潘多拉星球上存在32b,地球上此元素主要以42b形式存在,32b比42b少一个质子 |
下列说法中,不正确的是:
| A.短周期元素中,最外层电子数是其电子层数两倍的元素共有3种 |
| B.第三周期元素的离子半径大小比较:Cl->S2->Na+>Mg2+>Al3+ |
C.日本福岛核电站释放出的放射性核素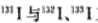 互为同位素 互为同位素 |
| D.相同条件下,测定同浓度的H2CO3溶液和H2SO4溶液的酸性,可比较C和S的非金属性强弱 |
有A、B、C、D四种短周期主族元素,其原子序数依次增大。A、B可形成A2B和A2B2两种共价化合物,B、C同主族且可形成CB2和CB3两种化合物。完成下列问题。
(1)C的名称为________
(2)写出表示非金属性C<D的化学方程式(任一个):________ 。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中,溶液由黄色逐渐变为浅绿色,该反应的离子方程式为______________。
(4)请依据(4)中的反应,设计一个原电池。要求:画出实验装置图,注明电解质溶液名称、正负极及正负极材料,并标出电子移动方向,写出负极反应式。
负极反应式:__________________________________________________________。
(11分)研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)C、Si、N元素的电负性由大到小的顺序是_______________。
(2)A、B均为短周期金属元素。依据下表数据,写出B原子的电子排布式:________。
| 电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
| A |
932 |
1 821 |
15 390 |
21 771 |
| B |
738 |
1 451 |
7 733 |
10 540 |
(3)依据第2周期元素第一电离能的变化规律,参照右图中B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。
(4)基态铜原子的核外电子排布式为________。
(5)基态Si原子中,电子占据的最高能层符号为______,该能层具有的原子轨道数为________、电子数为________。
(10分)五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是________,非金属性最强的是______。(填元素符号)
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是_________(用化学式表示)。
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________,其中存在的化学键类型为________________。
(4)D最高价氧化物的水化物的化学式为________。
(5)单质E与水反应的离子方程式为________________________。
(10分)元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价:
| 元素代号 |
A |
B |
C |
D |
E |
| 原子半径/nm |
0.16 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合物 |
+2 |
+3 |
+6,-2 |
+2 |
-2 |
(1)在下表中标出上述五种元素在元素周期表中的对应位置(用元素符号)。
(2)在下表中表明通常寻找催化剂材料的区域(用斜线阴影)。
(3)A、B、E三种元素各自形成简单离子,其中半径最大的为________(填离子符号)。
(4)证明B元素的单质与A元素的单质在化学性质上有明显不同的离子方程式为:_________________。
(5)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,请写出D的氧化物与强碱溶液反应的离子方程式:________________。
X、Y、Z、W、M、N六种元素均位于元素周期表的前四周期(如下图所示)。有关这六种元素的下列叙述中不正确的是
| A.元素的简单离子半径M<W<Z | B.Y元素在自然界存在多种同素异形体 |
| C.最高价氧化物的水化物酸性W>N | D.N与Z的质子数之差为16 |