已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为__________,该元素的符号是__________;
(2)Z元素位于元素周期表________区,目前该元素发现________种同位素;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为__________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是__________;
(5)X的氢化物与同族第二、第三周期元素所形成的氢化物沸点由高到低顺序是(用化学式表示)______.
回答下问题:
(1)C、N、O三种元素的第一电离能由大到小的顺序是__________________。
(2)C、Si、N的电负性由大到小的顺序是__________________。
(3)氟化氢水溶液中存在的氢键有_________种。
(4)金属镍及其化合物在合金材料以及催化剂等方面应用广泛,Ni的基态原子有________种能量不同的电子。很多不饱和有机物在Ni催化下可以H2发生加成反应。如①CH2=CH2、②HC≡CH、③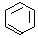 、④HCHO,其中碳原子采取sp2杂化的分子有__________(填物质编号),HCHO分子的立体构型为______________。
、④HCHO,其中碳原子采取sp2杂化的分子有__________(填物质编号),HCHO分子的立体构型为______________。
下列关于原子核外电子排布与元素在周期表中位置关系的表述中,正确的是( )
| A.基态原子的N层上只有一个电子的元素,一定是ⅠA族元素 |
| B.基态原子的价电子排布为(n-1)d6~8ns2的元素一定是副族元素 |
| C.基态原子的p能级上半充满的元素一定位于p区 |
| D.基态原子的价电子排布为(n-1)dxnsy的元素的族序数一定为x+y |
下列化学用语的书写正确的是( )
A.基态Mg原子的核外电子排布图: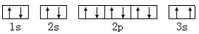 |
B.过氧化氢的电子式: |
| C.As原子的简化电子排布式:[Ar]4s24p3 |
D.羟基的电子式: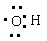 |
按电子排布,可以把周期表中的元素划分成几个区( )
| A.4个 | B.5个 | C.6个 | D.7个 |
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:四种元素的电子层数之和为10,且它们分别属于连续的四个主族;四种元素的原子中半径最大的是X原子.下列说法正确的
| A.四种元素中有两种元素在第二周期 |
| B.W所在主族元素的原子次外层电子数可能为2或8,不可能为18 |
| C.X、Y、Z的最高价氧化物对应的水化物两两之间能反应 |
| D.工业上获得X、Y单质的方法主要是电解其熔融的氯化物 |
根据原子结构及元素周期律的知识,下列推断正确的是
A. Cl2与 Cl2与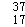 Cl2氧化能力相近,二者互为同位素 Cl2氧化能力相近,二者互为同位素 |
B.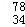 Se与 Se与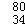 Se所含质子数相同,中子数不同 Se所含质子数相同,中子数不同 |
| C.同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱 |
| D.同周期主族元素形成的简单离子半径随核电荷数的增大而减小 |
分析下表中各项的排布规律,按此规律排布第26项应为
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
| C2H4 |
C2H6 |
C2H6O |
C2H4O2 |
C3H6 |
C3H8 |
C3H8O |
C3H6O2 |
C4H8 |
C4H10 |
A.C7H16 B.C7H14O2 C.C8H18 D.C8H18O
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/pm |
160 |
143 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+3、+5、-3 |
-2 |
下列叙述正确的是
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z从其氢化物中置换出来
短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.化合物YX、ZX2、WX3都是酸性氧化物 |
| B.元素W 的最高价氧化物对应水化物的酸性比Z 的弱 |
| C.原子半径的大小顺序: rY >rZ >rW >rX |
| D.元素X 的简单气态氢化物的热稳定性比W 的弱 |
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:
(1)元素Q的名称为____________,P的基态原子价层电子排布式为____________。
(2)O的氢化物的沸点比其上一周期同族元素的氢化物低,是因为______________。
(3)M、O电负性大小顺序是__________(用元素符号表示),O的最高价含氧酸根的空间构型为__________,其中心原子的杂化类型为__________。
(4)M、N形成的化合物的晶胞如图所示,该晶胞的化学式为__________,其中M离子的配位数为__________,该晶体类型为______________。
(5)该晶胞的边长为a×10-10cm,则距离最近的M、N离子间的距离为__________ 。
合成尿素的反应为: 完成下列填空:
完成下列填空:
(1)写出NH3的电子式 ;画出碳原子结构示意图 ;氧元素位于周期表第 周期第 族。
(2)上述反应所涉及的4种元素,原子半径从大到小的排列顺序为 。
(3)上述反应所涉及的4种元素中,非金属性最强的是 。
(4)一定条件下,在10L的恒容密闭容器中,充入2mol NH3和1mol CO2,反应经5min后达到平衡,测得容器中水蒸气0.6mol,则平均反应速率v(NH3)= mol/(L·min)。
(5)下列能说明上述反应己达平衡的是 。(填序号)
a.2c(NH3)=c(H2O) b.CO2的浓度不变
c.v正(NH3):v正(CO2)=2:1 d.气体的压强不变
(6)为提高氨气的转化率,工业上用该反应生产尿素时,合适的反应条件是 。(填序号)
a.200℃ b.800℃ c.101kPa d.24000kPa
下列情况中不能说明X的非金属性比Y强的是
| A.同主族时X原子的电子层数比Y原子的电子层数少 |
B.X2+H2 2HX ,Y2+H2 2HX ,Y2+H2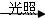 2HY 2HY |
| C.气态氢化物水溶液的酸性X比Y强 |
| D.X的单质能将Y从NaY溶液中置换出来 |
下列说法正确的是
| A.石油裂解、煤的气化、海水制镁等过程中都包含化学变化 |
| B.通过化学变化可以实现235U与238U的相互转化 |
| C.煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 |
| D.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
钚( )是制造威力更大原子弹的良好原料。下列有关说法错误的是
)是制造威力更大原子弹的良好原料。下列有关说法错误的是
| A.原子序数为94 | B.质子数为94 | C.质量数为239 | D.中子数为94 |