NA代表阿伏加德罗常数。已知C2H4和C3H6的混合物的质量为a g,则该化合物
| A.所含共有电子对数目为(3a/14)NA |
| B.所含碳氢键数目为aNA/14 |
| C.完全燃烧时消耗的O2一定是33.6a/14 L |
| D.所含原子总数为aNA/14 |
NA为阿伏加德罗常数的值。下列说法正确的是
| A.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
| B.50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
| C.过氧化钠与CO2反应时,生成0.1mol氧气转移的电子数为0.2NA |
| D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
某实验小组设计实验测定Na2SO4和Na2CO3混合物中各组分的含量。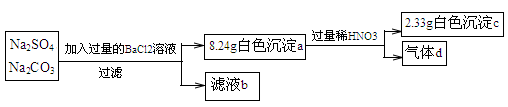
下列说法不正确的是
| A.沉淀a的主要成分是BaSO4和BaCO3 |
| B.滤液b中Na+的物质的量为0.08mol |
| C.气体d在标准状况下的体积为224mL |
| D.原混合物中Na2SO4与Na2CO3的物质的量之比为1:3 |
2015年10月,屠呦呦因发现青蒿素和双氢青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。双氢青蒿素的化学式为C15H24O5,相对分子质量为284。下面关于双氢青蒿素的说法正确的是
| A.1mol双氢青蒿素的质量为284g∙mol-1 |
| B.双氢青蒿素的摩尔质量等于它的相对分子质量 |
| C.14.2g双氢青蒿素中含有的原子总数为2.2NA |
| D.含有6.02×1023个碳原子的双氢青蒿素的物质的量为1mol |
(1)AlCl3溶液与NaOH溶液反应时,当Al3+的物质的量与OH-的物质的量之比(以下均填物质的量之比)为________时,Al(OH)3沉淀量最多。
(2)NaAlO2溶液与盐酸溶液反应时,AlO的物质的量与H+的物质的量之比为________时,Al(OH)3沉淀恰好溶解。
用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )
| A.干燥的 | B.瓶塞不漏水的 |
| C.用待配溶液洗涤过的 | D.以上三项都符合的 |
若NA为阿伏加德罗常数的值,下列说法正确的是
| A.NA个Fe(OH)3胶体粒子的质量为107g |
| B.8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA |
| C.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA |
| D.5.6gFe与0.1mol Cl2完全反应,反应中转移的电子数为0.3NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.54 g Al分别与足量的稀硫酸及氢氧化钠溶液反应失去的电子数都是6NA |
| B.同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等 |
| C.1mol·L-1的MgCl2溶液中,含有Cl-个数为2NA |
| D.11.2L氧气中所含有的原子数为NA |
实验室需要400mL 0.5 mol·L-1的稀硫酸溶液,现用密度为1.84g·mL-1,质量分数为98%浓硫酸来配制,请回答下列问题:
(1)若要实施配制,下列仪器中,不会用到的是 (填字母)。
A 250mL容量瓶;B 500mL容量瓶;C 托盘天平;D 量筒;E 烧杯;F 玻璃棒
(2)配制过程中,除上述仪器外,尚缺的仪器是 。
(3)未冷却至室温立即转移硫酸溶液,则所配硫酸溶液的浓度 (填“偏高”、“偏低”或“无影响”,下同);若定容时,滴加蒸馏水不慎超过了刻度线,则所配硫酸溶液的浓度 。
(4)通过计算,用量筒量取 mL浓硫酸。
(1)MgCl2的摩尔质量是 ;0.1mol CO2在标准状况下体积约是 ;0.2 mol·L-1的Cu(NO3)2溶液中NO3-的物质的量浓度是 。
(2)现有以下物质:①熔融NaCl ②液氨 ③醋酸水溶液 ④HCl气体 ⑤酒精(C2H5OH)。请用相应序号填空:能导电的是 ;属于电解质的是 。
(3)CH3COOH的电离方程式为 。
设NA为阿伏加德罗常数,下列叙述中正确的是
| A.标准状况下,22.4LH2中所含质子数、中子数均为2NA |
| B.46gNO2气体和46gN2O4气体的分子数之比为2∶1 |
| C.1L1mol·L-1的盐酸中所含粒子总数为2NA |
| D.71g氯气与足量铁粉充分反应,转移的电子数为3NA |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.46g乙醇中含有的C—H键的数目为6NA |
| B.0.lmol丙烯酸中含有的双键的数目为0.lNA |
| C.1mol甲基(—CH3)中含有的电子总数为9NA |
| D.标准状况下,22.4L己烷完全燃烧生成的CO2分子的数目约为6NA |
下列是用98%的浓H2SO4(ρ=1.84g/cm3)配制500mL 0.5mol∙L-1的稀硫酸的实验操作,请按要求填空:
(1)实验中量取浓硫酸的体积为_________mL。
(2)如果实验室有10mL、20mL、50mL的量筒,应选_______规格的量筒最好,如果量取浓硫酸时仰视读数,所配溶液浓度将(填“偏高”、“偏低”或“无影响”)__________。
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约少量水的烧杯里,并不断搅拌,搅拌的目的是_____________________。
(4)将冷却至室温的上述溶液沿玻璃棒注入_______中,并用50mL蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液要转入到容量瓶中,并振荡;在转移过程中有少量液体洒在桌子是,则最终所配浓度将(填“偏高”、“偏低”或“无影响”)__________。
(5)加水至距刻度线1~2cm处,改用______加水至刻度线,使溶液的凹液面恰好跟容量瓶刻度线相平,把容量瓶塞好,反复颠倒振荡,摇匀溶液。
下列关于物质的量浓度表述正确的是
| A.0.3mol∙L-1的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.9mol |
| B.当1L水吸收22.4L氨气时所得氨水的浓度不是1mol∙L-1,当22.4L氨气溶于水制得1L氨水时,其浓度才是1mol∙L-1 |
| C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 |
| D.10℃时,100mL 0.35mol∙L-1的KCl饱和溶液蒸发掉5g水,冷却到10℃时,其体积小于100mL。它的物质的量浓度仍为0.35mol∙L-1 |
下列溶液中物质的量浓度肯定是1mol/L的是( )
| A.将40gNaOH固体溶解于1L水中 |
| B.将22.4L氯化氢气体溶于水配成1L溶液 |
| C.将1L10mol/L浓盐酸与10L水混合 |
| D.10gNaOH固体溶解在水中配成250mL溶液 |