江苏省宿迁市高一上学期期末考试化学试卷
化学与生产、生活密切相关,下列表述错误的是
| A.使用新能源,减少化石燃料的燃烧,可防止酸雨的产生 |
| B.明矾在水中能形成胶体,可作为净水剂 |
| C.建设三峡大坝使用了大量水泥,水泥是硅酸盐材料 |
| D.给汽车安装尾气转化装置,易产生光化学烟雾 |
2015年2月朝鲜准备进行第四次核试验,引起国际社会的极大关注。 是一种重要的核燃料,这里的“235”是指该原子的
是一种重要的核燃料,这里的“235”是指该原子的
| A.质子数 | B.中子数 | C.电子数 | D.质量数 |
下图所示的实验操作,不能达到相应目的的是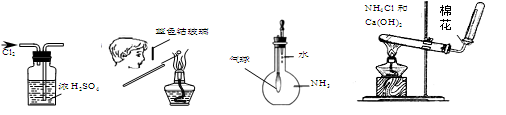
| A.干燥氯气 | B.检验K2CO3中K+ | C.证明NH3极易溶于水 | D.实验室制NH3 |
下列说法正确的是
| A.FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 |
| B.食盐水中Ca2+、SO42-等杂质的去除,应先加Na2CO3溶液,后加BaCl2溶液 |
| C.用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 |
| D.用BaCl2溶液来检验暴露在空气中的Na2SO3样品是否变质 |
设NA为阿伏加德罗常数,下列叙述中正确的是
| A.标准状况下,22.4LH2中所含质子数、中子数均为2NA |
| B.46gNO2气体和46gN2O4气体的分子数之比为2∶1 |
| C.1L1mol·L-1的盐酸中所含粒子总数为2NA |
| D.71g氯气与足量铁粉充分反应,转移的电子数为3NA |
下列关于物质用途的叙述中不正确的是
| A.纯碱可用于治疗胃酸过多的药剂 |
| B.铝制容器可用于常温下贮存、运输浓硫酸 |
| C.二氧化硅可用于制造光导纤维和石英坩埚 |
| D.过氧化钠可用作漂白剂和呼吸面具中的供氧剂 |
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
| |
现象 |
解释 |
| A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
Cl2能与淀粉发生显色反应 |
| B |
SO2能使酸性高锰酸钾溶液褪色 |
SO2具有还原性 |
| C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有SO42- |
| D |
铁与稀硝酸反应有气泡产生 |
铁与稀硝酸发生了置换反应 |
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在的较多的阳离子是
| A.Cu2+ | B.Fe3+ | C.Fe2+ | D.H+ |
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随加入氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为
| A.2∶1 | B.4∶1 | C.1∶1 | D.1∶2 |
常温下,下列各组离子在指定溶液中可能大量共存的是
| A.FeCl3溶液中:K+、Na+、SO42-、SCN- |
| B.使酚酞试液变红的溶液中:NH4+、Na+、HCO3-、NO3- |
| C.漂白粉溶液中:K+、Na+、I-、CO32- |
| D.与铝反应产生氢气的溶液中:Na+、K+、CO32-、OH- |
下列离子方程式正确的是
A.钠投入到水中2Na+2H2O 2Na++2OH-+H2↑ 2Na++2OH-+H2↑ |
B.氯化铵溶液与浓NaOH溶液加热NH4++OH- NH3·H2O NH3·H2O |
C.氯化铝溶液中滴入过量氨水Al3++3NH3·H2O Al(OH)3↓+3NH4+ Al(OH)3↓+3NH4+ |
D.铁片插入氯化铁溶液中Fe+Fe3+ 2Fe2+ 2Fe2+ |
2.56gCu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标况),则反应消耗HNO3物质的量为
| A.0.05 mol | B.1mol | C.0.13mol | D.1.05mol |
(1)MgCl2的摩尔质量是 ;0.1mol CO2在标准状况下体积约是 ;0.2 mol·L-1的Cu(NO3)2溶液中NO3-的物质的量浓度是 。
(2)现有以下物质:①熔融NaCl ②液氨 ③醋酸水溶液 ④HCl气体 ⑤酒精(C2H5OH)。请用相应序号填空:能导电的是 ;属于电解质的是 。
(3)CH3COOH的电离方程式为 。
我国政府为了消除碘缺乏病,规定在食盐中必须加人适量的碘酸钾。检验食盐中是否加碘,可利用如下反应: KIO3 + KI + H2SO4  K2SO4 + I2 + H2O
K2SO4 + I2 + H2O
(1)将上面氧化还原反应的化学方程式配平。
(2)该反应中氧化剂和还原剂的物质的量之比为 。
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为
(4)若要提取生成的碘,所用的萃取剂可以是 (填序号)。
①水 ②酒精 ③淀粉溶液 ④苯
(5)加碘食盐不能长时间炖炒,且应避热保存,主要原因是 。
下图是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质,G、J的焰色均为黄色。反应①为炼铁高炉中的重要反应;反应②可用于焊接铁轨。

请回答下列问题:
(1)B的化学式为 ,J的化学式为 。
(2)工业上将氯气通入石灰乳中制取漂白粉,该反应的化学反应方程式为 。
(3)D→G是侯氏制碱法的主要反应,该反应的化学方程式为 。
(4)K→H是制作印刷电路板的重要反应,该反应的离子方程式为 。
(5)F→L是铝土矿提纯中的重要反应,该反应的离子方程式为 。
某化学兴趣小组为探究浓硫酸的性质,设计了如下图所示的装置进行实验。
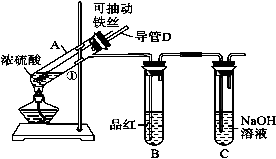
(1)用“可抽动的铁丝”代替“直接投入铁片”的优点是 。
(2)说明SO2气体产生的实验现象是 ;装置C的作用是 。
(3)反应一段时间后,他们对试管A中溶液的金属离子进行探究,请完成相关试题:
①提出假设: 假设1:只含有Fe3+;
假设2:只含有Fe2+;
假设3:既有Fe2+,又有Fe3+。
②请设计实验方案验证假设3。
限选试剂:稀硫酸、KMnO4溶液、KSCN溶液、NaOH溶液、H2O2溶液。
| 实验步骤 |
预期现象 |
| 步骤一:用胶头滴管取出A试管中的溶液,用水稀释后,并分装在试管Ⅰ、Ⅱ中备用 |
 |
| 步骤二:检验Fe3+,往试管Ⅰ中, |
|
| 步骤三:检验Fe2+,往试管Ⅱ中, |
|
(4)已知C+2H2SO4(浓)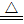 2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的 性。
2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的 性。
A.脱水性 B.强氧化性 C.吸水性
若要验证反应产物中同时混有SO2气体和CO2气体,可选择以下试剂进行实验:
①NaOH溶液②品红溶液③溴水④Ca(OH)2溶液,选择合适试剂并安排合理的顺序为 。
实验室需要400mL 0.5 mol·L-1的稀硫酸溶液,现用密度为1.84g·mL-1,质量分数为98%浓硫酸来配制,请回答下列问题:
(1)若要实施配制,下列仪器中,不会用到的是 (填字母)。
A 250mL容量瓶;B 500mL容量瓶;C 托盘天平;D 量筒;E 烧杯;F 玻璃棒
(2)配制过程中,除上述仪器外,尚缺的仪器是 。
(3)未冷却至室温立即转移硫酸溶液,则所配硫酸溶液的浓度 (填“偏高”、“偏低”或“无影响”,下同);若定容时,滴加蒸馏水不慎超过了刻度线,则所配硫酸溶液的浓度 。
(4)通过计算,用量筒量取 mL浓硫酸。
氮氧化物进入大气后,可能会形成硝酸型酸雨,因此必须对含有氮氧化物的废气进行处理。
(1)用NaOH可以吸收废气中的氮氧化物,反应的化学方程式如下:2NO2 + 2NaOH  NaNO2 + NaNO3 + H2O 反应中,还原剂是 ,NO2 + NO + 2NaOH
NaNO2 + NaNO3 + H2O 反应中,还原剂是 ,NO2 + NO + 2NaOH  2NaNO2 + H2O 反应中,氧化产物和还原产物之比为 。
2NaNO2 + H2O 反应中,氧化产物和还原产物之比为 。
(2)NO2和Br2蒸汽都是红棕色气体,下列可以用来鉴别这两种气体的试剂是 。
| A.用氢氧化钠溶液 | B.淀粉碘化钾溶液 | C.用硝酸银溶液 | D.用蒸馏水 |
(3)汽车尾气中含有一氧化氮和一氧化碳,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成两种对大气无污染的气体,该反应的化学方程式为 。
(4)氨气也可用来处理氮氧化物,例如:氨气与二氧化氮反应生成氮气和水,写出该反应的化学方程式: ,若某工厂排出的废气中二氧化氮含量为0.5%(体积分数),处理1000m3(标准状况)这种废气,需要 千克氨气。(结果保留两位小数)

 粤公网安备 44130202000953号
粤公网安备 44130202000953号