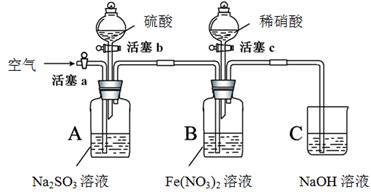
某小组同学为比较酸性条件下NO3-、SO42-、Fe3+的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
实验记录如下:
| |
实验操作 |
实验现象 |
| I |
打开活塞c,将过量稀HNO3加入装置B中,关闭活塞c |
B中浅绿色溶液立即变为深棕色;一段时间后,溶液最终变为黄色。 |
| II |
用注射器取出少量B装置中的溶液,加入KSCN溶液 |
溶液变为红色。 |
| III |
打开活塞b,向A装置中加入足量硫酸,关闭活塞b |
A中产生气体;B中有气泡,液面上有少量红棕色气体生成。 |
| IV |
一段时间后,用注射器取出少量B装置中的溶液,…… |
…… |
| V |
打开活塞a,通入一段时间空气 |
———— |
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2+ + NO [Fe(NO)]2+
[Fe(NO)]2+
用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。
有下列三个反应:①Cl2+FeI2=FeCl2+I2 ②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O,下列说法正确的是
| A.①②③中的氧化产物分别是I2、Fe3+、CoCl2 |
| B.根据以上方程式可以得到氧化性Cl2>Fe3+>Co2O3 |
| C.可以推理得到Cl2+FeBr2=FeCl2+Br2 |
| D.在③反应中生成1 mol Co2O3参加反应时,有2 mol HCl被氧化 |
臭氧具有强氧化性,可使湿润的碘化钾淀粉试纸变蓝,有关反应如下:
O3 + 2KI + H2O =" 2KOH" + I2 + O2,对于此反应下列说法正确的是
| A.反应中O3是氧化剂,H2O和KI是还原剂 |
| B.在反应中,每消耗1molO3转移2mol电子 |
| C.氧化产物I2和还原产物O2的物质的量之比为1∶1 |
| D.由此反应可知,氧化性强弱顺序为O3>I2>O2 |
有A、B、C、D四种物质,已知它们能发生下列变化:
①A2++B===B2++A ②A2++C===C2++A
③B2++C===C2++B ④C2++D===D2++C
由此可推知,各物质的氧化性、还原性强弱顺序正确的是
A.氧化性:A2+>B2+>C2+>D2+
B.氧化性:D2+>C2+>B2+>A2+
C.还原性:A>B>C>D
D.还原性:D>B>A>C
Ⅰ.过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。回答下列有关双氧水的问题:
(1)下述反应中,H2O2仅体现氧化性的反应是(填代号) 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(2)保存过氧化氢的试剂瓶上最适合贴上的一个标签是 (填代号)。
A.自燃物品 B.氧化剂 C.剧毒品 D.腐蚀品
Ⅱ某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下:
实验①:在淀粉KI溶液中加入少量NaClO溶液,并加入少量的稀H2SO4,溶液立即变蓝;
实验②:向实验①的溶液中加入4 L 0.5 mol/L的Na2SO3溶液,发生反应如下
SO32-+ I2+H2O→SO42-+I-+H+(未配平),恰好完全反应。
(1)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是 。
(2)实验②中化学反应转移电子的物质的量是 。
(3)写出实验①中发生反应的离子方式 。
某同学以反应2Fe3++2I- 2Fe2++I2为原理,研究浓度对氧化还原性和平衡移动的影响。实验如下图:
2Fe2++I2为原理,研究浓度对氧化还原性和平衡移动的影响。实验如下图:
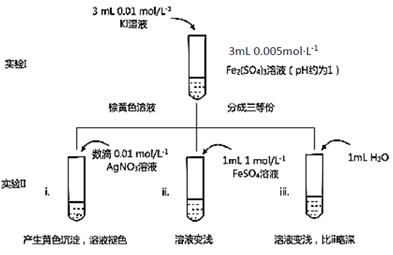
(1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到 。
(2)iii是ii的对比试验,目的是排除有ii中 造成的影响。
(3)i和ii的颜色变化表明平衡逆向移动,Fe2+向Fe3+转化。用化学平衡移动原理解释原因: 。
(4)根据氧化还原反应的规律,该同学推测i中Fe2+向Fe3+转化的原 因:外加Ag+使c(I-)降低,导致I-的还原性弱于Fe2+,用右图装置(a、b均为石墨电极)进行实验验证。
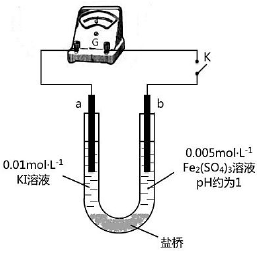
①K闭合时,指针向右偏转,b作 极。
②当指针归零(反应达到平衡)后,向U型管左管滴加0.01 mol·L-1 AgNO3溶液,产生的现象证实了其推测,该现象是 。
(5)按照(4)的原理,该同学用右图装置进行实验,证实了ii中Fe2+向Fe3+转化的原因,
①转化原因是 。
②该实验与(4)实验对比,不同的操作是 。
(6)实验I中,还原性:I->Fe2+;而实验II中,还原性:Fe2+>I-,将(3)和(4)、(5)作对比,得出的结论是 。
已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O72-(橙色)+ H2O 2H++ 2CrO42-(黄色)
2H++ 2CrO42-(黄色)
①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。
②向2 mL 0.1 mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72-+ 14H++ 6Fe2+ 2Cr3+(绿色) + 6Fe3++ 7H2O。下列分析正确的是
2Cr3+(绿色) + 6Fe3++ 7H2O。下列分析正确的是
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
| B.实验②能说明氧化性:Cr2O72- > Fe3+ |
| C.CrO42- 和Fe2+在酸性溶液中可以大量共存 |
| D.稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
(1)通常状况下,已知X、Y两种气体,其质量分别为a、b时,体积之比为2:3。 两种气体X、Y的相对分子质量之比为________;相同条件下的X、Y两种气体,体积相同时,则X、Y的密度之比为__________;相同条件下,同质量的两种气体,X与Y的分子数之比为________。
(2)已知下列反应能发生:
2A3+ + 2B - = 2A2+ + B2;
C2 + 2B- = 2C- + B2;
2A2+ + C2 = 2A3++ 2C-
上述三个反应中氧化剂的氧化性强弱顺序为___________;还原剂的还原性强弱顺序为___________。
(3)一定条件下硝酸铵受热分解的化学方程式为: NH4NO3→HNO3+N2↑+H2O(未配平),写出配平后的化学方程式:________________________。在反应中被氧化与被还原的氮原子数之比为
(4)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是( )
| A.野火烧不尽,春风吹又生 |
| B.春蚕到死丝方尽,蜡炬成灰泪始干 |
| C.粉身碎骨浑不怕,要留清白在人间 |
| D.爆竹声中一岁除,春风送暖入屠苏 |
水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。
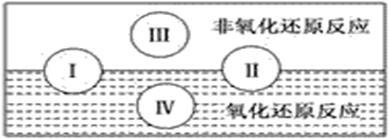
试写出有水参加的符合反应类型Ⅳ的一个化学方程式___________________________
已知常温下,在溶液中发生如下反应,由此推断下列说法正确的是
①16H++10Z-+2XO4-=2X2++5Z2+8H2O;②2A2++B2=2A3-+2B-; ③2B-+Z2=B2+2Z-
| A.Z元素在反应①中被还原,在反应③中被氧化 |
| B.反应Z2+2A2+=2A3++2Z-可以进行 |
| C.氧化性由弱到强的顺序是XO4-,Z2,B2,A3+ |
| D.还原性由弱到强的顺序是Z-,B-,A2+,X2+ |
根据下列反应:2Fe3++2I-=2Fe2++I2,Br2+2Fe2+=2Br-+2Fe3+,判断微粒的氧化性从强到弱的顺序是( )
| A.Fe3+、Br2、I2 | B.I2、Br2、Fe3+ | C.Br2、Fe3+、I2 | D.Br2、I2、Fe3+ |
已知反应:①Cl2+2KBr=2KCl+Br2 , ②KClO3+6HCl=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3,下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.氧化性由强到弱顺序为Cl2>Br2>KBrO3>KClO3 |
| C.反应②中还原剂与氧化剂的物质的量之比为5:1 |
| D.反应③中1 mol KBrO3参加反应时有10 mol电子转移 |
已知反应:①Cl2+2KBr=2KCl+Br2 ;
②KClO3+6HCl=3Cl2↑+KCl+3H2O;
③2KBrO3+Cl2=Br2+2KClO3下列说法正确的是( )
| A.氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2 |
| B.①中KCl是氧化产物,KBr 发生还原反应 |
| C.③中1mol氧化剂参加反应得到电子的物质的量为2mol |
| D.反应②中氧化剂与还原剂的物质的量之比为1:6 |
已知:2BrO3-+Cl2=Br2 +2ClO3-;5Cl2 +I2 +6H2O =2HIO3 +10HCl;
ClO3-+5Cl-+6H+ =3Cl2+3H2O判断下列物质氧化能力强弱顺序为
| A.ClO3->BrO3->IO3->Cl2 | B.BrO3->Cl2>ClO3->IO3- |
| C.BrO3->ClO3->Cl2>IO3- | D.Cl2>BrO3->ClO3->IO3- |
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是 ( )
①I2 + SO2 + 2H2O = H2SO4 + 2HI;
② 2FeBr2 + Br2 = 2FeBr3;
③2FeCl3 + 2HI = 2FeCl2 + 2HCl+I2
| A.SO2>I->Fe2+>Br- | B.Br->Fe2+>SO2>I- |
| C.Fe2+>I->Br->SO2 | D.I->Fe2+>Br->SO2 |