化学变化的本质特征是有新物质生成,化学变化中的一些现象有助于我们判断物质是否发生了化学变化,
分析一:化学变化中的现象
实验内容 |
实验现象 |
实验分析 |
(1) 木炭在氧气中燃烧 |
发出白光,发出热量 |
燃烧是 的剧烈的化学反应 |
(2) |
镁表面 铜无明显变化 |
镁与稀盐酸反应,铜不与稀盐酸反应 |
(3) |
产生白色沉淀 |
该反应的化学方程式
|
(4) |
玻璃管内的固体由红棕色变为 色 |
发生了化学变化 |
22444244的混合溶液)结合已有知识,进行大胆猜想:
(1)现象及可能产生该现象的依据
(2)现象及可能产生该现象的依据 。
根据表中信息,请回答下列问题。
测试类别 S化合价 |
氢化物 |
单质 |
① |
酸 |
盐 |
+6 |
﹣ |
﹣ |
3 |
24 |
2444424 |
② |
﹣ |
﹣ |
2 |
23 |
23 |
0 |
﹣ |
S |
﹣ |
||
﹣2 |
2S |
﹣ |
﹣ |
2S |
2S |
(1)填写表中内容:① ;② 。
(2)物质可以按照一定规律发生转化,请按要求各写出一个对应的化学方程式。
①置换反应 ;②复分解反应 。
424是农业上常用的铵态氮肥,在实验室检验其为铵态氮肥的实验操作是______(写出一种即可)
222O,反应前后硫元素化合价发生的变化是
(5)在实验室中,可用热的碱液除去试管内壁上附着的硫,请完成该反应的化学方程式: S+ NaOH═ 23+ + 2O。
有一包白色固体可能含氯化钠、碳酸钙、硝酸铵、氯化钡和硫酸钠中的一种或几种,实验小组设计如下实验方案,检验白色固体的成分(假设实验中每一步均恰好完全反应)。
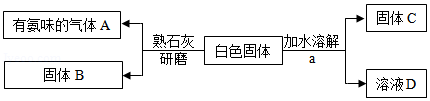
回答下列问题:
(1)a处的操作是 。
(2)气体A的化学式是 。
(3)硝酸铵在农业上常用作 肥。
(4)若固体C中加入稀硝酸,有一部分溶解则原粉末的成分中一定有 。
(5)若固体C中加入稀硝酸,固体不溶解,写出生成固体C的化学反应方程式 ,化学反应基本类型为 。
金属材料与人类的生产、生活密切相关。
(1)大自然向人类提供了丰富的金属矿物资源,其中提取量最大的是铁。工业上利用赤铁矿石炼铁的原理是 (用化学方程式表示)。实验室用的铁架台是铁的合金制成,合金比纯的金属硬度、强度更高, 也更好。用久的铁架台有一些出现锈迹,学校要对这些铁架台进行除锈,防锈处理,写出除去铁锈所发生的化学反应方程式 ,从实际考虑,学校应对这些除锈后的铁架台做 的防锈处理。
(2)为了比较铜、锌、铁三种金属的活动性强弱,可以将打磨光亮的两根铁丝分别插入 的溶液中,能判断出三种金属的活动性由强到弱的顺序是 。
随着人们生活水平的提高,汽车已经走进千家万户.
(1)在汽车电路中,经常用铜做导线,这是利用铜的延展性和 性.
(2)车体多用钢材制造,钢铁厂用赤铁矿为原料炼铁的原理是(用化学方程式表示) .
(3)为减少汽油燃烧产生的废气对环境的污染,我国开发推广使用一种车用乙醇汽油,其中含乙醇10%.请写出乙醇在空气中完全燃烧的化学方程式 .
对知识的归纳和总结是学习好化学的重要方法。在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图所示),即氢氧化钙与图中四类物质能够发生化学反应。
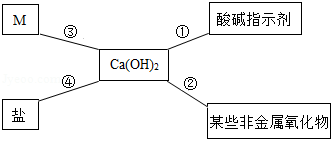
(1)图中M所属的物质类别是 。
(2)氢氧化钙可由生石灰和水反应制得,该放应能 (填"吸收"或"放出")热量。
(3)利用图中氢氧化钙能与 反应的性质,可以解释"用石灰浆粉刷墙壁,干燥后墙壁就变硬了"的现象。
(4)利用图中④氢氧化钙和盐反应的性质,除去氢氧化钠溶液中少量的氢氧化钙杂质。请写出该反应的化学方程式 。
金属材料是重要的资源,在日常生活中已经得到越来越广泛的应用。
(1)将铝片和硬铝片相互刻画,铝片上留下明显的划痕,说明 。
(2)沙漠地区的铁制品锈蚀较慢,其原因是 。
(3)为了比较铁、铜、银三种金属的活动性顺序强弱,某同学设计了下列四种方案:
①将铁丝、银丝分别浸入硫酸铜溶液中;②将银丝分别浸入到硫酸亚铁、硫酸铜溶液中;
③将铜丝、银丝分别浸入到硫酸亚铁溶液中;④将铜丝分别浸入到硫酸亚铁、硝酸银溶液中其中可行的方案是 (填序号)。可行方案中发生的基本反应类型为 。
(4)工业上将赤铁矿石冶炼成铁是一个复杂的过程。炼铁高炉中发生的主要反应有:
①高温下一氧化碳将铁矿石还原为铁;②高温煅烧石灰石;③灼热的焦炭和二氧化碳的反应;④焦炭充分燃烧,其中体现焦炭作用的反应是 (填序号)。
通过一年的化学学习,我们学会了从微观角度认识物质。
(1)如图是部分原子的结构示意图请回答问题:
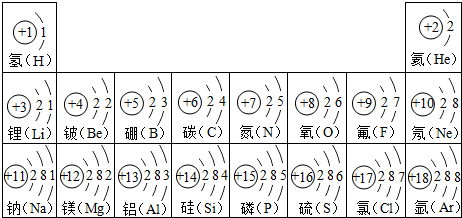
①化学上将质子数为 的所有氯原子统称为氯元素。
②8号元素和地壳中含量最多的金属元素组成的化合物中,金属元素的化合价为 。
③在化学反应中,11号元素的原子易 电子。
(2)如图是氢气在氯气中燃烧生成氯化氢的微粒示意图。
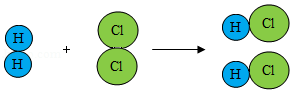
请据图回答:
①氢气可压缩储存于钢瓶中,因为受压时氢气分子之间的 减小。
②从微观的角度解释该化学变化的实质是 。
请你铵要求回答下列问题:
(1)阜新"宝地斯帕温泉"远近闻名。若要检验温泉水是硬水还是软水,可加入 检验。
(2)电解水的实验证明了水的组成。电解水的化学方程式为 。
(3)在做"细铁丝在盛有氧气的集气瓶中燃烧"的实验时,常常要在集气瓶里预先加少量的水,这样做的目的是 。
(4)为了设计实验证明二氧化碳能溶于水,某同学做了如图所示实验,该实验的现象是 。
(5)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+2O 2  CO 2+2H 2O,则X的化学式为 。
CO 2+2H 2O,则X的化学式为 。
(6)氯化钠是食盐的主要成分,氯化钠的用途很多。例如,生活中的氯化钠是常用的调味品。此外,还可以利用氯化钠 等。

一班的同学在探究金属镁的化学性质时发现,将镁条放到盛有冷水的试管中,没有明显的现象,然后将试管放在酒精灯上加热,发现试管中有气泡产生。
(1)小明认为,据此现象可断定加热时镁能和水反应,小强认为小明的结论不正确,理由是 。
(2)小明向加热的试管中滴入酚酞溶液,溶液显红色,证明镁在加热时 (填“能”或“不能”)与水发生反应
(3)小明将加热后的试管放置在空气中一段时间后,同学们发现溶液中的红色消失了。
在确定酚酞溶液没有变质的情况下,请你根据初中所学化学知识,对溶液中红色消失的原因做出合理猜想。
猜想一:
猜想二:
请设计实验方案,对其中一种猜想进行验证 。(只需答出实验方案,不需要回答现象和结论)
海洋中有丰富的水生生物和化学资源。海水晒盐能得到粗盐和苦卤,粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。请回答下列问题。
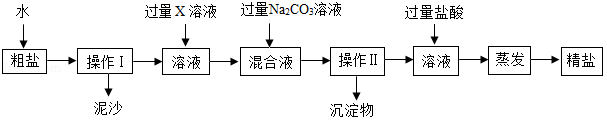
(1)蒸发过程中使用到玻璃棒,其作用是 。
(2)若要去除粗盐中可溶性的杂质氯化镁和氯化钙,可依次加入过量的X和碳酸钠两种溶液。下列物质中,可作为X的物质有 。
A、KOH
B、Ba(OH) 2
C、Ca(OH) 2
D、NaOH
(3)操作Ⅱ后向所得滤液中加入适量的盐酸,其目的是 ,最后通过蒸发结晶得到较为纯净的氯化钠。
根据如图图示回答下列问题:
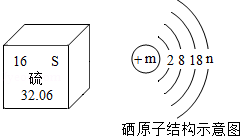
①从图中不能直接获取的信息是 。
A.硫属于非金属元素 B.硫的核外电子数为16
C.硫的相对原子质量为32.06 D.硫元素形成的单质有还原性
②根据硫原子的最外层电子数,推出硫元素的最低化合价为﹣2价,则硫元素的最高化合价为 价。
③元素周期表中同一主族的元素具有相似的化学性质,例如硒(Se)和S有相似的化学性质,则图中m= 。
初中阶段:物质得氧和失氧的反应是氧化还原反应;高中阶段:凡是有元素化合价升降的化学反应都是氧化还原反应.元素化合价升高的为还原剂,发生氧化反应;元素化合价降低的为氧化剂,发生还原反应;氧化反应和还原反应同时发生的,这样的反应称为氧化还原反应.请回答下列问题:
(1)根据化合价改变判断下列四种基本反应类型,一定不是氧化还原反应的是 .(选填序号)
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(2)下列化学反应中,属于氧化还原反应的是 (选填序号),该反应的还原剂是 (填化学式).
| A. |
Na 2CO 3+CaCl 2═CaCO 3↓+2NaCl |
B. |
Fe+CuSO 4═Cu+FeSO 4 |
| C. |
Ca(HCO 3) 2 |
D. |
CaO+H 2O═Ca(OH) 2 |
(3)下列反应中,氧化反应与还原反应在同一元素中进行的是 .(多选,选填字母序号)
| A. |
Cl 2+2NaOH═NaCl+NaClO+H 2O |
B. |
4P+5O 2 |
| C. |
Zn+CuCl 2═Cu+ZnCl 2 |
D. |
3NO 2+H 2O═2HNO 3+NO. |
在盛有11.9g纯碱样品 ( 含少量氯化钠杂质 ) 的烧杯中加入167.8g水,完全溶解后,再向其中逐滴加入一定质量分数的氯化钡溶液,生成沉淀的总质量与所滴入氯化钡溶液质量关系如图所示:
(1)反应过程中生成沉淀的质量是 g。
(2)在B点时,溶液中含有的溶质是 (写化学式 )
(3)求A点时溶液中的所含溶质质量分数。 写出计算过程

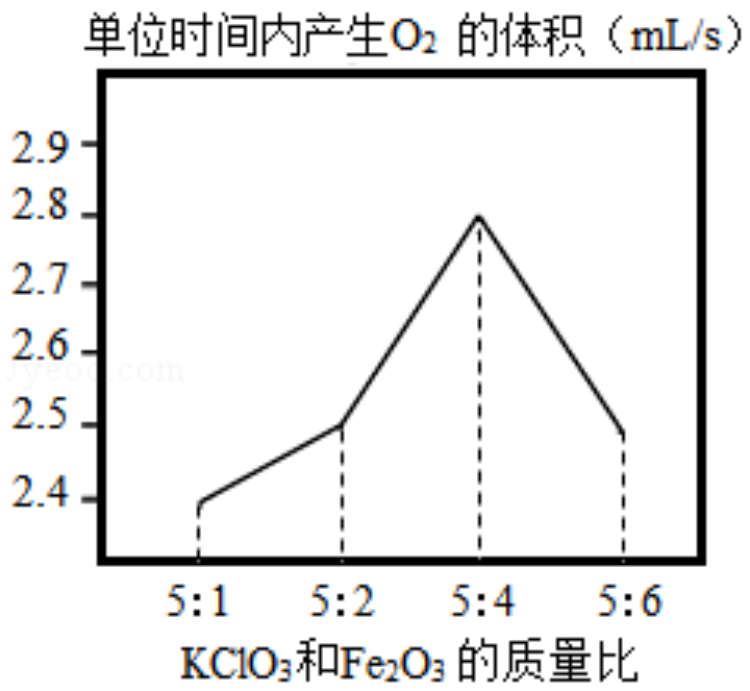
氧气是人类生产活动的重要资源。
( 1 )下列属于 O 2 的化学性质的是 (填标号)。
| A. |
O 2能支持燃烧 |
| B. |
O 2的密度比空气的密度略大 |
| C. |
O 2在低温、高压时能变为液体或固体 |
( 2 )小圳同学进行实验室制备 O 2 的相关探究。
【 查阅 】 他得知在 KClO 3 分解制 O 2 的反应中, Fe 2 O 3 可作催化剂。
【 实验 】 他用电子秤称取 0.49g Fe 2 O 3 和一定量的 KClO 3 ,充分混合后加热至 KClO 3 完全分解,冷却至室温,称得剩余固体的质量为 1.98g 。
【计算】①剩余固体中KCl的质量是 g。
② 该反应生成 O 2 的质量(根据化学方程式写出完整的计算步骤)。
【 思考 】 他发现制备 O 2 较慢,猜测 KClO 3 和 Fe 2 O 3 的质量比可能会影响反应的快慢。
【 探究 】 ③ 他调节 KClO 3 和 Fe 2 O 3 的质量比制备 O 2 ,整理数据绘制出如图,从图中得出 KClO 3 和 Fe 2 O 3 最佳质量比是 。
【 结论 】 ④ 根据质量守恒定律,请你计算出小圳同学在 [ 实验 ] 中称取的 KClO 3 的质量为 g , KClO 3 和 Fe 2 O 3 的质量比是 (填最简比),不是最佳质量比。