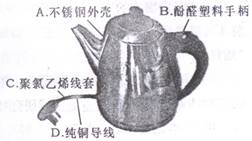
(1)如图是一种家用电热水壶,所用材料属于合金的是___ _________(填字母序号,下同),属于单质的是_____ ______,属于合成材料的是_____ _________。
(2)学习化学需要在宏观物质的性质与其微观结构之间建立联系。1个CO2分子由___ ______构成。在氢氧化钠、氯化钠、硫酸三种物质中,由阴阳离子构成的是_____ ______,这三种物质的水溶液中PH<7的是_____ ______。
(3)A~G七种物质之间具有如下图所示转化关系。已知:A是一种含铁的矿石的主要成分,其中金属与非金属元素的原子个数比为1:2;B中铁的质量分数为70%;C是有刺激性气味的无色气体,它是形成酸雨的物质之一;F可溶于G的稀溶液并产生气体,该气体是有利于环境保护的理想燃料。请回答下列问题:
①A的化学式为____ _____,已知A转化为B时金属元素的化合价升高,则A中非金属元素的化合价是___________。
②B与CO反应的化学方程式是。
③C→D反应的化学方程式是____ _________________。
④B与G的稀溶液反应的化学方程式是___ _______。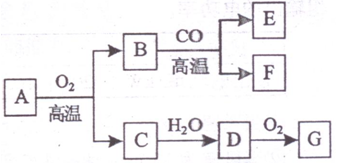
有A、B、C三种物质,已知A为一种氯化物,B为一种钠盐,C为一种可溶性碱。下图表示的是A、B、C的溶液两两反应的实验现象。请根据有关实验现象回答:
(1)A的化学式___________;D的化学式________;蓝色沉淀的化学式是________;
(2)B与C反应的化学方程式:___________________;
(3)A溶液与洁净的铁钉反应的化学方程式:_________________。
(10湛江22).(8分)某学校化学兴趣小组用NaCl固体(含有的杂质CaO)来配制一定质量分数的NaCl溶液,实验的流程图如下: 
请回答:
(1)写出适量HCl加入到溶液B中所发生反应的化学方程式为__________________________。
(2)操作2的名称是__________,在溶液A中加入过量碳酸钠的目的是________________。
(3)若要配制100g质量分数为10%的氯化钠溶液,除了用到天平、烧杯、量筒外,还需用到的玻璃仪器是__________,其作用是______________________________。
阅读下列科普材料,回答相关问题。
【材料1】1915年4月22日下午5时,在第一次世界大战两军对峙的比利时伊珀尔战场,趁着顺风,德军一声令下开启了大约6000只压缩氯气(Cl2)钢瓶。霎时间,在长约60公里的战线上,黄绿色的云团飘向法军阵地。所经之地绿色植被枯黄褪色;英法士兵先是咳嗽继而喘息,甚至死亡,部分逃到高高的山上的士兵活了下来;战场上的武器锈迹斑斑。这就是战争史上第一次化学战。
(1)推测氯气可能具有的物理性质是______。
(2)推测氯气可能具有的化学性质是______。
(3)元素周期表中氯元素的信息如图所示,其原子的核外电子数为______。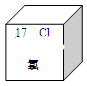
【材料2】氯气可用于制备多种消毒剂。①二氧化氯是一种高效、安全环保型杀菌消毒保鲜剂。②漂白粉是一种广泛普及的杀菌消毒漂白剂,有效成分是次氯酸钙[Ca(ClO)2],其水溶液遇空气中的二氧化碳生成碳酸钙和次氯酸[HClO],HClO起到杀菌、消毒、漂白的作用。
(1)①中二氧化氯的化学式为ClO2,其中氯元素的化合价为______。
(2)②中发生反应的化学方程式为______。
.海水是巨大的资源宝库。下图是综合利用海水制备的一些产品的流程:
(1)操作a 的名称是 ,在实验室中完成此项操作需要的玻璃仪器有烧杯、玻璃棒和 。
(2)步骤①中用蒸发结晶法而不采用降温结晶法的理由是 。
(3)步骤④应加入的物质是 。
(4)请写出步骤②、③发生反应的化学方程式:
② ,③ 。
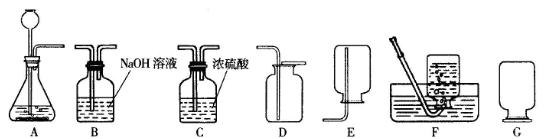
(1)氢气是最轻的气体,难溶于水。氢气作为未来的理想能源,是航天工业的高能燃料,也是化工生产的重要原料。实验室通常采用下面装置制取少量氢气,请根据
要求回答:
要求回答:
①实验室使用稀盐酸和金属锌制取氢气的化学反应方程式为,这种方法制得的氢气往往含有少量(原因是)和水蒸气,可将杂质气体通过装置除去;
②实验中可采用装置收集氢气;集满氢气后的集气瓶按装置G方式放置备用,原因是。
(2)某校课题研究小组到电镀厂考察,了解到铁件镀铜的主要工艺流程如下:

(2)某校课题研究小组到电镀厂考察,了解到铁件镀铜的主要工艺流程如下:
结合流程中提供的信息回答:
①流程Ⅱ废水中含有的物质有;
②经测定:流程Ⅳ中废水的pH为4,废水中一定没有;
③流程Ⅳ废水中除流程Ⅰ、Ⅱ引入的物质外,还含有;
请设计简单方案来证明你的推断:
。
我们学习化学的目的之一就是学会从化学的视角认识和分析生活生产中的一些问题。
(1)2013 年济南市整合趵突泉、大明湖、五龙潭、护城河等旅游资源,组建天下第一泉风景区,它集独特的自然山水景观和深厚的历史文化底蕴于一体,为 5A 级景区。
①对泉水的下列说法中明显错误的是 (填序号)
A.清澈的泉水是溶液 B.蒸馏是净化程度很高的净水方法
C.可用煮沸的方法降低泉水的硬度 D.过滤可以除去泉水中的可溶性杂质
②某化学小组的小泉同学取2滴非常清澈的趵突泉水滴在洁净的玻璃片上,置于酒精灯上小心加热,水分消失后,观察到玻璃片上有少许固体残留物,产生该现象的原因是
。
③济南市区居民的大部分饮用水来自地表天然水,天然水转化成饮用水需经一系列净化,Cl2是一种廉价的自来水消毒剂,与水反应生成次氯酸(HClO)有较强的杀菌作用。氯气(Cl2)和次氯酸中氯元素的化合价分别是 。
(2)化学与食品安全、环境保护、人体健康等密切相关。下列说法错误的是 (填序号)
A.在食盐中添加适量碘酸钾,补充人体所需的碘元素
B.“低碳生活”倡导大量使用化石燃料,鼓励人们多开汽车出行
C.香烟的烟气中含有许多有毒物质,吸烟有害健康
铜和铁是生产、生活中广泛使用的金属。
(1)工业上用一氧化碳和赤铁矿(主要成分是氧化铁)冶炼铁,反应的化学方程式为____。
(2)铁生锈的条件是____;铜表面也容易生成绿色铜锈,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3,其组成元素有_____种。
(3)老师用生锈的铜片、铁粉和稀硫酸进行实验,实验过程如下图所示(部分生成物已略去)。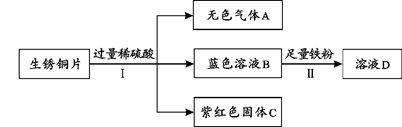
①紫红色固体C的化学式为 ;
②写出II中反应的化学方程式 。
(10芜湖12).某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。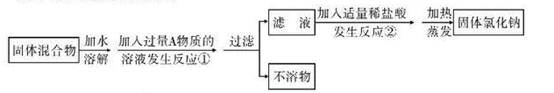
(1)写出A物质的化学式: ,写出A物质的俗称: 。
(2)写出反应②的化学方程式: 。
(3)反应①中加入过量A物质的目的是 。
反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度 (填“有”或“没有”)影响。
(4)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果 (填“增大”、“不变”或“减小”)。
【10桂林30】 (6分) A、B、C、D、E是初中化学中的五种常见物质。C、D是单质,C为紫红色固体,D被认为是最清洁的能源。B的浓溶液常用做干燥剂。已知Fe和A、B的水溶液分别能发生反应:
①Fe + A → C + E; ②Fe + B → D + E 。
(1)写出A、B、C的化学式: A , B ,C 。
(2)现有Fe和A、C三种固体组成的混合物,小刚想测定该混合物中C物质的质量分数,他设计并完成了以下实验:
你认为,小刚的实验数据处理是否正确(填“正确”或“ 不正确”) ,理由是 。
水是生命之源、万物之基,与人类的生活和生产密切相关。小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如图所示。请回答以下问题。
(1)A物质的名称是 ,操作①的名称是 ,若经过操作①后,所得液体C中仍有浑浊,其原因可能是 (填写序号);
a.漏斗内的滤纸有破损
b.漏斗下端未靠在烧杯内壁
c.漏斗内液面高于滤纸的边缘
(2)操作②应选用的装置是下图中的 (填序号),该过程主要是 变化(填“物理”或“化学”)。
(3)小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是 水。操作③应选用的装置是 (填序号),经过操作③以后,小刚重复上述实验,他观察到的实验现象是 。
比较、分析、归纳是学习化学的重要方法。通过比较可以发现相同的反应物在不同外界条件下,会发生不同的反应。请参照示例归纳反应规律:
| 组别 |
化学方程式 |
规律 |
| 示例 |
 |
反应物相同时,反应物的量不同,生成物不同 |
| (1) |
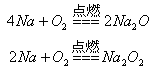 |
|
| (2) |
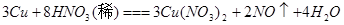 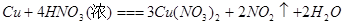 |
|
以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制。以粗盐为原料的“氯碱工业”流程如下: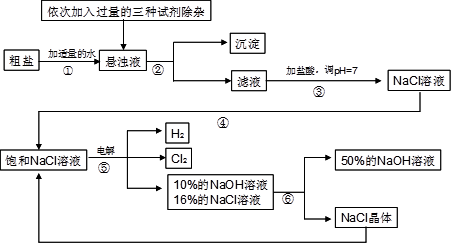
(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,不正确的是 。
| A.能去除油污,可做厨房清洁剂 | B.易溶于水,溶解时放出大量的热 |
| C.水溶液能使石蕊溶液变红 | D.可用作某些气体的干燥剂 |
(2)操作②的名称是 ,该操作所需的玻璃仪器是 ;操作④的名称是 ,该操作需玻棒不断搅拌,这是为了防止 。
(3)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),其顺序要求是:Na2CO3溶液必须在BaCl2溶液之 (填“前”或“后”)加入。有同学提出用 溶液代替BaCl2溶液可达到同样的目的。
(4)电解饱和NaCl溶液的化学方程式是 。
(5)该流程中可以循环利用的物质是 。
有下图装置,请回答有关问题: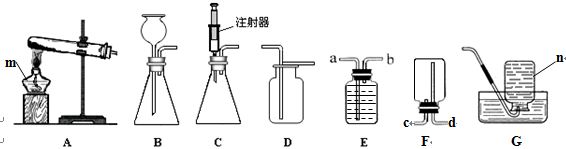
(1)图中标有字母的仪器的名称:m ,n 。
(2)实验室用氯酸钾和二氧化锰共热制取氧气,应选用的发生装置是 (填字母序号),反应的文字表达式为 。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,与B相比优点是 。
(4)若用装置E收集氧气,则气体从 (填“a”或“b”)端通入;若使用装置F收集氧气,则气体应
从 (填“c”或“d”)端通入。
(5)小明对妈妈杀鱼时从鱼肚内取出的鱼鳔(如图所示)产生了兴趣,他以“探究鱼鳔内气体体积和成分”作为研究性学习的课题进行探究实验,通过查阅资料获知:这种鱼鳔内氧气约占1/4,其余主要为二氧化碳和氮气,且二氧化碳能溶于水。以下是小明分两步进行的探究实验: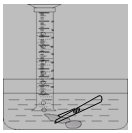
①用两种方法测量鱼鳔内气体体积:A、用医用注射器抽取鱼鳔内气体,测量其体积;B、在水下刺破鱼鳔,用排水集气法收集鱼鳔内气体并测量其体积(如图所示)。你认为测量结果最不准确的一种方法是 (填“A”或“B”),理由是 。
②探究鱼鳔内气体的成分:用两瓶鱼鳔内的气体进行实验,帮助他完成下表中的实验记录:
| 实验目的 |
实验方法 |
实验现象 |
| 验证鱼鳔内含O2 |
|
|
| 验证鱼鳔内含CO2 |
|
|
某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2,小青同学设计了以下实验方案来除去可溶性杂质。 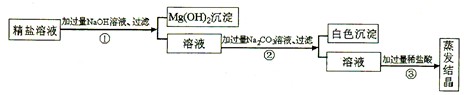
步骤①的化学方程式为_______________________________________。
步骤②中得到的白色沉淀是_________________________ (填化学式)
步骤③中加稀盐酸是为了除去溶液中的___________________。
| A.CaCl2 | B.MgCl2 | C.NaOH | D.Na2CO3 |