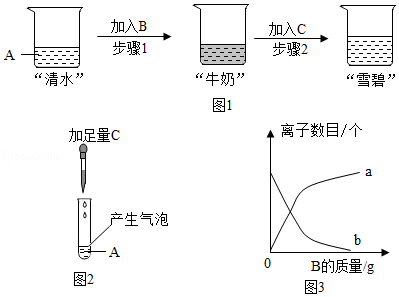
在化学兴趣小组的活动中,老师让甲同学给大家表演了一个小魔术:"清水变牛奶,牛奶变雪碧"。A、B、C三种溶液分别是稀盐酸、氢氧化钙溶液、碳酸钠溶液中的某一种。
【实验活动】
[交流讨论]同学们根据新奇的现象展开了热烈的讨论。
乙同学:"清水变牛奶"就是无色溶液中产生白色浑浊。
丙同学:"牛奶变雪碧"就是白色浑浊消失,溶液中产生大量的气泡。
大家都点头认同。
[提出问题]甲同学:A、B、C分别是什么?为什么能出现上述现象呢?
[解释结论]丁同学:根据步骤2的现象可确定C为 (填名称)。
戊同学:产生步骤1现象的原因是 (用化学方程式表示),但还无法确定A、B各是什么。
[实验证明]己同学:另取A于试管中,把C滴加到A中观察到的现象如图2所示,因此他断定A是 (填化学式)溶液、同时也确定了B。
[深入交流]甲同学:步骤1加入B时,溶液中CO 3 2 ﹣的数目变化趋势曲线应该是 (如图3,填a或b)。
[总结归纳]上述实验活动涉及的这类化学反应,只有当两种化合物互相交换成分, 时,复分解反应才可以发生,除此之外还可能生成 ,且反应前后没有 (答一点)。
小组活动结束,老师为同学们的探究意识和探究能力点赞。
化学兴趣小组对“可乐除铁锈”实验展开探究。同学们将几枚生锈的铁钉放入某品牌的可乐中,观察到铁钉表面有气泡产生,容器底部沉有固体物质。取出铁钉后用水清洗,铁钉恢复光亮。
Ⅰ.容器底部固体成分探究。
【实验探究1】取出容器底部剩余的固体物质,用水清洗后干燥,分成甲、乙两份备用。
实验操作 |
实验现象 |
解释与结论 |
①用磁铁靠近固体物质甲 |
固体物质 (填“能”或“不能”)被吸引 |
固体物质中不含铁单质 |
②将固体物质甲放入20%的盐酸中 |
固体逐渐消失,溶液变成黄色 |
固体物质主要是氧化铁,化学反应方程式为 。 |
Ⅱ.溶液中逸出气体成分探究。
【猜想假设】气体中除了可乐本身含有的CO2外,可能还有H2。
【查阅资料】①H2可以还原CuO,生成Cu和H2O。
②无水硫酸铜为白色固体,遇水变蓝。
【实验探究2】将逸出气体依次通过如图的组合装置。

(1)NaOH溶液的作用是 。
(2)实验过程中观察到 现象,证明逸出气体中含有氢气。
Ⅲ.深入探究
【提出问题】铁钉表面已变光亮,而容器底部有大量铁锈剩余的原因是什么?
【猜想假设】①可乐太少,酸性物质量不足。②可乐酸性弱,与铁锈反应太慢。
【实验探究3】取可乐与锈铁钉反应后的剩余液,测得溶液仍然呈酸性,猜想①不成立。
【查阅资料】3%的稀盐酸pH约为1,某品牌可乐的pH值为3.39.质量分数为3%的稀盐酸比该品牌可乐的酸性 (选填“弱”或“强”)。
【实验探究4】取另一份固体物质乙放入3%的稀盐酸中,振荡,观察无明显现象。
【实验结论】对比【实验探究1】和【实验探究4】的不同反应现象可得出:化学反应速率与反应物的 有关。猜想②成立。
【合理推测】可乐能快速去除铁钉表面铁锈的真正原因是:铁锈结构疏松多孔, 。
Ⅳ.废液处理
将【实验探究1】和【实验探究4】中废液混合,得到澄清溶液100.0g,通过氯离子检测仪测得氯离子质量分数为7.1%.从环保角度考虑,最好在废液中加入 g氢氧化钠固体,充分反应,过滤后再将废液排放。
北宋沈括编撰的《梦溪笔谈》中,记录了用CuSO4溶液熬制胆矾的铁釜,使用时间久了也可以化作铜。
(1)由上述材料分析,Fe比Cu的金属活动性 (填“强”或“弱”)。
(2)如果向足量的CuSO4溶液中加入5.6g Fe粉,充分反应后,理论上可以得到Cu的质量是多少?
市售的某些银首饰是银、锌合金。小庆同学取该合金样品20g,加入100g稀硫酸恰好完全反应,产生气体质量与反应时间的关系如图所示,计算:
(1)该合金中锌的质量(精确到0.1g)。
(2)该稀硫酸中溶质的质量分数(精确到0.1%)。

某NaCl样品中只含有杂质CaCl2,为测定样品中CaCl2质量分数,取样品20g完全溶解于水中,并向其中加入过量的Na2CO3溶液,生成沉淀的质量是2g。计算样品中CaCl2的质量分数。
阅读下列材料,回答问题:
材料一:研究人员发现大气层中特别是南极上空的臭氧层日益变薄。进入大气平流层的氯氟烃(一类合成有机化合物,应用于冰箱和空调的制冷剂、灭火器等)是造成臭氧层变薄的主要原因。因为在紫外线的照射下,平流层中的臭氧存在如下平衡:O 3 O 2+O;而氯氟烃进入平流层后会分解产生氯原子(Cl),进而发生下列反应:Cl+O 3→ClO+O 2;ClO+O→Cl+O 2
研究表明:平流层中1个氯原子大约可以破坏1×10 5个臭氧分子。氯氟烃分解产生的氯原子在上述反应中起着 作用。
二氧化硫属于空气污染物,应处理后排放。32g硫与足量的氧气完全反应,生成二氧化硫的质量是多少?
往100g硫酸和硫酸铜的混合液中,逐滴加入8%的氢氧化钠溶液直至过量,根据实验事实绘制了如图所示曲线,分析并计算:
(1)a→b段表示氢氧化钠与混合物中的 发生反应。
(2)求反应前混合液中硫酸铜的质量分数。(写出计算过程)

小苏打的主要成分是碳酸氢钠,其中往往含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌小苏打样品中碳酸氢钠的质量分数。
(1)准确称取9.0g小苏打样品放入烧杯中,逐滴加入质量分数为5%的稀盐酸至恰好不再产生气泡为止,共消耗稀盐酸73.0g,烧杯中没有残留不溶物。计算样品中碳酸氢钠的质量分数。(写出计算过程)
(2)请你设计一个与上述实验原理和操作方法均不相同的实验,测定小苏打样品中碳酸氢钠的质量分数 。
将9g含少量杂质(杂质既不溶于水也不参加化学反应)的碳酸氢钠样品放入烧杯中,加入稀盐酸至恰好完全反应,共用去稀盐酸54.5g。烧杯内剩余物质的总质量为59.1g。请计算:
(1)产生二氧化碳气体的质量。
(2)反应后所得溶液中溶质的质量分数。
我市覃塘区石灰石资源丰富,某石灰厂为了测定某石灰石样品中CaCO3的质量分数,往盛有300g稀盐酸的烧杯中依次加入粉碎后的石灰石样品(杂质不与盐酸反应),充分反应后,实验数据记录如表:
实验次数 |
第一次 |
第二次 |
第三次 |
石灰石样品/g |
25 |
15 |
10 |
烧杯中物质总质量/g |
316.2 |
326.8 |
m |
请回答:
(1)CaCO3中钙、碳、氧三种元素的质量比为 ;(写最简比)
(2)表中m= ;
(3)所用稀盐酸的溶质质量分数为 ;
(4)求该石灰石样品中CaCO3的质量分数。(写出计算过程)
向一定量的澄清石灰水中通入适量的二氧化碳,使氢氧化钙全部转化为碳酸钙沉淀,得到的沉淀质量为1.00g。计算澄清石灰水中氢氧化钙的质量(计算结果精确至0.01g)。
小华同学发现自家的水壶用久以后底部会附着一层白色固体,查阅资料后得知,水在加热或长久放置时,溶于水中的可溶性钙和镁的化合物会生成沉淀(水垢),于是他邀请同学小雪进行了以下实验探究。
探究一:自家的井水是软水还是硬水?
取少量井水样品于试管中,加入 ,振荡,出现大量浮渣,由此得出结论:自家的井水属于 。
探究二:白色固体的主要成分是什么?
[假设与猜想]猜想Ⅰ:CaCO3。
猜想Ⅱ: (填化学式)。
猜想Ⅲ:CaCO3和Mg(OH)2。
[实验与探究]取少量白色固体样品(不考虑杂质和微溶物对实验的影响)于试管中,向其中加入足量稀盐酸,白色固体溶解,有 产生,根据以上现象,小华认为:猜想Ⅰ正确。小雪认为小华的结论不严谨,理由是 。经过两人反复讨论,进一步设计了如下实验。
实验步骤 |
实验现象 |
实验结论 |
取上述实验中的上层清液于试管中,滴加足量NaOH溶液 |
无明显现象 |
猜想Ⅰ成立 |
|
猜想Ⅲ成立 |
[拓展与迁移]取含有MgCl2和HCl的混合溶液165.8g于烧杯中,向其中缓慢加入200g溶质质量分数为8%的NaOH溶液,恰好完全反应后过滤得到沉淀和滤液,其中滤液的质量为360g。请计算:
(1)生成沉淀的质量是 克。
(2)原混合溶液中,MgCl2的质量是多少?(请写出具体的计算过程,下同)
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?(结果保留至0.1%)
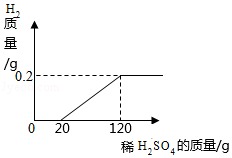
向表面生锈的铁片中滴加稀硫酸,产生氢气的质量与所加稀硫酸的质量关系如图所示,请回答:
(1)从图中可以看出完全反应后产生氢气的质量为 g。
(2)求所加稀硫酸中溶质的质量分数。(写出计算过程,计算结果精确到0.1%)