某化学小组的同学对金属元素及金属材料进行系列研究.
(1)人类文明与金属材料的发展应用关系十分密切.下列三种金属合金中,直到近代才得以应用的是 (填写序号之一).
①铜合金 ②铝合金 ③铁合金
(2)孔雀石的主要成分是碱式碳酸铜[Cu 2(OH) 2CO 3],以其为原料的炼铜方式有以下两种:①Cu 2(OH) 2CO 3═(加热)2CuO+CO 2↑+H 2O
②Cu 2(OH) 2CO 3+2H 2SO 4═2CuSO 4+CO 2↑+3H 2O
以上 ① ② 两种方式,再通过一步反应都可得到单质铜,其中不属于湿法冶铜的是 (填写序号 ①、②之一).
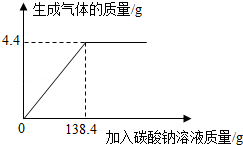
(3)已知碱式碳酸铜[Cu 2(OH) 2CO 3]难溶于水,现取33.3g的碱式碳酸铜固体,放入干净的烧杯中,逐渐滴入溶质质量分数为10%的H 2SO 4溶液,滴入该H 2SO 4溶液的质量和反应产生气体的质量关系曲线如图所示.请回答下列问题:
①当滴入上述H 2SO 4溶液196g(即图中A点)时,烧杯内溶液中的溶质质量为 g.
②当滴入上述H 2SO 4溶液294g(即图中B点)时,试通过计算,求此时所得不饱和溶液的质量.(计算结果精确至0.1g)

黑豆是传统的养生食材,食用9°米醋泡制得到黑豆是一种很好的食疗方法。小明为判断家中的9°米醋含酸量是否合格,拟配制一定质量分数的氢氧化钠溶液进行测定。产品部分信息如图所示。请回答相关问题。
(1)配制100g质量分数为4%的氢氧化钠溶液需要水 mL(水的密度为1g/cm 3)。
(2)若9°米醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的方程式为:
CH 3COOH+NaOH═CH 3COONa+H 2O,小明取出10mL9°米醋,加入4%的氢氧化钠溶液12g,恰好完全反应。请通过计算判断该产品含酸量是否合格?(写出计算过程)

铁的锈浊对社会生产造成较大损害,但也有有利的一面,如某些食品包装袋内常放入还原性铁粉作"双吸剂"以防止食品腐败。某课外兴趣小组在实验室发现了一包破损的还原性铁粉(含少量杂质,杂质既不溶于水也不溶于酸),他们取六份样品,分别加稀硫酸反应。测得部分数据加下,请根据有关信息回答问题。
| 实验次数 |
1 |
3 |
4 |
5 |
6 |
| 取样品质量(g) |
31.0 |
31.0 |
31.0 |
31.0 |
31.0 |
| 取稀硫酸质量(g) |
30.0 |
90.0 |
120.0 |
150.0 |
180.0 |
| 产生气体质量(g) |
0 |
a |
0.3 |
0.5 |
0.6 |
(1)食品袋内放入"双吸剂"是为了吸收 ,用铁粉而不用铁块作"双吸剂"的理由是 。
(2)a的数值为 。
(3)第4次实验,所得到溶液中溶质的化学式为 。
(4)列式计算该样品中单质铁的质量分数(保留至0.1%)。
胃酸过多的病人,通常需每天服用含碳酸氢钠的药物9片,能消耗胃酸中的氯化氢2.19g.某病人有胃溃疡症状,这种药物会加剧胃部疼痛.医生建议改用含氢氧化铝(其他成分不与胃酸反应)的胃舒平,药物标签如图.请计算中和相同质量的胃酸,每天需要服用胃舒平多少片?

为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图。
(1)上述反应产生二氧化碳的质量为 g;
(2)计算该赤铁矿石中氧化铁的质量分数。

2017年5月5日我国自主研发的首架大型客机c919试飞成功,镁铜合金常用作飞机天线等导电材料。现取一定质量的该合金样品,加入足量的稀硫酸,充分反应后,放出0.3g氢气,剩余固体质量为6.4g。
(1)求合金样品中镁的质量。
(2)求合金样品中铜的质量分数。
现有含杂质的氢氧化钙样品10g向其中加入10%的稀盐酸溶液73g恰好完全反应(杂质不参与反应),求样品中氢氧化钙的质量分数。
某同学在实验室作酸碱中和反应实验.将稀硫酸滴入到8克10%的氢氧化钠溶液中至恰好完全反应,共消耗稀硫酸10克,请计算该硫酸中溶质的质量分数.
草酸(H2C2O4)又名乙二酸,是一种有机酸,易溶于水,广泛存在于植物源食品中。草酸不稳定,在浓硫酸的催化作用下,草酸固体受热分解生成碳的氧化物和水。某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究:
[提出问题]生成物中有哪几种碳的氧化物?
[实验猜想]猜想1:只有CO;
猜想2:只有 (填化学式);
猜想3:含有CO和CO2。
[设计实验]基于猜想3,根据CO和CO2的性质,兴趣小组同学设计了如下实验:

[实验探究]
(1)观察到A装置中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成,请写出A装置中的化学反应方程式: ;
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置澄清石灰水不变浑浊,F装置中出现 的现象;
②E装置中出现 的现象。
[实验结论]通过实验探究证明:猜想3成立。
草酸分解的化学方程式是 。
[问题讨论]
(1)B装置的作用是 ;
(2)C装置的作用是 ;
(3)该试验装置的设计还有一处明显不足(实验前已排尽装置内的空气),请提出改进措施 (任写一条)。
向一定质量、一定溶质质量分数的稀盐酸中逐滴加入某碳酸钠溶液.实验过程中,产生气体质量与加入碳酸钠溶液的质量关系如图所示,试计算:
(1)恰好完全反应时,生成气体的质量为 g;
(2)恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量是多少?
(3)若恰好完全反应时所得溶液的溶质质量分数为5%,则稀盐酸的溶质质量分数是多少?
铜是一种常见的金属,在生活、生产中有广泛的应用.
(1)电气工业上常用铜作电缆的内芯,是利用铜具有良好的 性;
(2)铜是一种不活泼的金属,但铜制品长期露置在潮湿空气中,表面变绿色,即生成了"铜绿"[化学式:Cu x(OH) yCO 3].
小明和小丽为了探究"铜绿"的组成,查阅资料:"铜绿"受热易分解生成CuO、CO 2和H 2O.他们进行如下实验:称取22.2克"铜绿",充分加热至固体质量不再改变,把产生的气体全部依次通过足量浓硫酸和足量氢氧化钠的溶液,发现浓硫酸增重1.8克,氢氧化钠溶液增重4.4克.
根据以上实验.他们推断出:x= ,y= ;铜与潮湿空气中变成"铜绿"的化学方程式是 ;
(3)小明和小丽分别取24.0克氧化铜,用CO还原制铜,小明得到19.2克红色固体,小丽得到20.8克红色固体.他们质疑:为什么两人得到的红色固体质量不相等?
查阅资料:
Ⅰ.CO还原CuO时也可产生红色的氧化亚铜(Cu 2O)
Ⅱ.Cu 2O+H 2SO 4(稀)═Cu+CuSO 4+H 2O
他们分析推断:
①一致认为 (填"小明"或"小丽")的产物中没有Cu 2O;
②用CO还原a克Cuo得到红色固体b克,若红色固体为Cu和Cu 2O的混合物,则a与b的数量关系是 ;
③还可以简单的实验验证红色固体是否有Cu 2O,请简述操作、现象及结论: .
通过化学变化可以制备物质。
(1)某兴趣小组欲用200g 4%的氢氧化钠溶液吸收二氧化碳制备碳酸钠,反应的化学方程式是 ;若要将提供的氢氧化钠全部转化为碳酸钠,请列出计算需二氧化碳质量(x)的比例式 ;
(2)在实验中,该小组同学发现,要定量控制通入氢氧化钠溶液中二氧化碳气体的质量,难以操作。请分析若通入二氧化碳气体的量不足时会导致产物中混有的杂质是 ;
(3)查阅资料:
Na2CO3+CO2+H2O=2NaHCO3;
NaHCO3+NaOH=Na2CO3+H2O;
该小组同学将制备方案改进如下:
步骤 |
实验操作 |
实验目的 |
一 |
将200g 4%的NaOH溶液分为两等份 |
/ |
二 |
① |
将其中一份溶液中的NaOH全部转化为NaHCO3 |
三 |
将步骤二所得溶液小心煮沸1﹣2分钟 |
② |
四 |
③ |
将NaHCO3全部转化为Na2CO3 |
(4)假设每步转化都完全,该小组同学利用改进后的方案制取的碳酸钠质量m1= g;经老师指导,该小组同学将步骤四反应后的溶液蒸干并充分灼烧得到碳酸钠粉末的质量为m2g,发现m1=m2,由此证明他们的方案改进成功。
FeCl2溶液中混有 少量的CuCl2,为了除去CuCl2,某课外小组同学取该溶液50g于烧杯中,然后等量分5次加入某物质M充分反应,所得数据如下表,请根据相关知识和数据回答下列问题:
次数 |
1 |
2 |
3 |
4 |
5 |
加入M的质量(g) |
0.28g |
0.28g |
0.28g |
0.28g |
0.28g |
溶液的总质量(g) |
49.96g |
49.92g |
49.88 g |
49.84 g |
49.84 g |
(1)写出物质M的化学式 。
(2)参加反应M的总质量是多少?
(3)FeCl2溶液中CuC12的质量分数是多少?