已知:Na2O为白色,Na2O2为淡黄色;Na2O+H2O=2NaOH.某兴趣小组对钠和铜的单质及其化合物的性质进行了如下实验探究。
①将铜片置于铁架台的铁圈上,用酒精灯加热,观察到铜片表面变黑;
②趁热将钠置于铜片表面,钠剧烈燃烧,有淡黄色物质生成,将此淡黄色物质转移到试管中待用,再用蒸馏水冲洗铜片,观察到铜片上钠燃烧处出现了光亮的铜斑;
③向盛装淡黄色物质的试管中滴加蒸馏水,观察到冒气泡,将带火星的木条伸入试管,木条复燃。
回答下列问题:
(1)步骤①产生的黑色物质是 ,步骤②淡黄色产物中氧元素的化合价为 价。
(2)步骤②中产生铜斑反应的另一产物,进一步与氧气反应也转化为淡黄色物质,则产生铜斑反应的化学方程式为 。
(3)步骤③产生的气体物质为 。
(4)猜想步骤③还可能有一种常见物质 (填化学式)生成,向反应后的溶液中滴加 溶液(可供选择的试剂:H2SO4、CuSO4、KOH、Na2CO3),观察到 的现象时,即证明了你的猜想。
科学兴趣小组的同学在学了俗称为苏打的碳酸钠后,得知它还有一个俗称为小苏打的"兄弟",这个"兄弟"的性质是否和它相似?它们之间能发生转化吗?
小明查阅了资料,将相关信息整理如表:
| 俗名 |
苏打 纯碱 |
小苏打 |
| 化学式 |
Na 2CO 3 |
NaHCO 3 |
| 构成微粒 |
Na + CO 3 2 ﹣ |
Na + HCO 3 ﹣ |
| 溶解度(常温) |
21.5克 |
9.6克 |
| 两者的转化 |
Na 2CO 3+CO 2+H 2O═2NaHCO 3 |
2NaHCO 3 |
下面是小明同学进行的探究:
(1)用试管取适量NaHCO 3溶液,向试管中滴加酚酞试液,观察试液颜色变化。此实验的目的是 。
(2)在研究Na 2CO 3与NaHCO 3转化时,小明觉得Na 2CO 3转化为NaHCO 3过程中,由于NaHCO 3溶于水,整个过程不会有明显现象。老师笑着对小明说:"做实验吧,实验会告诉你答案。"于是小明在老师的指导下,向饱和的Na 2CO 3溶液中通入CO 2,起初无明显现象,继续不断地通入CO 2,溶液中出现了白色沉淀。这让小明很疑惑:NaHCO 3溶于水,为什么还有白色沉淀呢?小明经过思考,明白了白色沉淀产生的原因是 。
(3)在小明同学的带动下,兴趣小组又对NaHCO 3的其他性质进行了探究,发现两"兄弟"既有相似的性质也有不同的个性。从微观角度分析,造成两"兄弟"不同个性的原因是 不同。
近五年来,我国在科技、文化、环境等方面创新发展。
I.大国重器航天、航空取得重大突破
2018年4月2日,天宫一号目标飞行器圆满完成各项任务返回大气层。这标志着我国航天航空事业进入了新时代。
(1)硅是天宫一号动力源太阳能电池的主要构成材料。单质硅是由石英(SiO 2)固体与碳在高温条件下反应制得的,同时生成一种可燃性气体,该反应的化学方程式为 。
(2)硅还是计算机芯片的基体材料,但其导热性不好,而金刚石在导热性方面远超过硅,于是它成了芯片基体材料的最佳选择。
①从原子结构上分析,金刚石(C)和硅有相似化学性质的原因是 。
②因天然金刚石资源稀少,难以满足要求。人们就根据金刚石的组成和结构设法制造金刚石。现有两种制造金刚石的方法,一是以石墨为原料在高温高压和催化剂的条件下合成;二是在较低温度和压力下用甲烷(CH 4)等为原料制造金刚石薄膜。
下列说法不正确的是 (写字母序号)。
A.一种元素可以组成多种性质不同的单质
B.石墨合成金刚石发生的是物理变化
C.石墨与金刚石物理性质不同是因为结构不同
D.物质的性质在很大程度上决定了物质的用途,但不是唯一的决定因素
③不仅硅与碳具有相似化学性质,其氧化物二氧化硅和二氧化碳也有相似化学性质。试写出二氧化硅与氢氧化钠溶液反应的化学方程式 。
Ⅱ.文化自信一传承中华优秀传统文化
古代我国人民就积累了许多对物质变化的认识。春秋末期齐国的工艺官书《考工记》中载有"涑帛"的方法,即利用"灰"(草木灰)和"蜃"(贝壳灰)混合加水所得溶液来洗涤丝帛。这种溶液能洗涤丝帛主要是因为其中一定含有 (写化学式,水除外)。(注:草木灰的主要成分为碳酸钾,贝壳灰的主要成分为氧化钙)
科学兴趣小组做碳还原金属氧化物实验后,收集到CO和CO 2的混合废气,考虑到废气直接排放会污染环境,想把废气初步分离回收再利用。用如图所示的装置进行分离实验(收集装置略去)。
(1)广口瓶中加入的是 。
A.NaOH溶液 B.NaCl溶液 C.Ca(OH) 2溶液
(2)打开阀门K 2通入混合气体,首先分离得到 气体,接着关闭阀门K 2打开阀门K 1,将分液漏斗中装的 溶液滴入广口瓶中,在广口瓶中看到有气泡产生,从而分离出第二种气体。

化学兴趣小组的同学对“天气瓶”(如图)是否可预测天气很好奇。他们自制了“天气瓶”,并对其晶体析出的影响因素展开了探究。
步骤:(1)称取10.0g樟脑丸溶解于40.0mL无水酒精中得溶液a。
(2)向35.0g水中依次加入2.5gKNO3和2.5gNH4Cl,制得溶液b。
(3)将a、b两种溶液倒入容器中混合,密封即制得“天气瓶”。
(4)模拟不同的天气情况,将制得的“天气瓶”置于不同的温度和大气压的环境中,并记录析出晶体情况如下:
|
0℃ |
20℃ |
40℃ |
101.3kPa |
|
|
|
100.5kPa |
|
|
|
99.7kPa |
|
|
|
根据以上信息回答下列问题:
(1)配制溶液a时,为加快樟脑丸的溶解,可以采用搅拌、微热、 等方法。溶液a中的溶质以分子形式分散,所以该溶液 (选填“能”或“不能”)导电。
(2)溶液b中NH4Cl的质量分数是 。
(3)为进一步探究析出的晶体中是否含有铵盐,需要的实验用品有 (填序号)。
a.稀盐酸
b.氢氧化钠溶液
c.蓝色石蕊试纸
d.红色石蕊试纸
(4)从表格信息中可知, 条件对“天气瓶”晶体析出的影响较大。

开春以来,为提高水稻产量,某农场积极做好科学施肥、精准防治病虫害等工作。
(1)水稻不同生长期需要不同的肥料。如在水稻抽穗、开花时期,为促进穗数增多、籽粒饱满,需要多施磷肥。下列属于磷肥的是 。
| A. |
碳酸钾( ) |
| B. |
尿素[ ] |
| C. |
磷酸二氢钙[ ] |
(2)氮肥能促进水稻幼苗生长。一百亩水稻需要施碳酸氢铵3950千克,用氨气、水和二氧化碳反应来制取,化学方程式为 ,需要氨气多少千克?
(3)井冈霉素是防治水稻纹枯病的常用药。要为一百亩水稻喷洒一次这种农药,需要配制溶质质量分数为0.01%的药液7500千克,应购买5%的井冈霉素药液 千克。
2022年我国将有6名航天员生活在空间站。氧气、水、食物等是维持航天员驻留空间站的必要物质。为提高物质的利用率,目前空间站通过以下途径实现物质循环利用:
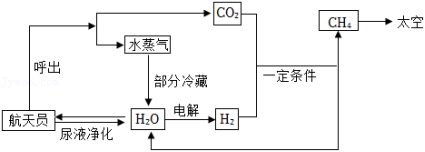
(1)由图可知,目前空间站通过物质循环获得水的途径共有 条,其中尿液净化时必须除去尿液中的 等代谢废物。
(2)为实现氧的循环,目前空间站内利用氢气和航天员呼出的二氧化碳,在一定条件下转化为甲烷和水,化学方程式为 。据测算,正常情况下一位航天员一天呼出的二氧化碳质量约1.1千克,若这些二氧化碳全部与氢气反应,则可生成水多少千克?
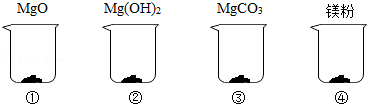
举重前运动员常常会抓一把“镁粉”在手里搓,以起到防滑效果,某种“镁粉”中只含有 、 、 中的一种或几种固体。某兴趣小组对其成分展开了探究:分别取4.2克 、 、 和“镁粉”置于烧杯中,逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失。四种固体消耗稀盐酸的质量如表所示,且烧杯③和烧杯④中产生了大量气泡。请结合实验现象和数据回答问题。
|
物质 |
|
|
|
“镁粉” |
|
消耗稀盐酸的质量/克 |
121.8 |
|
58.0 |
61.9 |
(1)烧杯③中产生的气体是 。
(2)“镁粉”中不只含有 一种物质,理由是 。
(3)表格中 的值为多少?(请写出计算过程)
(4)为确定“镁粉”的具体成分,兴趣小组补充了如下实验:取“镁粉”和 各4.2克,加入足量稀盐酸,生成相同条件下的气体体积分别为952毫升和1120毫升。由此可知该种“镁粉”的成分是 。
化学是一门以实验为基础的自然科学
(一)实验帮助我们研究物质的组成
如图是测定空气中氧气体积分数的实验装置,请回答下列问题:

(1)红磷在空气中燃烧的现象是 ,发生反应的化学方程式为: 。
(2)实验结论:氧气约占空气总体积的 。
(二)实验帮助我们研究物质的性质
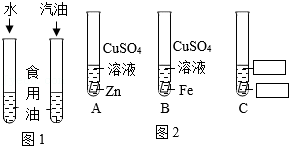
(3)图1实验中,食用油溶解于 中,该实验表明影响物质溶解性的因素是 。
(4)图2试管B中发生反应的化学方程式为: 。
(5)为了探究 、 、 的金属活动性顺序,图2试管C中需要补全的一组试剂是 。
(三)实验帮助我们研究物质的制法
实验室模拟炼铁原理的装置如图所示,请回答下列问题:
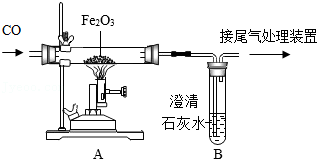
(6)写出A装置玻璃管中发生反应的化学方程式: ,该反应前后碳元素化合价发生的变化是 。
(7)B装置中的现象是 。
(8)实验中需要进行尾气处理的原因是 。
如图为高炉冶铁、炼钢并用生产的钢来探究白铜成分的流程图。(已知硫酸镍的化学式为NiSO 4)
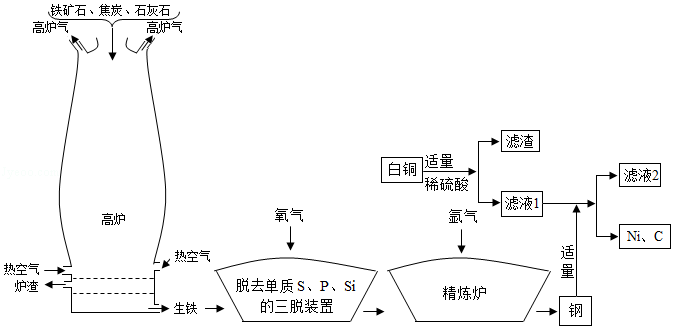
(1)用高炉冶铁的主要反应原理是 (用化学方程式表示)。
(2)分析流程图,三脱装置中发生反应的基本反应类型是 。
(3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中 (填一种仪器的名称)的作用。
(4)铁与镍相比,铁的金属活动性 镍(选填">"、"="或"<"),判断依据是 (用化学方程式表示)。
(5)通过以上信息,得出白铜的成分是 ,其硬度比纯铜 (填"大"或"小")。
某化学兴趣小组同学为探究硫酸的化学性质,做了如下实验:

(1)能产生气泡的是 (填序号)。
(2)溶液变为蓝色的是 (填序号),写出其中发生的化学方程式 。
(3)能证明C中发生了反应的现象是 。
(4)实验过程中,发现只有A中无明显现象,说明铜与稀硫酸不发生反应。
【提出问题】铜与硫酸真的不能反应吗?
【查阅资料】
①铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O
②SO2能使品红溶液褪色;
③SO2能与碱溶液反应;
④SO2能溶于水,但不溶于饱和NaHSO3溶液
【进行实验】
同学们在老师的帮助下用如图所示装置进行实验:

请回答下列问题:
(1)实验开始时,打开开关K,发现D中品红溶液褪色,装置D中试管口放置的棉花上浸有浓氢氧化钠溶液,其作用是 。
(2)装置B的作用是收集贮存多余的气体,当D中有明显现象后,关闭K,移去酒精灯,但由于余热的作用,A有仍有气体产生,此时B中现象是:长颈漏斗内液面 (填“上升”或“下降”),则B中盛放的液体为 (填序号)。
A.水
B.氢氧化钠溶液
C.饱和石灰水
D.饱和NaHSO3溶液
【知识拓展】化学反应的进行与物质的溶质质量分数,反应条件都有一定的关系。
掌握化学知识有利于我们更好地生活。
(1)在炎热的夏天,应该把自行车停放在阴凉处,防止因暴晒而爆胎。请用微观粒子观点解释爆胎的原因: 。
(2)家庭使用燃气时要特别注意安全,当发现燃气泄漏时,一定要防止电火花的产生,否则可能发生 现象。
(3)沙漠地区的铁制品锈蚀较慢的原因是 。
(4)主要成分为氧化钙的食品干燥剂与水接触时会对人体造成伤害,因为氧化钙与水反应生成具有腐蚀性的碱溶液,同时还能 。
某化学小组选用如图部分装置制取纯净、干燥的CO2。

(1)写出A中所发生反应的化学方程式 。
(2)若将a、b连接,B中溶液不变浑浊,这是因为CO2中混有哪种杂质? 。
(3)为达到实验目的,所选用装置的导管接口从左到右的正确连接顺序为: a接 、 接 、 接j。
(4)用F收集CO2,j为进气口。请将F中的玻璃导管补画完整。
甜叶菊苷具有高甜度低热能的特点,是一种新型甜味剂,我国是全国最主要的生产国,实验小组欲探究甜叶菊苷的元素组成,进行如下实验:
[提出猜想]甜叶菊苷由什么元素组成?
[进行实验]小晴取适量的甜叶菊苷按如图1进行操作,并分别将干冷的烧杯和蘸有澄清石灰水的烧杯倒置与火焰上方。
[讨论交流]其他同学认为小晴的实验设计不严谨,原因是 。经改进试验后,检验到甜叶菊苷在氧气中充分燃烧的产物只有二氧化碳和水,由此确定甜叶菊苷中一定含有碳,氢元素。
[继续探究]为了进步确定其元素组成。利用如图2进行实验。(已知:装置中C中的氧化铜能确保甜叶菊苷中的碳元素完全转化为二氧化碳)
(1)实验前要通一会儿氮气,目的是 。
(2)A装置中发生反应的化学方程式为 。
[数据记录]4.02g甜叶菊苷在C装置中充分燃烧后,D装置增重2.7g,E装置增重8.36g。(产物被完全吸收)
[分析与讨论]数据分析:4.02g 甜叶菊苷中氧元素的质量为 g,由此可以确定甜叶菊苷是由碳,氢,氧元素组成。
[反思评价]若没有F装置,对氧元素质量测定结果的影响是 。 (填“偏大”、“偏小”或“无影响”)。