在探究金属活动性顺序时,华雪同学把两根绕成螺旋状的洁净铜丝分别浸入硫酸铝溶液、硝酸银溶液中,过一会儿取出:
(1)铜丝浸入硫酸铝溶液中,可观察到的现象是: 。
(2)铜丝浸入硝酸银溶液中,可观察到铜丝上有 色物质生成,溶液逐渐变成蓝色。
(3)铜丝浸入硝酸银溶液中,离子数目减少的是 ,离子数目增加的是 。
(4)根据上述实验所观察到的现象,华雪同学 (填“能”或者“不能”)证明铝、铜、银的金属活动性顺序Al>Cu>Ag
纯净的二氧化硅是现代光学及光纤制品的基本原料。请回答下列问题:
(1)二氧化硅的化学性质很不活泼,氢氟酸(HF)是唯一可以与之发生反应的酸(生成物为水和四氟化硅气体),该反应的化学方程式为 。
(2)二氧化硅与碳酸钙在高温下反应生成硅酸钙( CaSiO3)和二氧化碳:在物质的分类①单质②化合物③氧化物④酸⑤碱⑥盐中,硅酸钙属于 (填序号)。
铁是一种常见的金属,也是目前世界上年产量最高的金属。下面归纳了初中化学有关铁的知识。
(1)比较生铁和纯铁,其中硬度较大的是 。
(2)焦炭的主要成分是碳,在生铁冶炼过程中,焦炭参与了下列反应:
①C+O2 CO2 ②C+CO2
CO2 ②C+CO2 2CO
2CO
其中为冶炼生铁提供热量的反应是 (填序号)。
(3)物质甲的阳离子符号是 。
(4)若铁与物质乙反应时,火星四射,则生成物中固体的化学式是 。
(5)若固体为红色单质,则铁与物质乙反应的化学方程式是 (任写一个)。
2017年5月,我国南海海域首次实现“可燃冰”试采成功。“可燃冰”为甲烷的水合物,其化学式为CH4•8H2O,主要是由甲烷与水在高压低温条件下形成的类冰状物质,可燃烧。
(1)目前使用的主要化石燃料有 、石油和天然气等。
(2)甲烷属于 (填“有机物”或“无机物”)
(3)可燃冰中元素质量比C:H:O为 。
(4)可燃冰在空气中燃烧的化学方程式为 。
(5)与化石燃料相比较,开采可燃冰的积极意义有 (写一条)。
NSR技术通过BaO和Ba(NO3)2的相互转化实现NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如图所示。
(1)还原时还原尾气可以是CO、H2等,存在如下反应:5CO+Ba(NO3)2═N2+X+5CO2
①反应中,碳元素的化合价 (填“升高”或“降低”)。
②X的化学式是 。
(2)储存时,部分NO发生反应的化学方程式为 ;吸收NOx(如NO、NO2)的物质是 。
(3)NO气体通过NSR技术转化为N2的总反应方程式是 。

某同学发现家里的铜质水龙头表面出现了一层绿色的锈渍,经查阅资料,了解到这层锈渍的化学成分是碱式碳酸铜[Cu 2(OH) 2CO 3],并对Cu 2(OH) 2CO 3受热完全分解后的产物进行探究。
【查阅资料】(1)碱式碳酸铜受热分解生成水蒸气、二氧化碳和一种黑色固体。
(2)白色无水硫酸铜遇水变成蓝色。
【提出猜想】该同学根据碱式碳酸铜的化学式对黑色固体产物作出以下猜想:
①可能是碳 ②可能是氧化铜 ③可能是碳和氧化铜的混合物。
他猜想的依据是 ,且碳和氧化铜都是黑色的。
【实验探究】实验Ⅰ:按如图进行实验,证明分解产物中有H 2O和CO 2(图中夹持装置省略)
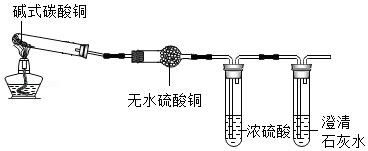
实验Ⅱ:为验证猜想,他做了如下实验:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置,观察现象。
【实验分析及结论】
实验Ⅰ中:证明产物中有水生成的依据是 ;澄清石灰水变浑浊,产物中有 生成。
实验Ⅱ中:因为 且溶液变成蓝色,所以猜想②正确,故碱式碳酸铜受热分解的化学方程式为 。
通过上述实验及结论分析可知,铜质水龙头生锈过程中与水、二氧化碳、 有关。
【实验反思】为了防止铜质水龙头生锈,通常可采取的有效措施是 。
【拓展应用】依据碱式碳酸铜受热分解的产物及所学酸碱盐的知识,该同学认为可以用稀盐酸除去铜质水龙头表面的锈渍,反应的化学方程式为 。
高纯氧化铁[Fe 2O 3]又称"引火铁",可作催化剂,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量不溶于水的SiO 2等)为原料,制备高纯氧化铁的生产流程示意图。

已知:氨水呈碱性(主要成分NH 3•H 2O是一种碱);(NH 4) 2CO 3溶液呈碱性,40℃以上易分解。
(1)写出高温时赤铁矿中的Fe 2O 3与CO发生反应的化学方程式 。
(2)①处发生反应的化学方程式为 。
(3)加入(NH 4) 2CO 3后,该反应必须控制的条件是 。
(4)加适量氨水的目的是 ,使加入的(NH 4) 2CO 3能顺利发生复分解反应而生成FeCO 3,则②处反应的化学方程式为 。
(5)用蒸馏水洗涤FeCO 3的目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入适量的BaCl 2溶液,无 产生(填现象),即为洗涤干净。
阅读下面科普短文(有删改)
火炸药的绿色制造技术发展
以硝基化合物为代表的含能材料是火炸药技术的基础,其传统的制造工艺过程会产生含有大量有机物的废酸和废水,环境污染严重,治理费用高,因此火炸药原材料组分传统制造工艺需要进行绿色化和低成本改进,以及积极开发含能材料的绿色合成工艺。
硝基含能化合物的生物合成是火炸药原材料制造技术中最新颖的前沿研究领域,是一种真正绿色合成路线。最具代表性的新型硝化技术是用N2O5作为绿色硝化剂,这一技术的关键是如何制备N2O5和怎样实现N2O5硝化工艺。
研究的N2O5制备方法主要有半渗透膜电解法和臭氧氧化法:
1)半渗透膜电解法是在电解池内用特制的半渗透膜隔开两个电极,电解无水硝酸而生成N2O5;
2)臭氧氧化法是将浓度5%﹣10%的臭氧与氧气的混合物和N2O4进行气相反应生成N2O5。
试验的N2O5硝化工艺主要有2种:
1)用N2O5﹣HNO3﹣N2O4作硝化剂进行硝化;
2)用N2O5和无水HNO3于液态二氧化碳中进行硝化。
南京理工大学研究了用DADN原料在N2O5﹣HNO3体系中绿色硝解制备HMX.以DADN为原料,不同硝解方法的优缺点比较见表:
硝化体系 |
收率/% |
优点 |
缺点 |
HNO3 |
40 |
步骤简单 |
得率低 |
H2SO4﹣NH4NO3﹣HNO3 |
80﹣85 |
工艺成熟 |
废酸量大,难处理 |
P2O5﹣HNO3 |
99 |
得率高,纯度好 |
P2O5和HNO3需大大过量,腐蚀性大 |
N2O5﹣有机溶剂 |
65 |
无需废酸处理 |
得率低,溶剂易挥发 |
N2O5﹣HNO3 |
94 |
得率高,废酸少,硝化剂的过量比小 |
无 |
火炸药的安全使用知识有:防止炸药受热、火焰引起的爆炸;按炸药使用温度使用,不要超过温度条件;禁止长时间阳光照射;禁止电焊、气焊、气割作业等。
依据文章内容,回答下列问题:
(1)文中涉及到的下列物质:P2O5、HNO3、O3、NH4NO3、N2O4中,不包括的物质类别是 (填序号)。
A.单质 B.氧化物 C.酸 D.碱 E.盐
(2)最具代表性的新型硝化技术是用 作为绿色硝化剂。
(3)如表中,以DADN为原料,不同硝解方法比较中,P2O5和HNO3需大大过量,腐蚀性大的硝化体系是 。
(4)火炸药的安全使用还有哪些注意事项 。 (原文已有方法不能重复,任答一点)
2017年5月,中国首次海城天然气水合物(可燃冰)试采成功,成为全球第一个稳定开采可燃冰的国家。可燃冰开采困难重重,原因之一是可然冰极不稳定易爆炸,大甲烷气体涌入大气层,会产生比二氧化碳更为严重的温室效应。置换法是开采方法之一,将CO2液化后进入1500米以下的洋面,就会生成二氧化碳水合物沉人海底,因CO2较甲烷易于形成水合物,因而就可能将甲烷水合物中的甲烷分子置换出来。
(1)甲烷属于 (填“有机物”或“无机物”),其氢元素的质量分数为 。
(2)甲烷燃烧是将化学能主要转化为 能,甲烷燃料电池则是将化学能转化为 能。
(3)下列有关说法正确的是 。
A.开采可燃冰不会产生环境问题 B.二氧化碳水合物的密度比水小
C.可燃冰比二氧化碳水合物稳定 D.可燃冰是一种前景广阔的清洁燃料
(4)可燃冰的微观构成为46个H2O分子形成8个笼,有6个笼中每个笼容纳了1个CH4分子,余下2个笼每个容纳1个H2O分子,则可燃冰中H2O与CH4的分子数之比是 。
(5)一定条件下,甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,产物都是常见双(两)原子分子,请写出反应的化学方程式 。
地壳中的元素分布(质量分数)如图,请回答下列问题。
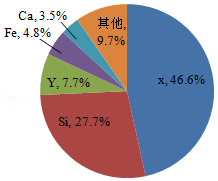
(1)元素X是 ,由X与Y组成的化合物的化学式是 。
(2)地壳中的赤铁矿(Fe2O3)与CO高温反应可炼铁,其中Fe2O3发生了 反应(填“氧化”或“还原”)。
(3)如图是Si与Cl2反应生成SiCl4的图示,请在方框内补充所缺反应物的图示。

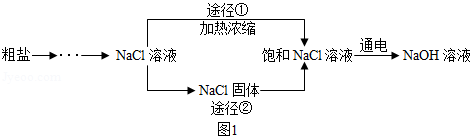
某同学设计的工业制备氢氧化钠的流程如图
1.
资料:2NaCl+2H2O 2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
(1)晾晒海水得到粗盐的原理是
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和______
(3)工业生产中应选择途径 (“①”或“②”),理由是
(4)Cl2可用于生产84消毒液(有效成分 NaClO),反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,反应前后氯元素的化合价有 种。
(5)图2实验测定水组成,不能加入NaCl增强水的导电性的理由是 。电解水的化学方程式为 。
(6)图3实验获得84消毒液,直流电源正极应与 (填a或b)连接,才能使 NaClO的含量更高。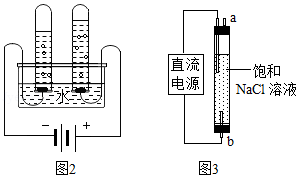
根据实验回答:
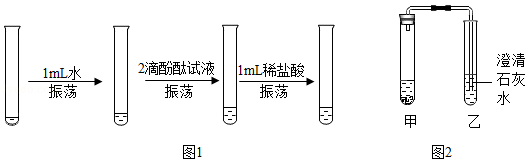
(1)图1实验,用药匙的柄把端挑起一点氢氧化钙粉末于试管中,依次进行实验。观察到现象为:
浑浊→变红→红色消失。
根据现象判断氢氧化钙的性质有 、 (物理和化学性质,各填一条)
(2)按图1实验完毕,所得溶液中除酚酞外一定有的溶质是 ,可能有的溶质是 。
(3)图2装置气密性良好。取0.5g碳酸氢钠于甲中,加入2mL盐酸, (填操作),并将导管伸入澄清石灰水中,观察到出现浑浊。乙中反应的化学方程式为 。
(4)图2中甲作为发生装置还可制得的气体是 (填一种)。
黑火药由硝酸钾、硫磺和木炭组成,爆炸时主要反应的化学反应方程式:
2KNO3+S+3C +N2↑+3CO2↑
+N2↑+3CO2↑
(1)反应涉及的物质中,属于空气主要成分的是
(2)横线上的物质由离子构成,阴离子的符号是
(3)黑火药制作的烟花燃放时,产生的空气污染物有 、 (固体和气体污染物,各填一种)
(4)硝酸钾分解的化学方程式为:2KNO3=2KNO2+O2↑.根据化学反应方程式计算,生成24g氧气需硝酸钾的质量是多少?
我国科学家屠呦呦发现并提纯抗疟疾药物青蒿素(C15H22O5)荣获2015年诺贝尔奖,请计算青蒿素中碳、氢、氧元素的质量比(直接写出结果)