莽草酸(化学式:C7H10O5)是制取抗“H1N1流感”药物“达菲”的原料。请计算:(写出计算过程,并注意格式)
(1)莽草酸分子中C、H、O的质量比;
(2)莽草酸中氢元素的质量分数(精确到0.1%);
(3)174g莽草酸含氢元素的质量:
(4)对1岁以上的儿童推荐按照下列“体重一剂量表”服用“达菲”:
假如患病儿童的体重是35千克,在治疗过程中,需每天服用“达菲”胶囊(每颗胶囊含“达菲”60mg)2次,一个疗程5天,那么该患儿一个疗程共需服用多少颗?
某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①称取25.0g石灰石样品,平均分成两份,并分别加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示:

请回答:
(1)每份样品充分反应后.生成二氧化碳的质量为g;该样品中碳酸钙的质量分数为%.
(2)若每份样品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数。(要求写出计算过程.不考虑水、氯化氢的逸出.结果精确到0.1%)
解:
(3)由图中曲线分析得出,影响该化学反应速率的因索是:.
请另外举出-个生活或生产中控制化学反应速率的实例:.
为测定石灰石中碳酸钙的质量分数,化学兴趣小组的同学设计了以下方案:将94.9g稀盐酸加入到15g石灰石样品中,恰好完全反应。生成的二氧化碳气体全部用足量的
溶液吸收,
溶液增加的质量随时问变化如下表:(友情提示:石灰石中的杂质不参加反应且难溶于水)
| 时间(min) |
t1 |
t2 |
t3 |
t4 |
t |
t6 |
t7 |
t8 |
| 氢氧化钠溶液增加的质量(g) |
1.5 |
2 |
2.5 |
3 |
3.5 |
4 |
4.4 |
4.4 |
求:(1)最终生成
的质量;
(2)样品中
的质量分数(计算结果精确到0.1%);
(3)将石灰石与稀盐酸反应后的剩余物质进行过滤,再向滤液中加入多少克水可以得到10%的
溶液。
纸包皮蛋是一项新技术,制作过程中需要配制料液。某配方料液中含NaOH、
NaCl、红茶末、五香粉等,技术员先配得NaOH、NaCl的昆合液2400g,其中含
80gNaOH,81gNaCl。计算:
(1)混合液中NaOH的质量分数。
(2)如果取24g混合液,加入一定质量3.65%的稀盐酸恰好完全反应,计算所加稀盐
酸的质量。
(3)24g混合液与稀盐酸反应后所得溶液中NaCl的质量分数。
现有一瓶硫酸溶液,为测定其溶质的质量分数,取该溶液
于烧杯中,逐渐加入足量的氯化钡溶液,反应中物质间的质最关系如右图所示。

请计算:
(1)原硫酸溶液中溶质的质量分数。
(2)若取一定量该硫酸溶液配制
溶质的质量分数为
的稀硫酸,需加人水的质量是多
曾多次发生将亚硝酸钠误作食盐用于烹调而引起的中毒事件。亚硝酸钠的化学式为
,试回答:
(1)亚硝酸钠中
、
、
三种元素的质量比为。
(2)亚硝酸钠中氮元素的质量分数为。(结果精确到0.1
)
钢铁的生产和使用是人类文明和社会进步的一个重要的标志。
(1)每年钢铁锈蚀都会造成巨大的损失,铁制品锈蚀的主要原因是。
校课外兴趣小组的同学们去潍坊某钢铁长生铁样品进行实验:将四份不同质量的生铁样品(假定其中只含单质铁和单质碳)分别加到100g质量分数相同的稀硫酸中,充分反应后,测得的实验数据如下表(已知:在标准状况下,22.4LH2的质量为2g)
| 实验序号 |
1 |
2 |
3 |
4 |
| 生铁样品的质量 / g |
2.88 |
5.76 |
9.24 |
10.28 |
| 生成H2的体积(标准状况下)/L |
1.12 |
2.24 |
3.36 |
m |
通过计算回答下列问题:
①上述表格中m的值为。
②根据表中数据计算稀硫酸中H2SO4的质量分数。
某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,取该溶液20g,加入二氧化锰0.5g,完全反应后,称得烧杯内剩余物质的总质量为19.7g。请回答下列问题:
(1)上述过程中生成氧气质量是。
(2)计算该过氧化氢溶液中溶质的质量分数。
钙是维持人体正常功能所必需的元素。右图所示为某种补钙剂"葡萄糖酸钙片"说明书的一部分。试根据图示中的信息回答下列问题:

(1)葡萄糖酸钙中碳、氢、氧、钙的原子个数比为:;
(2)葡萄糖酸钙中钙元素的质量分数为(计算结果精确到0、1%)
(3)按照说明书上用量服用,成人每天摄入的钙元素的质量是g。(计算结果精确到0、01 g)
将104g由氯化钠和氯化钡
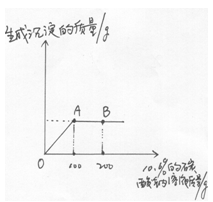
组成的固体混合物溶解于足量水中,向所得溶液中滴加10.6%的碳酸钠溶液,所加碳酸钠溶液的质量与生成沉淀质量关系见右图
①图中表示恰好完全反应的点是,此时溶液中的溶质为。(写化学式)
②求生成沉淀的质量。
③求原混合物中氯化钠的质量分数。
将一定质量的碳酸钠粉末溶于
克水中配制成溶液,取一半该溶液,向其中加入
的盐酸若干克,恰好反应完全,放出气体的质量为
克。试计算:
(1)碳酸钠溶液的总质量;
(2)反应后所得溶液中溶质的质量分数。
乙炔( )是一种重要的化工原料,实验室常用碳化钙( )与水反应制取乙炔,该反应方程式为: 。若要制取 乙炔气体,需要碳化钙的质量是多少克?