某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:
(1)当加入212g稀盐酸时,放出气体的质量为__________g
(2)碳酸钠样品中碳酸钠的质量分数为多少?(写出计算过程)
(3)加入106g稀盐酸(即A点)时烧杯中溶液溶质的质量分数为多少?(写出计算过程)
(4分) 儿童缺锌会引起食欲不振、发育不良.右图为某种补锌口服液说明书的一部分.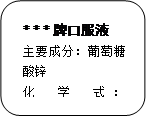
请回答:
(1)该口服液中的锌属于 ▲ (填:“常量”或“微量”)元素;
(2)计算组成葡萄糖酸锌中的碳、氢元素的质量比?
(3)计算葡萄糖酸锌中碳元素的质量分数为多少?(精确到0.1%)
(4)若儿童1kg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半;体重为20kg的儿童每天还须服该口服液 ▲ 支,才能满足身体的需要.
取4g氧化铜固体于烧杯中,向其中加入一定量的稀盐酸,恰好完全反应,得到溶液的质量为40.5g。请计算:该稀盐酸中溶质的质量分数。
化肥对提高农作物的产量具有重要作用,NH4NO3是一种含氮量较高的化肥。
(1)NH4NO3中氮、氢、氧元素的质量比为 。
(2)NH4NO3中氮元素的质量分数为 。
(3)为保证农作物获得70g氮元素,则至少需施用 g NH4NO3。
长期使用的水壶底部结有一层水垢,其主要成分是碳酸钙和氢氧化镁,为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用如图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表
| |
第一次 |
第二次 |
第三次 |
平均值 |
| B装置增加的质量 |
2.17 |
2.22 |
2.21 |
|
分析上面实验与数据后回答;
(1)第一次实验测得数据较低的原因是___________;
(2)平均每份水垢样品中碳酸钙的质量为___________克.
某兴趣小组用如图所示装置制取 ,加热混合物至不再产生气体后,称量试管中剩余固体的质量为 。请计算:
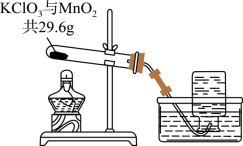
(1)生成 的质量为_____ 。
(2)剩余固体中 的质量分数。
根据
 反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁 的生铁的质量是多少?
铝碳酸镁咀嚼片(主要成分是 )可治疗胃酸过多症,反应原理可用化学方程式表示为 。某化学兴趣小组使用如图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入 片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中。已知 的相对分子质量为 。请计算:
时间( ) |
|
|
|
|
|
|
|
|
读数( ) |
|
|
|
|
|
|
|
|
(1)生成二氧化碳_____ 。
(2)每片该咀嚼片中铝碳酸镁的含量为多少(计算结果保留到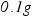 )?
)?

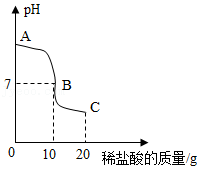
常温下,一锥形瓶中盛有10g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加一定溶质质量分数的稀盐酸,用pH传感器测得溶液pH与加入稀盐酸的关系曲线如图所示,请回答下列问题:
(1)图中B点溶液呈 色。
(2)计算稀盐酸中溶质质量分数。(写出计算过程)
在82.8克碳酸钠溶液中,逐滴加入盐酸,所加盐酸的质量与产生气体的质量关系如图所示(滴加过程中先发生化学反应:Na2CO3+HCl═NaHCO3+NaCl)。试计算(不考虑气体的溶解和盐酸的挥发):

(1)m的值为 。
(2)刚好不再产生气体时,溶液中溶质的质量分数(写出化学方程式及计算过程)。
将50.0g盐酸、氯化镁和氯化铝的混合溶液置于烧杯中,逐滴加入质量分数为20.0%的氢氧化钠溶液,生成氢氧化铝沉淀的最大质量为7.8g。加入氢氧化钠溶液质量和生成沉淀质量的关系如图所示。请根据题意回答问题:
已知:Al(OH) 3+NaOH═NaAlO 2+2H 2O
(1)B点溶液中所含溶质是 (填化学式)。
(2)求图中A点的坐标: 。
(3)原混合溶液中MgCl 2的质量分数是多少?(写出计算过程,计算结果精确到0.1%)

工业盐酸中通常溶有少量的FeCl 3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl 3与NaOH反应的化学方程式为FeCl 3+3NaOH═Fe(OH) 3↓+3NaCl.请回答下列问题:
(1)FeCl 3与NaOH恰好完全反应时,生成沉淀的质量是 g。
(2)该工业盐酸中HCl的质量分数是多少?(写出计算过程)
(3)取l00g该工业盐酸稀释成HCl质量分数为10%的稀盐酸,需加多少克水?(写出计算过程)

某兴趣小组在实验室用硫酸铜溶液和氢氧化钠溶液制取少量氢氧化铜固体。他们的实验过程和相关数据如图所示。请计算:
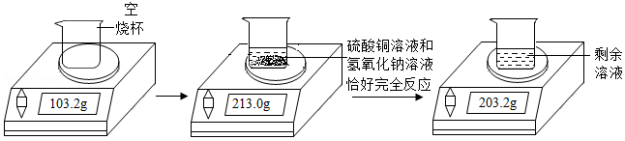
(1)生成沉淀的质量为 g。
(2)恰好完全反应后所得溶液的溶质质量分数。
为了测定某品牌小苏打样品中碳酸氢钠的质量分数,兴趣小组进行了如下图所示的实验(假设该样品中只含有氯化钠一种杂质)。请计算:
(1)生成CO2气体的质量;
(2)样品中碳酸氢钠的质量分数。
为测定某碳酸钠溶液的溶质质量分数,小虎取
该溶液,向其中滴加11.1%的氯化钙溶液直至不再产生沉淀,共用去氯化钙溶液
,反应的化学方程式为:
↓.求:
(1)碳酸钠溶液的溶质质量分数;
(2)反应后所得溶液的溶质质量分数(结果保留至0.1%).