某碳酸钠样品中含有少量氯化钠。现取一定量该样品,加水配制成80g溶液,再加入80g氯化钙溶液,恰好完全反应,过滤后得到溶质质量分数为10%的滤液150g。求:
(1)生成沉淀的质量为 g;
(2)原样品中氯化钠的质量。
造纸是我国古代四大发明之一,它有效地推动了人类文明的发展。
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的污染。秸秆的主要成分是纤维素[
],纤维素中
三种元素的质量比为(用最简整数比表示)。
(2)造纸会产生大量含
的碱性废水,需经处理呈中性后排放。
①检测废水呈碱性的简单方法是。
②若某造纸厂废水中
的质量分数为l.6%,现有废硫酸9.8
(
的质量分数为20%),可以处理的废水质量是多少?(计算过程写在答题卡上)
某化学实验小组要检测黄铜(铜、锌合金)中金属铜的纯度,同学们取20 g黄铜样品,向其中分三次共加入15 g盐酸溶液,充分反应后测得实验结果如下: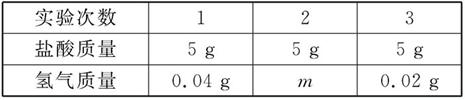
请计算:(1)第2次实验产生氢气的质量m= g。
(2)黄铜(铜、锌合金)中金属铜的纯度。
(3)该盐酸溶液中溶质的质量分数。
某化学兴趣小组,在一次查阅 "关于如何治疗人体胃酸过多"的资料后,决定利用实验室相关仪器(高温消毒)自制小苏打水(NaHCO3水溶液),用来缓解胃酸过多的症状。具体配制步骤(经医生建议)如下:
第一步:准确称量
食品级小苏打粉末;第二步:将第一步所称粉末配成
溶液;
第三步:将第二步所得溶液取出
,再加水配制成
溶液即得到治疗胃酸过多的
小苏打水(密度为
)。
请回答下列问题:
(1)第一步用到的主要仪器是;第二步使用的玻璃仪器有(至少写两种);
(2)第三步配制所得的小苏打水中
的质量分数是 ;
(3)胃酸过多者在医生的指导下,每次喝50mL第三步配制所得的小苏打水,一天两次,则一天可反应掉胃液中的
g。
在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示:

(1)100g稀盐酸中氯化氢的质量.
(2)完全反应后,所得溶液中溶质的质量分数?
某兴趣小组用如图所示装置制取 ,加热混合物至不再产生气体后,称量试管中剩余固体的质量为 。请计算:
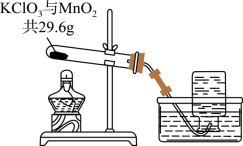
(1)生成 的质量为_____ 。
(2)剩余固体中 的质量分数。
根据
 反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁 的生铁的质量是多少?
铝碳酸镁咀嚼片(主要成分是 )可治疗胃酸过多症,反应原理可用化学方程式表示为 。某化学兴趣小组使用如图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入 片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中。已知 的相对分子质量为 。请计算:
时间( ) |
|
|
|
|
|
|
|
|
读数( ) |
|
|
|
|
|
|
|
|
(1)生成二氧化碳_____ 。
(2)每片该咀嚼片中铝碳酸镁的含量为多少(计算结果保留到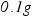 )?
)?

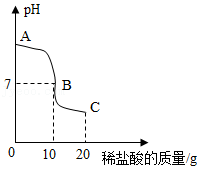
常温下,一锥形瓶中盛有10g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加一定溶质质量分数的稀盐酸,用pH传感器测得溶液pH与加入稀盐酸的关系曲线如图所示,请回答下列问题:
(1)图中B点溶液呈 色。
(2)计算稀盐酸中溶质质量分数。(写出计算过程)
在82.8克碳酸钠溶液中,逐滴加入盐酸,所加盐酸的质量与产生气体的质量关系如图所示(滴加过程中先发生化学反应:Na2CO3+HCl═NaHCO3+NaCl)。试计算(不考虑气体的溶解和盐酸的挥发):

(1)m的值为 。
(2)刚好不再产生气体时,溶液中溶质的质量分数(写出化学方程式及计算过程)。
将50.0g盐酸、氯化镁和氯化铝的混合溶液置于烧杯中,逐滴加入质量分数为20.0%的氢氧化钠溶液,生成氢氧化铝沉淀的最大质量为7.8g。加入氢氧化钠溶液质量和生成沉淀质量的关系如图所示。请根据题意回答问题:
已知:Al(OH) 3+NaOH═NaAlO 2+2H 2O
(1)B点溶液中所含溶质是 (填化学式)。
(2)求图中A点的坐标: 。
(3)原混合溶液中MgCl 2的质量分数是多少?(写出计算过程,计算结果精确到0.1%)

工业盐酸中通常溶有少量的FeCl 3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl 3与NaOH反应的化学方程式为FeCl 3+3NaOH═Fe(OH) 3↓+3NaCl.请回答下列问题:
(1)FeCl 3与NaOH恰好完全反应时,生成沉淀的质量是 g。
(2)该工业盐酸中HCl的质量分数是多少?(写出计算过程)
(3)取l00g该工业盐酸稀释成HCl质量分数为10%的稀盐酸,需加多少克水?(写出计算过程)

某兴趣小组在实验室用硫酸铜溶液和氢氧化钠溶液制取少量氢氧化铜固体。他们的实验过程和相关数据如图所示。请计算:
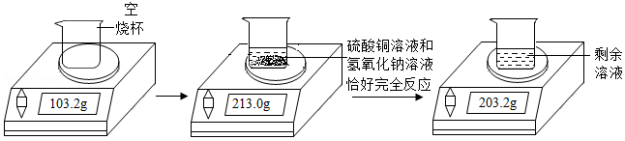
(1)生成沉淀的质量为 g。
(2)恰好完全反应后所得溶液的溶质质量分数。
为了测定某品牌小苏打样品中碳酸氢钠的质量分数,兴趣小组进行了如下图所示的实验(假设该样品中只含有氯化钠一种杂质)。请计算:
(1)生成CO2气体的质量;
(2)样品中碳酸氢钠的质量分数。
为测定某碳酸钠溶液的溶质质量分数,小虎取
该溶液,向其中滴加11.1%的氯化钙溶液直至不再产生沉淀,共用去氯化钙溶液
,反应的化学方程式为:
↓.求:
(1)碳酸钠溶液的溶质质量分数;
(2)反应后所得溶液的溶质质量分数(结果保留至0.1%).