2020年9月,中国向世界宣布了2030年前实现碳达峰、2060年前实现碳中和的目标。
(1)为减缓大气中二氧化碳含量的增加,下列措施可行的是 (填序号)。
A.植树造林,开发和利用太阳能、水能、风能等新能源
B.禁止使用煤、石油、天然气等化石燃料
(2)绿色植物通过光合作用吸收二氧化碳,生成葡萄糖并放出氧气,其反应的化学方程式:6CO2+6H2O 葡萄糖+6O2,则葡萄糖的化学式为 。若吸收44g二氧化碳,理论上可释放出氧气 g。
葡萄糖+6O2,则葡萄糖的化学式为 。若吸收44g二氧化碳,理论上可释放出氧气 g。
(3)近年我国科学家合成了一种新型催化剂,可将二氧化碳和氢气转化为清洁的液体燃料甲醇(CH3OH)和水,该反应的化学方程式为 。
(4)将一氧化碳和二氧化碳的混合气体3.2g通过足量灼热氧化铜粉末,充分反应,将所得的气体全部通入足量的氢氧化钡溶液中,气体全部被吸收,生成白色碳酸钡沉淀,溶液质量减少15.3g。则原混合气体中碳、氧元素的质量比为 (填最简比)。
探秘火星上的化学物质
2021年5月15日,我国自主研制的天问一号搭载祝融号火星车,成功登陆火星。
研究表明,火星上有大气,但总量很小,密度只有地球空气的1%左右,主要成分是二氧化碳,年平均气温﹣55℃,冬季最低至﹣133℃,夏季最高至27℃。火星地表没有发现水,但地表下发现有水冰的痕迹,并有大量干冰。土壤及岩石中含有的无机盐跟地球相似,表层土壤主要为氧化铁。到目前为止,火星上还没有发现生命迹象。
(1)下表是火星大气及土壤的部分成分。请你完善下表信息:
成分 |
二氧化碳 |
氮气 |
氩气 |
氧气 |
水蒸气 |
碳酸钙 |
构成微粒 (写符号) |
||||||
体积分数 |
95.3% |
2.7% |
1.6% |
0.15% |
0.03% |
/ |
(2)已知干冰在﹣78.5℃升华。一年四季火星大气中二氧化碳的含量波动较大,原因是 。
(3)移居火星是人类的梦想,根据题中信息回答:跟地球相比,火星上没有或含量不足以支持人类生命活动的基本物质有哪些? 。
(4)要在太空中制取氧气、水和铁,有关物质的信息如下:
资料1.用铁酸镍(NiFe2O4)做催化剂,用舱外太阳能电池发电,通电分解二氧化碳可生成氧气和碳。
资料2.氮气的沸点﹣196℃;氢气的沸点﹣253℃;肼(分子式为N2H4,读音:jing)的沸点114℃;肼是一种无色、易挥发、有刺激性气味的油状液体,有腐蚀性,能腐蚀玻璃和橡胶,有剧毒。肼是航空器上常用的燃料。
请根据提供的信息,探究制取氧气、水和铁的方法。
①在密闭的太空舱中,用资料1中的方法制备氧气的优点是 ,该反应的化学方程式为 。
②肼在氧气中燃烧是否有可能获得水?请说明理由 。
③已知肼在金属铂(Pt)的催化作用下,常温即可分解产生氢气和氮气。反应的化学方程式为 。写出从氢气、氮气混合气体中分离出氢气的依据 。分离出的氢气在氧气中燃烧可制得水。
④根据资料2中肼的性质,在使用肼制取氢气时,为保障安全,需要注意的问题有 。
⑤以资料1中二氧化碳分解产生的碳、火星大气中的二氧化碳和火星土壤中的氧化铁为原料制备金属铁,反应的化学方程式为 。
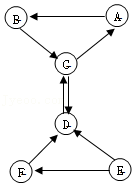
A~F为初中化学常见的物质。D、E、F为不同类别的化合物,A是C通过绿色植物光合作用产生的气体,E是常用的食品干燥剂。它们的转化如图所示(“→”表示一种物质可以转化为另一种物质,部分反应物、生成物和反应条件已略去)。请回答。
(1)A物质是 。
(2)B物质所属的类别是 (填“单质”、“氧化物”、“酸”、“碱”或“盐”)。
(3)E→F的反应 (填“吸收”或“放出”)热量。
(4)F→D发生复分解反应的化学方程式为 。
江西赣州被誉为“世界钨都”,钨(W)是一种重要的战略资源。如图是一种生产钨的工业流程:
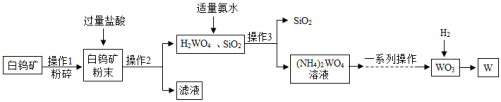
已知:白钨矿的主要成分是钨酸钙(CaWO4),还含有CaO、SiO2等;碳在高温条件下会与金属钨反应生成碳化钨。
(1)操作1中粉碎白钨矿的目的是 。
(2)操作2所得滤液中一定含有的阳离子是 、 。
(3)流程中氨水(NH3•H2O)和H2WO4反应生成(NH4)2WO4的化学方程式为 。
(4)用氢气还原WO3可获得高纯度的钨,此处不宜用焦炭代替氢气的原因是 。
(1)操作1中粉碎白钨矿的目的是增大反应物接触面积,加快反应速率;
(2)白钨矿的主要成分是钨酸钙(CaWO4),还含有CaO、SiO2,加入盐酸后二氧化硅没有参加反应,所以操作2所得滤液中一定含有的阳离子是Ca2+和过量的盐酸中的H+;
(3)反应物是NH3·H2O和H2WO4生成物是(NH4)2WO4,所以方程式是:2NH3·H2O+H2WO4═(NH4)2WO4+2H2O
(4)碳在高温条件下会与金属钨反应生成碳化钨,所以此处不宜用焦炭代替氢气。
2017年4月,"航母"下水,开拓中国新蓝海。
(1)"航母"舰体材料为合金钢,国产航母使用的"超级钢"具有极佳的抗压性、延展性和焊接性。合金钢是 (填序号)
a.合成材料 b.复合材料 c.无机材料
(2)"航母"升降机可由铝合金制造,用石墨作电极在高温条件下电解熔融氧化铝,在阴极和阳极区分别得到A1和O 2,阳极区使用的石墨易消耗的原因是 。
(3)"航母"螺旋浆可由铜合金制造。铜合金比铜的硬度 (填"大"或"小"),铜比铁在海水中耐腐蚀的原因是 。
(4)由生铁炼钢时,硅(Si)与氧化亚铁在高温条件下反应生成二氧化硅和铁,该反应的化学方程式为

用盐酸可以清除铁锈(主要成分为Fe203),盐酸中主要含有H20分子、H+、c1﹣.某探究小组为探究稀盐酸中的哪种微粒能使氧化铁溶解,设计了如下实验方案,得出了初步结论.
(1)请填写下表中的实验结论:
| 实验过程 |
实验现象 |
实验结论 |
| 向盛有少量Fe2O3的试管中加入NaCl溶液振荡 |
固体不溶解 |
|
(2)是否需要做“向Fe2O3,中加入水”的对比实验?为什么?
如图所示,A瓶盛有澄清的石灰水,B瓶盛有紫色石蕊试液,C杯有高低不同的燃着的蜡烛。回答下列问题:
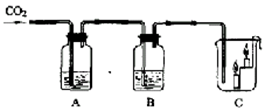
(1)A处澄清石灰水变浑浊了,写出这个过程发生的反应(用化学方程式表示)_____ ___
(2)B处紫色石蕊试液变红,这是因为( )
| A.二氧化碳使紫色石蕊变红 |
| B.水使紫色石蕊变红 |
| C.二氧化碳可使澄清石灰水变浑浊 |
| D.二氧化碳与水反应生成的碳酸使紫色石蕊变红 |
(3)C处出现的现象_____ ______;由此总结二氧化碳具有的性质:
①_____ _ _____;②_______ ____。
根据下列装置图,回答有关问题:

A B C D E F
(1)图中标有a的仪器名称是 。
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是 (填字母),以高锰酸钾为试剂利用此装置制取氧气时,还要做的改进是 ,其作用是 。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气的符号表达式为 ,若要制取并收集一瓶较干燥的氧气,应选用的装置组合为 (填字母),检验氧气是否收集满的方法为 。
(4)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂。现有一根洁净的铜丝,实验前先将其绕成螺旋状,然后将其灼烧(Cu+O2→CuO)。改进后的发生装置如图F所示(己略去夹持装置)。
①铜丝绕成螺旋状的作用是 (填字母)。
A.收集到更多的02 B.加快反应速率 C.没有影响
②与装置B比较,改进后装置的优点是 。
(5)氨气是一种无色、有强烈刺激性臭味的气体,极易溶于水,溶于水形成氨水。实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气。某兴趣小组的同学设计如图G~J所示装置对氨气的制取、性质进行探究。

①装置I中的现象是__________________________。
②根据氨气的性质,J处应选择的最佳收集装置为_________(填“K”、“L”或“M”)。
③装置H的作用是___________________________。
气体的实验室制取是初中非常重要的一组实验,结合下列实验装置图回答有关问题:

(1)仪器名称:①是 。
(2)用黑色笔画出D的装置图象(用导管和集气瓶)。
(3)某同学选用过氧化氢溶液制氧气,他选择的发生装置是 (填序号、下同),收集纯净一瓶氧气应选收集装置是 。
(4)某同学想用KClO3和MnO2制取氧气,若选择A和C装置制取并收集氧气.则要对A装置进行的改进是 ,证明氧气已收集满的方法是 ;某同学尝试在KClO3中加少量的KMnO4,结果也能加快KClO3的分解,用文字说明其原因 。
(5)另一同学学习氧气制取后,总结了制取气体的规律,选用的发生装置应考虑___________ (填下列编号,下同),收集装置应考虑__________。
①反应物的状态 ②气体的密度 ③气体是否溶液于水 ④反应条件是否加热 ⑤是否与空气成分反应
请根据下图回答下列问题:

(1)指出下列编号仪器的名称:X ;Y 。
(2)实验室某同学用高锰酸钾为原料制取氧气时,应选用 (填装置编号 )作发生装置,该反应的符号表达式为: ,若收集一瓶氧气,供硫在氧气中燃烧的实验使用,最好选用气体的收集装置中的 (填装置序号)。最后他还发现水槽内的水显红色,请你帮他分析一下原因是:___ _ 。
(3)写出实验室用H2O2制取氧气的表达式为 ,
(4)选用D装置收集氧气的原因是 。
(5)李刚同学想用装置F来收集氧气,氧气应该从 (填导管编号a或b,下同)通入,若用装置BFG组合来测定过氧化氢溶液生成氧气的体积,应先在集气瓶中装满水,然后将导管 和c导管连接。
(6)某同学制氧气时,试管炸裂了,造成试管炸裂的原因可能是下列中的
①没有给试管均匀预热;②试管外壁潮湿;③试管口没有略微向下倾斜;④忘了在试管口加一团棉花;⑤加热时试管与灯芯接触;⑥收集完氧气,先撤酒精灯;⑦高锰酸钾中混有可燃物
| A.①②③④⑤⑥⑦ | B.①②③⑤⑥⑦ |
| C.①②③④⑤ | D.①②③⑤ |
(7)实验室内用块状固体碳化钙与水反应制取乙炔(C2H2),该反应比二氧化锰催化过氧化氢分解更加激烈,所选发生装置最合适的是( )

右图有多种功能,如收集气体、洗涤气体、贮存气体等。回答下列问题: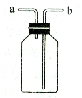
(1)如果用该装置收集二氧化碳(密度比空气大),则二氧化碳从哪端进入集气瓶?
(2)如果用该装置收集氢气(密度比空气小),则氢气从哪端进入集气瓶?
(3)该装置中预先盛满水,将水排出用来贮气,则气体从哪端进入集气瓶?
结合下图所示实验装置回答问题:


(1)实验室若用高锰酸钾制取氧气,可选用的发生和收集装置是________(填标号),反应表达式为:____________。
(2)检查装置A气密性的方法是________。
(3)装置B与C组合,可以制取的氧气,反应的反应表达式为:________,能用装置C收集该气体的原因是_________。
(4)一种洗气装置如下图所示,为了除去二氧化碳中混有的少量水分,气体应从________(填“a”或“b”)端导管口通入。【浓硫酸课吸收水蒸气,不吸收二氧化碳】
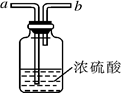
(5)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷。制取甲烷的发生装置应选择_____(填装置编号,下同),收集装置应选_____。
同学们利用装修后剩下的大理石碎片进行相关实验.
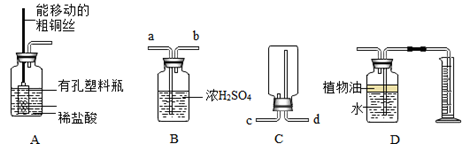
(1)一位同学设计了装置A制取CO2,该装置能通过上下移动穿过橡胶塞的粗铜丝来控制反应的发生或停止.大理石碎片应放在 中,A中反应的化学方程式为 .
该反应属于 反应(填基本反应类型).根据气体制备的一般原则,A中的粗铜丝能否用铁丝代替 (填“能”或“不能”),原因是 .
(2)浓H2SO4具有强烈的吸水性,可作为干燥剂除去某些气体中的水份.如用装置B干燥CO2,则CO2应从 (填字母)端口通入.
(3)如用装置C收集CO2,则CO2应从 (填字母)端口通入.
(4)装置D用于通入CO2将水压入量筒中以测量CO2的体积,植物油的作用是 .
某合金由铝、铁、铜三种金属组成.现要测定一定质量该合金中铝的质量.设计以下流程并实验。
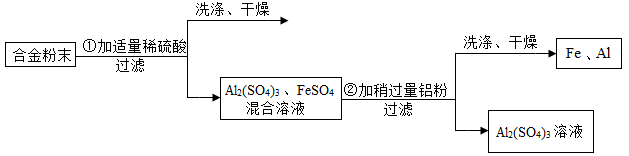
(1)通过以上实验也可验证三种金属的活动性顺序,写出判断依据.
(2)为什么要向合金粉末中加人适量的稀硫酸?
(3)为达到实验目的,需要称量上述流程中哪些物质的质量?如何确定铝的质量?
、
是生活中常见的盐,某实验小组通过以下实验来研究者离子物质的性质(已知:
、
的水溶液呈碱性;
受热易分解生成
、
和
).
(1)称取两种固体各1g分别放入两支试管中,再加入5mL水,振荡.固体充分溶解,并恢复至室温;
①发现
完全溶解,而
有剩余.由此得出结论:在相同温度下,;
②向所得溶液中各滴入1~2滴酚酞溶液后,溶液均呈 色。
(2)①取少量
按如图装置进行实验,可观察带的现象是:大试管口有水珠生成,;
②用的方法除去混在
粉末中少量的
。

(3)测定
样品(含
杂质)中
的质量分数:
①称取mg样品放入烧杯中加水溶解;
②加入过量的
溶液充分反应,反应的化学方程式为;证明反应后
有剩余的方法是;
③过滤、洗涤、干燥,称量测定的质量为ng.则样品中
的质量分数为.