重庆市初中毕业学业考试化学试卷
在下列变化中,有一个变化与其他变化的本质不同,该变化是( )
| A.石蜡融化 | B.纸张燃烧 | C.酒精挥发 | D.冰雪融化 |
2011年,我国进一步加大了对酒后驾车的查处力度,取得明显效果。交警使用的一种酒精检测仪中装有重铬酸钾(K2Cr2O7),重铬酸钾(K2Cr2O7)能够和已醇发生化学反应,通过反应现象判断驾驶员是否饮酒。该物质(K2Cr2O7)中,铬元素的化合价为( )
| A.+4 | B.+5 | C.+6 | D.+7 |
下列有关说法中,正确的是( )
| A.原子不显电性,是因为原子中不存在带点的粒子 |
| B.水通电产生氢气和氧气,说明水中含有氢分子和氧分子 |
| C.在化学反应中,反应前后的原子的种类没有改变,数目没有增减 |
| D.不同元素最本质的区别在是相对原子质量不同 |
下列宣传用语中,你认为不科学的是( )
| A.用甲醛水溶液浸泡的水产品,新鲜、口感好,可以放心食用 |
| B.使用含氟牙膏可预防龋齿 |
| C.蔬菜、水果能提供和补充多种维生素 |
| D.缺铁会引起贫血 |
下列分析判断正确的是( )
| A.酸能够使紫色石蕊溶液变红,二氧化碳能使紫色石蕊溶液变红色,所以二氧化碳是酸 |
| B.铁、铜都是金属单质,都能够置换出盐酸、稀硫酸中的氢 |
| C.氧化物中含有氧元素,但是含有氧元素的化合物不一定是氧化物 |
| D.点燃的木条伸入某无色气体中会熄灭,证明该无色气体一定是二氧化碳 |
使用右图装置可以进行下列实验中的( )
| A.锌与稀硫酸制取、收集氢气 |
| B.KClO3与MnO2制取、收集氧气 |
| C.KMnO4制取、收集氧气 |
| D.过氧化氢溶液与MnO2制取、收集氧气 |
下列各组物质中,在通常情况下不能发生化学反应的是( )
| A.铁与硫酸铜溶液 | B.氢氧化镁与稀盐酸 |
| C.碳酸钠与稀硫酸 | D.氮气和氧气 |
用化学符号或者化学式填写:
⑴2个氢原子 ; ⑵五氧化二氮分子 ;
⑶食盐水中的溶质 ;⑷地壳中含量最高的金属元素 。
请你从提供的试剂中选择一种试剂,除去氧气中混有的二氧化碳杂质。
提供的试剂有:①氢氧化钠溶液;②稀盐酸;③水。
你选择的试剂是 (填序号),发生反应的化学方程式是 ;在此处在过程中,氧气中又混入了其他杂质,该杂质是 。
相同质量的M、N两种活泼金属,分别与足量的稀盐酸在室温下发生反应(M、N在生成物中的化合价为均为+2价),生成H2的质量m和反应时间t的关系如右下图所示。
⑴金属活动顺序是M比N (填“强”或“弱”);相对原的相对原子质量是M比N的 (填“大”或“小”)。
⑵M与稀盐酸反应结束后,消耗稀盐酸中溶质的质量为 g。
请你选择有利于“双城同建,工件大美临沂”的做法,请讲序号填在横线上。
①工业废气、废水直接排放;②分类回收垃圾;③增大绿地面积;④合理使用农药、化肥;⑤使用节水水龙头;⑥开发利用太阳能、风能和氢能;⑦鼓励农民将秋后农作物秸秆焚烧。你选择的是 。
纳米材料和纳米技术的应用涉及现代工业的各个领域。用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体。请你写出该反应的化学方程式 。
食品保鲜的措施有添加防腐剂、充填气体、放置干燥剂和脱氧剂等。根据物质的性质选用合适的物质用于食品保鲜,对于保证食品安全和人体健康具有重要的意义。
⑴氮气是常用的充填气体。你认为选用氮气的主要原因是 。
⑵生石灰是常用的干燥剂。请你用化学方程式表示选用生石灰的原因 。
已知:A是相对分子质量最小的氧化物,D是最简单的有机物,也是天然气中最主要的成分。请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题。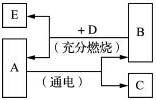
⑴请写出D、E的化学式:D 。E 。
⑵请写出AB+C的化学方程式: ;该反应的基本类型是 。
几位同学在实验室做木炭还原氧化铜的实验,实验完毕后,他们发现试管内仍有黑色固体物质存在。该试管中的黑色固体物质是什么?
【提出猜想】
小玉同学:木炭。
小兰同学:氧化铜。
小华同学:木炭和氧化铜。
【查阅资料】
木炭、铜都不与稀硫酸反应;Na2O、MgO、CuO、Fe2O3等金属氧化物能与稀硫酸反应生成盐和水。
【实验设计】
方案一:向盛有黑色固体的试管中加入足量的稀硫酸,充分振荡,静置后观察现象。
方案二:取少量该黑色固体在空气中灼烧,观察现象。
他们对“方案一”进行了分析讨论,达成了共识:若试管内溶液无色、还有黑色固体存在,证明 同学的猜想正确。若试管中溶液呈蓝色、无黑色固体,证明 同学的猜想正确。若出现的现象是 ,证明小华同学的猜想是正确的,发生反应的化学方程式为 。
他们按照“方案二”进行了实验操作,记录如下:
| 实验现象 |
实验结论 |
| 黑色固体红热并逐渐减少,最后消失 |
该黑色固体是 。 反应的化学方程式是 |
一瓶氢氧化钠固体,因不慎敞口放置了一段时间,已经部分变质。化学课外兴趣小组的同学决定测定该瓶试剂变质的程度,他们在知识回顾的基础上,依次进行了如下的实验操作:
知识回顾:氢氧化钠必须密封保存;氢氧化钠与二氧化碳反应生成Na2CO3和H2O;CaCO3不溶于水。
第一步:取该瓶中的试剂20g加水配制成溶液;
第二步:向上述溶液中加入足量的澄清石灰水;
第三步:过滤、干燥、称量,生成沉淀为5g。
⑴若该瓶试剂中的Na2CO3的质量分数为A,则氢氧化钠的质量分数 (填大于、等于或小于),原因是 。
⑵计算该20g试剂中含有杂质Na2CO3的质量分数(结果精确到0.1%)。
家庭厨房中常发生下列变化,其中属于物理变化的是()
| A. | 食物腐败 | B. | 水沸腾 |
| C. | 天然气燃烧 | D. | 菜刀生锈 |
当前,食品安全问题备受人们关注,但应该区别违法食品添加剂与正常食品添加剂。做馒头的过程中禁止添加的是 ( )
| A.小苏打 | B.增白剂 | C.蔗糖 | D.食盐 |
下列物质的工业制法中没有发生化学变化的是 ( )
| A.蒸发液态空气得到氧气 | B.铁矿石冶炼成生铁 |
| C.煅烧石灰石得到二氧化碳 | D.粮食发酵得到乙醇 |
全球最大瓦斯脱氧液化项目已经在綦江县安稳镇开工,力争在今年底竣工投入使用,届 时可满足近百万户家庭的用气需求。瓦斯中的主要可燃性气体是 ( )
| A.O2 | B.CO2 | C.N2 | D.CH4 |
02和CO2是动植物生命活动中不可缺少的两种气体,它们的相同点是 ( )
| A.都能供动植物呼吸 | B.都是植物光合作用的原料 |
| C.都难溶解于水 | D.都是空气中的固定成分 |
制作一件生活用品往往要用到多种材料,制作下列用品所列出的材料中都是有机合成材料的是 ( )
| A.雨伞:尼龙绸伞布、不锈钢伞骨 | B.牙刷:尼龙刷毛、塑料刷柄 |
| C.夹钳:钢钳嘴、橡胶钳柄 | D.导线:铜丝芯、塑料皮 |
下列叙述错误的是 ( )
| A.金属汞由汞原子直接构成 | B.原子核由电子和质子构成 |
| C.水分子保持水的化学性质 | D.化学变化中原子不能再分 |
英国科技人员研制出自动灭火陶瓷砖,这种砖砌成的房屋发生火灾时,在高温烘烧下,
砖会裂开并喷出氦气和二氧化碳。自动灭火陶瓷砖的灭火原理是 ( )
| A.清除可燃物 | B.降低温度 | C.降低可燃物着火点 | D.隔绝氧气 |
以下化学反应都是高中将要学习的内容,其中属于置换反应的是
A.Fe+S FeS FeS |
B.2Na+2H20==2NaOH+H2↑ |
| C.Cl2+H20="=HCl+HCl0" | D.3N02+H20==2HN03+NO |
下列实验方法不可行的是 ( )
| A.用过滤的方法软化硬水 |
| B.用澄清石灰水区别C0和C02 |
| C.用酚酞试液区别食盐水和石灰水 |
| D.用熟石灰区别化肥氯化钾和硝酸铵 |
分类是学习化学的常用方法,下列物质的归类完全正确的是 ( )
| A.碱:熟石灰、烧碱、纯碱 |
| B.氧化物:S02、KCl03、H2O |
| C.合金:生铁、不锈钢、黄铜 |
| D.化石燃料:石油、煤、木材 |
下列化学反应不能够发生的是 ( )
A.硝酸银溶液与稀盐酸 8.稀硫酸与氯化钡溶液
C.金属银与硫酸铜溶液 D.金属镁与稀盐酸
人们常说:①高原上缺氧②海产品中含锌③胃酸过多④硬水中含镁离子。请用
化学符号表示:
①中的 “氧” ; ②中的“锌” ;
③中的“酸” ;④中的“镁离子” 。
有些食品袋里装有一小袋铁粉作保鲜剂,它利用了钢铁生锈的化学原理,所以有
人称它为“双吸剂”,这里的“双吸”是吸收空气中的 这两种物
质。有一袋铁粉使用了一段时间,表面已经生锈,但经过验证它还可以继续使用,其验
证方法是加入过量稀盐酸,能观察到的现象是 。
加稀盐酸后发生反应的化学方程式为:
; 。
硫酸既是重要的化工产品,又是重要的化工原料,还是实验室重要的化学试剂。
(1)将浓硫酸滴到布条上,放置一会儿后可以观察到布条变成 色。
(2)浓硫酸运输过程中出现泄漏通常用熟石灰进行处理,其化学方程式为:
。
(3)浓硫酸能与金属铜反应,化学方程式为:Cu+2H2S04(浓)  CuS04 +2H2O+X,
CuS04 +2H2O+X,
X的化学式为 。
我国以食盐加碘方式防治碘缺泛病,碘盐就是在普通食盐中加入碘酸钾(KI03)。

(1)碘酸钾中碘元素(I)的质量分数是 。
(2)碘酸钾高温下容易分解,所以炒菜宜在起锅前才加食盐。有人认为高温下碘酸钾会
首先分解为碘化钾,化学方程式是2KIO3  2KI+302↑,该反应前后,碘元素
2KI+302↑,该反应前后,碘元素
的化合价是 (填“升高”、“降低”或“没变”)。
(3)日本地震造成了核泄漏,我国部分地区监测到了极微量的人工放射性核素
碘一131,该碘原子的结构示意图如右图所示。碘元素核电荷数是 ;
下列原子对府的元素与碘元素化学性质相似的是 。
甲、乙、丙三种固体物质的溶解度曲线如下图所示。
(1)30℃时,丙的溶解度是 。
(2) 5℃时,取甲、乙、丙三种固体物质各20g分别加入盛有lO0g水的烧杯中,充分搅拌后得到的溶液,能够饱和的是
物质的溶液。又将三个烧杯中的混合物温度都升高到30℃,所得溶液溶质质量分数的大小关系是
。
某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2。小青同学设计了以下实验方案来除去可溶性杂质。
(1)步骤①的化学方程式为 。
(2)步骤②中得到的白色沉淀是 (填化学式)。
(3)步骤③中加稀盐酸是为了除去溶液中的 。
| A.CaCl2 | B.MgCl2 | C.NaOH | D.Na2C03 |
实验室常用下列装置制取和收集气体,请根据下图回答有关问题。

(1)如果用高锰酸钾制取02,反应的化学方程式为 ,
你选择的发生装置是 ,你不能选择的收集装置是 。
(2)小红同学用石灰石与稀盐酸反应制取二氧化碳,反应的化学方程式为:
.
她应选用的发生装置是 ,若用右图装置进行“排空气法”收集CO2,请把图中的“导气管”补画完整。
今年我县各学区都进行了部分学生化学实验操作竞赛,某学区竞赛题目之一是“配制70g20%的氯化钠溶液”。该实验的部分操作如下图所示。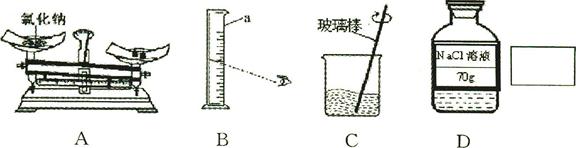
(1)需要称取氯化钠的质量是 g,称量时A出现了右盘低的现象,接下来的操作应该是 。
①左边的平衡螺丝向左调 ②右边的平衡螺丝向右调
③右盘中减少砝码 ④左盘中增加食盐
(2)B中仪器a的名称是 。量取水时,如果按照图B的方法读数,会使配制的溶液溶质质量分数 (填“偏大”或“偏小)。
(3)C中用玻璃棒搅拌的作用是 。
(4)D中所贴标签有不妥之处,请划掉不妥的地方,并在方框中写出你认为适合的内容。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号