某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2。小青同学设计了以下实验方案来除去可溶性杂质。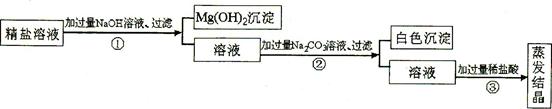
(1)步骤①的化学方程式为 。
(2)步骤②中得到的白色沉淀是 (填化学式)。
(3)步骤③中加稀盐酸是为了除去溶液中的 。
| A.CaCl2 | B.MgCl2 | C.NaOH | D.Na2C03 |
某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2。小青同学设计了以下实验方案来除去可溶性杂质。
(1)步骤①的化学方程式为 。
(2)步骤②中得到的白色沉淀是 (填化学式)。
(3)步骤③中加稀盐酸是为了除去溶液中的 。
| A.CaCl2 | B.MgCl2 | C.NaOH | D.Na2C03 |