复方碳酸氢钠片是一种常用的抗酸剂药物,口服后能迅速中和或缓冲胃酸,减少疼痛等症状。复方碳酸氢钠片的主要成分是碳酸氢钠(与盐酸反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑)。
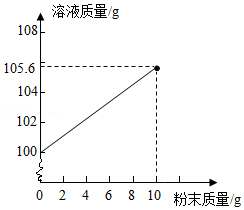
某科学兴趣小组为了测定药片中碳酸氢钠的含量做了以下实验:先将复方碳酸氢钠片制成粉末,取10克分多次放入盛有100克稀盐酸的烧杯中充分反应。测出加入的粉末质量和反应后的溶液质量,两者质量关系如图所示。
(1)实验后,兴趣小组又往烧杯中加入少量粉末,观察到 ,说明上述实验结束时稀盐酸过量。
(2)计算复方碳酸氢钠片中碳酸氢钠的含量。
(3)计算10克粉末与稀盐酸反应后所得氯化钠溶液的溶质质量分数。(计算结果精确到0.1%)
有一包白色粉末,可能含氯化钠、氢氧化钠、碳酸钠中的一种或几种,为了确定其组成,小明称取了9.3克粉末,向其中加入100克7.3%的稀盐酸充分反应,生成的二氧化碳气体完全逸出(忽略其他物质逸出),所得溶液的质量为107.1 克。用pH试纸检测溶液呈中性。
(1)产生二氧化碳气体的化学反应方程式为 。
(2)这包白色粉末的成分为 。
(3)求所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)
一种制备氢氧化镁的生产流程如图所示,MgCl 2和NaOH按恰好完全反应的比例加料。
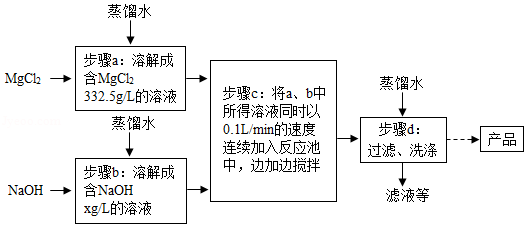
(1)写出步骤c中发生反应的化学方程式: 。
(2)x= 。
(3)过滤得到的粗产品还要经过洗涤,洗涤时主要除去的杂质是 。
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是 。
①盐酸 ②氯化钙 ③氨水 ④硫酸镁
为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有146g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为162.2g。计算:
(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数;
(3)反应后所得溶液中溶质的质量分数(结果精确至0.1%)。
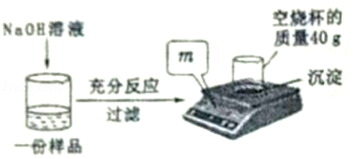
为测定某CuSO 4溶液中溶质的质量分数,取150g CuSO 4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见表。请计算:
| |
实验1 |
实验2 |
实验3 |
| 样品质量/g |
50 |
50 |
50 |
| NaOH溶液质量/g |
20 |
40 |
60 |
| m/g |
44.9 |
49.8 |
49.8 |
(1)50g CuSO 4溶液完全反应时,所得沉淀的质量为 g。
(2)CuSO 4溶液中溶质的质量分数。
取氯化钡和盐酸的混合溶液100g于烧杯中,向其中滴加碳酸钠溶液,产生气体或沉淀的质量与加入的碳酸钠溶液质量的关系如图所示,请回答:
(1)产生沉淀的质量为 g。
(2)x的值为 。
(3)求所用碳酸钠溶液中溶质的质量分数(请写出计算过程)。

硝酸是一种重要的酸,可用于生产化肥、染料和炸药。工业上利用氮的氧化物、氧气与水反应制备硝酸。
(1)某常见氮的氧化物中N、O两种元素的质量比为7:16,则该化合物的化学式为 。
(2)将该氮的氧化物23.0g与足量的氧气缓慢通入一定量水中(NO x+O 2+H 2O→HNO 3),得到60.0g硝酸溶液溶液的溶质质量分数为多少?(写出计算过程)
如图四个图象不能正确反映对应变化关系的是( )
A. 把NaOH和NH4NO3固体分别溶于水中
把NaOH和NH4NO3固体分别溶于水中
B. 分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量
分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量
C. 向一定质量硝酸铜和硝酸银的混合溶液中逐渐加入锌粉
向一定质量硝酸铜和硝酸银的混合溶液中逐渐加入锌粉
D.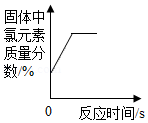 加热一定质量氯酸钾和二氧化锰的固体混合物
加热一定质量氯酸钾和二氧化锰的固体混合物
某兴趣小组取CaCO 3和CaCl 2的固体混合物7.5g,加入到盛有一定质量某浓度稀盐酸的烧杯中,恰好完全反应,气体全部逸出后,所得不饱和溶液的质量为41.8g。
烧杯及烧杯内物质质量随反应时间变化如表。
| 反应时间 |
0 |
t 1 |
t 2 |
t 3 |
| 烧杯及烧杯内物质质量 |
64 |
62.9 |
61.8 |
61.8 |
计算:
(1)生成CO 2的质量为 g。
(2)烧杯中原有稀盐酸的溶质质量分数是多少?
读图识图是学习化学的重要手段。下列四个图象中不能正确反映对应变化关系的是( )
A. 向一定量的饱和石灰水中加入少量生石灰
向一定量的饱和石灰水中加入少量生石灰
B.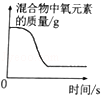 加热氯酸钾和二氧化锰的混合物制取氧气
加热氯酸钾和二氧化锰的混合物制取氧气
C.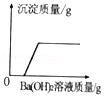 向一定量的稀盐酸和硫酸钠的混合溶液中加入Ba(OH)2溶液
向一定量的稀盐酸和硫酸钠的混合溶液中加入Ba(OH)2溶液
D. 将形状相同质量相等的铁和锌分别加入到足量的质量和浓度都相等的稀硫酸中
将形状相同质量相等的铁和锌分别加入到足量的质量和浓度都相等的稀硫酸中
化学兴趣小组要测定制作叶脉书签所用氢氧化钠溶液的浓度。取40g该氢氧化钠溶液于锥形瓶中,加入数滴酚酞溶液后再滴加质量分数为10%的稀硫酸,当锥形瓶中液体由红色恰好变成无色时,消耗稀硫酸的质量为49g。试计算该氢氧化钠溶液中溶质的质量分数。
学习化学开启了我们认识物质之旅。某实验小组的同学对氢氧化钠的性质及应用进行了如下的探究。
[探究一]溶解过程中的能量变化
如图所示,同学们设计了不同的实验方案进行探究:

(1)实验一中的硝酸铵溶解后,溶液温度 (填"升高"、"降低"或"不变")。
(2)实验二所加试剂及用量如图,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到U形管的液面左低右高,由此小明得出"氢氧化钠溶于水时放出热量"的结论,你是否同意小明的结论并写出你的理由 。
[探究二]氢氧化钠的化学性质
如图所示,同学们用氢氧化钠溶液进行了下列实验,请分析并回答下列问题:

(1)A试管中观察到的现象是 。
(2)B试管中发生反应的化学方程式: 。
(3)C、D试管中均无明显现象。
①为了证明D中已发生化学反应,向该试管中再加入足量的 ,观察到有气泡产生。
②为了证明氢氧化钠溶液和稀盐酸能发生化学反应,同学们设计并进行了如下实验:(所用稀盐酸经估算确保过量)

整个实验过程中无明显现象,证明氢氧化钠溶液和稀盐酸能发生化学反应。请写出步骤Ⅱ中所加试剂 。
[探究三]氢氧化钠的应用
(1)实验室中的应用
实验室中能用氢氧化钠溶液吸收的气体是 (填字母)。
a.二氧化碳
b.水蒸气
c.氯化氢
d.氧气
吸收上述所选气体,一般不用氢氧化钙溶液,主要是因为氢氧化钠和氢氧化钙的 不同。
(2)工业中的应用
氢氧化钠常用于制造人造丝、造纸、炼油、纺织、印染与橡胶工业。某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸4.9t(H 2SO 4的质量分数为20%),可以处理的废水质量是 t。
结合化学方程式中的数据分析:若将等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后,请判断溶液中一定含有的溶质,并简述你的判断理由: 。
取一定量的硫酸铵固体于烧杯中,加入100g氢氧化钠溶液,加热,恰好完全反应。反应后将溶液蒸干,得到7.1g固体。该反应的化学方程式为:(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑.请计算:
(1)生成氨气的质量。
(2)氢氧化钠溶液中溶质的质量分数。