某纯碱样品中含有少量的氯化钠,某化学兴趣小组欲测定其中碳酸钠的质量分数。他们称取6.0g样品放入锥形瓶中,加入稀硫酸直到不再产生气体为止,反应中生成气体的质量与加入稀硫酸的质量关系如图所示:
计算:
(1)反应生成的二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数(写出计算过程,计算结果精确到0.1%)。
(反应的化学方程式为:Na2CO3+H2SO4═Na2SO4+CO2↑+H2O)

下列图象与对应的操作过程相符的是( )
A. 向一定量的氯化钙溶液中通入二氧化碳至过量
向一定量的氯化钙溶液中通入二氧化碳至过量
B.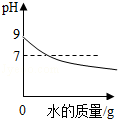 向pH=9的氨水中不断加水稀释
向pH=9的氨水中不断加水稀释
C.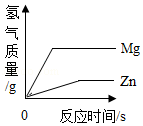 将等质量的镁片和锌片分别加入足量且溶质的质量分数相同的稀硫酸中
将等质量的镁片和锌片分别加入足量且溶质的质量分数相同的稀硫酸中
D. 用两份溶液质量和溶质的质量分数均相等的过氧化氢溶液制取氧气
用两份溶液质量和溶质的质量分数均相等的过氧化氢溶液制取氧气
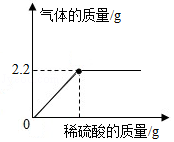
某纯碱样品中含有少量的氯化钠,某化学兴趣小组欲测定其中碳酸钠的质量分数。他们称取6.0g样品放入锥形瓶中,加入稀硫酸直到不再产生气体为止,反应中生成气体的质量与加入稀硫酸的质量关系如图所示:
计算:
(1)反应生成的二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数(写出计算过程,计算结果精确到0.1%)。
(反应的化学方程式为:Na2CO3+H2SO4═Na2SO4+CO2↑+H2O)
某袋装食品的脱氧剂由活性炭、铁粉和食盐混合而成,三者质量比为2:2:1.现用该脱氧剂进行实验,回答下列问题:
(1)将该脱氧剂加入盐酸中,发生反应的化学方程式为 。
(2)打开失效的脱氧剂小袋,发现里面出现了红褐色物质,该物质的主要成分是 (填化学式)。5.0g未经使用的该脱氧剂最多能够吸收氧气 g。
(3)用电子秤称取7.20g完全失效后的脱氧剂放入烧杯中,加入足量稀硝酸,充分溶解后过滤,滤渣为黑色粉末。向所得滤液中加入足量AgNO3溶液,充分反应产生的沉淀质量为2.87g。列式计算该失效脱氧剂中NaCl的质量分数(计算结果精确到0.1%)。
实验室为了测定过氧化氢溶液的质量分数,称取85.00g H2O2溶液和2.00g MnO2混合放入质量为50.00g的烧杯中,用电子天平称得烧杯的总质量随时间变化如表所示:
时间/S |
15 |
30 |
45 |
60 |
75 |
90 |
烧杯总质量/g |
136.5 |
136.1 |
135.70 |
135.50 |
135.40 |
135.40 |
(1)产生O2的质量为 g。
(2)过氧化氢溶液中溶质的质量分数为?(写出计算过程)
菱镁矿中主要含MgCO3、FeCO3和SiO2.以菱镁矿为原料制取镁的工艺流程如图。
回答下列问题:
(1)菱镁矿属于 (选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是 。
(3)写出菱镁矿中MgCO3与稀HCl反应的化学方程式 。
(4)溶液b→溶液c反应的化学方程式为:4FeCl2+ +4HCl=4FeCl3+2H2O(补充完方程式)
(5)溶液c调pH使Fe3+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8﹣ 。
已知:物质沉淀的pH见下表:
物质 |
Mg(OH)2 |
Fe(OH)3 |
开始沉淀的pH |
8.9 |
1.5 |
完全沉淀的pH |
10.9 |
2.8 |
(6)结合流程中的数据计算。
①菱铁矿中镁元素的质量分数为 (不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量(写出计算过程)。
某炼钢厂每天需消耗5000t含Fe2O376%的赤铁矿,该厂理论上可日产含Fe 98%的生铁的质量是多少?
数据处理能及时获得更多的信息。下列图示中,不能正确反映化学原理及实验操作规范的是( )
A.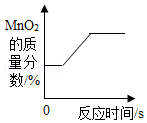 加热一定质量的KClO3和MnO2的混合物
加热一定质量的KClO3和MnO2的混合物
B.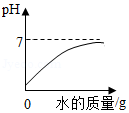 稀释浓硫酸
稀释浓硫酸
C.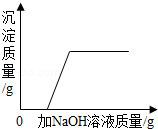 向pH=4的CuSO4溶液中滴加NaOH溶液
向pH=4的CuSO4溶液中滴加NaOH溶液
D.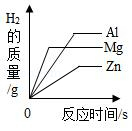 向足量相同质量分数的稀硫酸中分别加入等质量Zn粉、Al粉、Mg粉
向足量相同质量分数的稀硫酸中分别加入等质量Zn粉、Al粉、Mg粉
实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将140g氯化钙溶液分四次加入,充分反应,
注:发生反应的化学方程式为:CaCl2+Na2CO3 ═CaCO3↓+2NaCl
四次测量所得数据如表所示:
次数 |
累计加入氯化钙溶液的质量/g |
烧杯中溶液的总质量/g |
一 |
40 |
135 |
二 |
80 |
170 |
三 |
120 |
205 |
四 |
140 |
225 |
(1)恰好完全反应时,生成沉淀的总质量为 g。
(2)第四次测量时,所得溶液中的溶质有 (填化学式)
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)
将20g镁、铁的金属混合物加入到一定质量的稀硫酸中,恰好完全反应后,经测定溶液质量增加了19g,将反应后的溶液蒸干,得到固体的质量为( )
A.39gB.60gC.68gD.73g
向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是( )
A.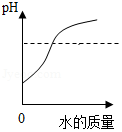 B.
B.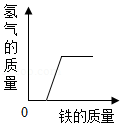
C.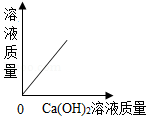 D.
D.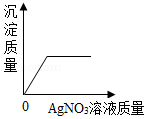
某兴趣小组同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,测得实验数据如下表所示:
| |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
| 氢氧化钠溶液的质量/g |
20 |
20 |
20 |
20 |
20 |
| 沉淀质量/g |
4.9 |
9.8 |
m |
19.6 |
19.6 |
(1)表格中m的值为多少。
(2)计算恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程)
73g盐酸与足量锌粒反应,生成的气体在标准状况下的体积为4.48L.(在标准状况下,氢气的密度为0.0899g/L)
(1)生成的气体的质量为 (结果保留1位小数)。
(2)计算盐酸中溶质的质量分数(写出计算过程)。
中国北斗,星耀全球﹣﹣6月23日,由氢氧发动机提供动力的长征三号乙火箭成功将北斗三号最好一颗全球组网卫星送上太空。已知火箭将卫星送入预定轨道需要44t液氢(H2),则使液氢完全燃烧需提供液氧(O2)多少吨?