某化验室用20%的氢氧化钠溶液洗涤一定量工业产品中残余的H2SO4(工业产品及其他杂质都不与氢氧化钠溶液反应),当恰好完全反应时,共消耗氢氧化钠溶液80g,求产品中残余的H2SO4质量和生成硫酸钠的质量。
某学生将二氧化锰粉末制成颗粒。放入100g溶质的质量分数为10%的过氧化氢溶液中。一段时间后,取出二氧化锰,共收集到3.2g氧气。
(1)利用化学方程式计算,参加反应的过氧化氢的质量。
(2)向反应后的溶液中加入30%的过氧化氢溶液,使其质量分数重新达到10%备用。计算最终可得到10%的过氧化氢溶液的质量。
实验室用34g过氧化氢溶液和2g二氧化锰混合制取氧气。完全反应后剩余物质总质量为35.2g。请计算:
(1)生成氧气的质量为 g。
(2)求所用过氧化氢溶液溶质的质量分数。(根据化学方程式进行计算,写出计算过程)
称取5g含杂质的氢氧化钙固体样品放入烧杯中,向烧杯中加入50g溶质的质量分数为7.3%的稀盐酸(假设杂质不与稀盐酸反应),二者恰好完全反应。请计算:固体样品中氢氧化钙的质量分数。
赤铁矿石的主要成分为氧化铁。将10g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,再加入92g稀硫酸,恰好完全反应,过滤,得到滤液和2g滤渣。请计算:
(1)赤铁矿石样品中氧化铁的质量分数。
(2)反应后所得溶液中溶质质量分数。
84消毒液的有效成分是次氯酸钠(NaClO),次氯酸钠工业制法的反应原理是:Cl 2+2NaOH═NaClO+NaCl+H 2O.某同学将Cl 2通入185.8g NaOH溶液中(NaOH过量),充分反应后得到混合溶液200g。计算:(计算结果精确到0.1%)
(1)参加反应的氯气质量是 g。
(2)混合溶液中次氯酸钠的质量分数。
(3)84消毒液中起消毒作用的是次氯酸钠中的氯元素。已知某品牌84消毒液中起消毒作用的氯元素质量分数为6%,计算该84消毒液中次氯酸钠的质量分数。
过氧化氢溶液俗称双氧水,是一种常见消毒剂。实验员用以下方法制取了少量过氧化氢溶液,在低温下,向56.4g某浓度的稀硫酸中逐渐加入一定量的过氧化钡(BaO 2),发生的化学反应为BaO 2+H 2SO 4═BaSO 4↓+H 2O 2,当恰好完全反应时生成23.3g沉淀。计算:
解:(1)设加入BaO 2的质量为X,生成的H 2O 2质量为Y,需要加入水的质量为Z
BaO 2 +H 2SO 4 ═BaSO 4↓+H 2O 2
169 233 34
X 23.3g Y
X=16.9g;Y=3.4g
(2)反应后所得溶液中溶质质量分数为: 6.8%;
(3)设需加入水的质量为Z
(16.9g+56.4g﹣23.3g)×6.8%=(16.9g+56.4g﹣23.3g+Z)×3%
Z=63.3g
答:(1)加入BaO 2的质量是16.9g;
(2)反应后所得溶液中溶质质量分数6.8%;
(3)需加入水的质量63.3g。
今后学习常见物质时,会从“价”和“类”两个方面进行学习。如图表示铁元素的常见化合价与含铁物质类别的关系。
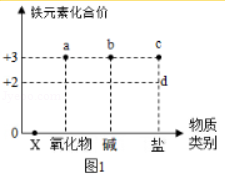
(1)X的物质类别是 。
(2)铁和稀硫酸反应生成的含铁化合物属于如图1中的 (填序号)。
(3)某同学想用物质a制取物质b,设计了如图2实验步骤:
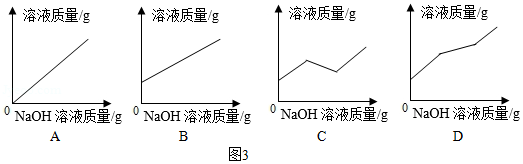
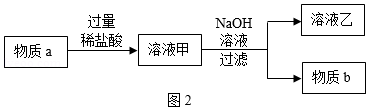 物质a与稀盐酸反应的化学反应方程式为 。溶液乙中的溶质一定有 。如果向盛有溶液甲的烧杯中滴加NaOH溶液至过量,图3中图象能正确表示烧杯中溶液质量变化的是 (填序号)。
物质a与稀盐酸反应的化学反应方程式为 。溶液乙中的溶质一定有 。如果向盛有溶液甲的烧杯中滴加NaOH溶液至过量,图3中图象能正确表示烧杯中溶液质量变化的是 (填序号)。
在100g的某盐酸中加入硝酸银溶液,反应为AgNO3+HCl═HNO3+AgCl↓,至恰好完全反应,经过滤、洗涤、干燥、称量得到质量为28.7g的AgCl沉淀,求盐酸的溶质质量分数。
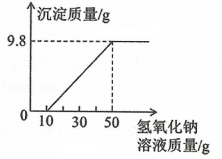
向盛有100g稀硫酸和硫酸铜混合溶液的烧杯中滴加氢氧化钠溶液至过量,过滤、烘干并称量沉淀的质量。该反应过程如图所示。请按要求回答问题:
(1)滤液中的溶质是 (填化学式)。
(2)计算原混合溶液中硫酸铜的质量。
(3)氢氧化钠溶液的溶质质量分数。
如图图象分别对应四个变化过程,不能正确反映对应变化关系的是( )
A. 加热一定质量的氯酸钾和二氧化锰的混合物
加热一定质量的氯酸钾和二氧化锰的混合物
B. 气体物质的溶解度受温度影响的变化
气体物质的溶解度受温度影响的变化
C. 中和反应是放热反应,向稀KOH溶液中加入稀盐酸
中和反应是放热反应,向稀KOH溶液中加入稀盐酸
D. 向等质量的铝粉和锌粉中分别滴加足量的相同浓度的稀盐酸
向等质量的铝粉和锌粉中分别滴加足量的相同浓度的稀盐酸
某工厂利用废硫酸溶液与铁反应制取硫酸亚铁。49t废硫酸溶液中的硫酸与5.6t铁恰好完全反应。求:
(1)废硫酸溶液中溶质的质量分数。
(2)理论上生产的硫酸亚铁的质量。[温馨提示:Fe+H2SO4═FeSO4+H2↑]
如图图象能正确表示对应叙述的有( )
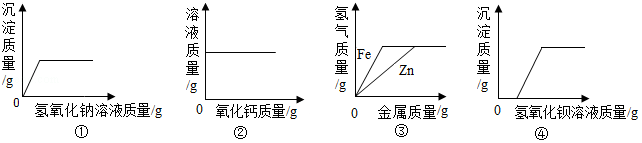
①向一定量硫酸和硫酸铜的混合溶液中逐滴加入氢氧化钠溶液
②向一定量的饱和氢氧化钙溶液中加入氧化钙
③向等质量、等质量分数的稀盐酸中分别加入锌和铁
④向一定量的盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液
A.1个B.2个C.3个D.4个
工业上制作电路的一种反应原理是Cu+2HCl+H2O2 CuCl2+2H2O.若反应了6.4g Cu,计算需要10%的H2O2溶液的质量。