“黄铜”是铜锌合金,具有较好机械性能,比纯铜耐腐蚀,街头许多“金色”饰品就是用它来制作的.现取20.0 g某种黄铜投入100 g某稀硫酸中,恰好完全反应后剩余的溶液和残余固体总质量为119.8 g.请计算:
(1)产生氢气的质量为____g.
(2)这种黄铜中铜的质量分数是多少?
(3)剩余溶液中溶质的质量分数是多少?(结果精确到0.1%)
氢化钙(CaH2)是一种重要的制氢剂,与水接触时发生如下反应:
CaH2+2H2O = Ca(OH) 2+2H2↑。若要制得2 g氢气,需CaH2的质量为多少?
环保部门对某工厂的废水进行抽样分析,结果表明废水中含少量硫酸。取一定量废水用质量分数为2%的氢氧化钠溶液中和(已知废水中的其它成分不与氢氧化钠反应),至pH = 7时,消耗氢氧化钠溶液的质量为40g,同时测得反应后溶液质量为138g。请计算该工厂排放的废水中硫酸的质量分数。
甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0 g样品溶于一定量的水中得到25.0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表:
| |
甲 |
乙 |
丙 |
| 加入氢氧化钠溶液质量 (g) |
20.0 |
40.0 |
60.0 |
| 反应得到沉淀的质量 (g) |
1.45 |
2.9 |
2.9 |
试回答下列问题:
(1)上述实验中,__________同学所用的氢氧化钠溶液一定过量。
(2)求原固体样品中氯化镁的质量分数。
(3)计算乙同学实验后所得溶液中的溶质的质量分数。(计算结果保留小数点后一位)
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
| 样品 |
第1份 |
第2份 |
第3份 |
第4份 |
| 取样品质量(g) |
50.0 |
50.0 |
50.0 |
50.0 |
| 取稀硫酸质量(g) |
40.0 |
80.0 |
120.0 |
160.0 |
| 产生气体质量(g) |
0.4 |
0.8 |
1.0 |
1.0 |
试计算: ⑴经分析,在第1份样品测得的数据中, (填物质)完全反应了。
⑴经分析,在第1份样品测得的数据中, (填物质)完全反应了。 ⑵列式计算黄铜屑样品中的锌的质量分数和所用稀硫酸中溶质的质量分数。
⑵列式计算黄铜屑样品中的锌的质量分数和所用稀硫酸中溶质的质量分数。
某化学研究小组对当地的石灰石样品进行了研究。称取石灰石样品16g,把80g稀盐酸分四次加入样品中,测得实验数据见下表(假设石灰石样品中杂质不溶于水、不与盐酸反应,二氧化碳不溶解)。
| 实验序号 |
加入稀盐酸的质量/g |
剩余固体物质的质量/g |
| 第1次 |
20 |
11 |
| 第2次 |
20 |
6 |
| 第3次 |
20 |
3.2 |
| 第4次 |
20 |
m |
(1)第4次剩余固体物质的质量m= g
(2)石灰石样品中CaCO3的质量分数为 。
(3)计算稀盐酸的溶质质量分数。
取盐酸与氯化钙的混合溶液11.88kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液pH与加入的碳酸钠溶液的质量关系如右图所示
(1)通过右图可知,当碳酸钠溶液质量加到 kg时,溶液恰好完全反应 (盐酸与氯化钙的混合溶液完全转化成氯化钠溶液)。
(2) 溶液恰好完全反应时所得溶液中所含溶质氯化钠质量?
为测定某NaCl、Na2CO3固体混合物的组成,小明同学取16g该混合物放入烧杯中,分五次加入稀盐酸(每次加入稀盐酸的质量为25g),待反应完全后,得到下面的质量关系:
请分析以上数据后计算:
⑴原固体混合物中Na2CO3的质量。
⑵当加入稀盐酸至固体混合物恰好完全反应时,所得溶液的溶质质量分数。(计算结果精确到0.1)
2010年全国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与水反应):
| |
烧杯① |
烧杯② |
烧杯③ |
烧杯④ |
烧杯⑤ |
| 加入样品的质量/g |
10 |
10 |
10 |
10 |
10 |
| 加入稀盐酸的质量/g |
10 |
20 |
30 |
40 |
50 |
| 充分反应后生成气体的质量/g |
0.88 |
1.76 |
X |
3.52 |
3.52 |
(1)表中X的值为 ▲ ;
(2)求样品中碳酸钙的质量分数;
中国核潜艇技木世界领先。在潜艇中常用过氧化钠吸收二氧化碳并产生氧气来维持艇内空气成分平衡,其反应的化学方程式为:2Na202+CO2=2Na2CO3+O2.现有
质量分数为78%的过氧化钠100g.与足量的二氧化碳反应,可生成氧气多少克?(杂
质不参加反应)
Ag-Zn合金可用于工艺品的制作。某化学兴趣小组的同学为了测定某银锌合金的组成,取一定量样品于烧杯中,向其中分5次加入相同质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量均为20g,剩余固体的质量记录于下表:
| 实验次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
| 反应后剩余固体的质量(g) |
17.4 |
14.8 |
12.2 |
10.8 |
10.8 |
试回答下列问题(填写数据一定要有单位!):
①该样品中银的物质的量为 (34) ;实验用样品的总质量是 (35) 。
②有同学认为没有必要进行第五次的实验,你的理由是 (36) ;
③计算所用稀硫酸溶质的质量分数,除需用到稀硫酸溶液的质量为20g,还需要用到表格中的数据有(37) (多选不给分!)。
工业上,高温煅烧石灰石(CaCO3)可制得生石灰( CaO)和二氧化碳( CO2 )。如果要制取10吨氧化钙,需要碳酸钙多少吨?(写出计算过程,结果保留一位小数)。
为测定铜锌合金的组成,某化学小组的同学将200克稀硫酸分四次加入到40克合金中,得出如下数据和图像。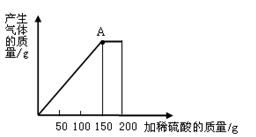
请计算:
(1)a的数值为 。
(2)合金中铜的质量分数为 。
(3)实验所用稀硫酸的质量分数是 。
超氧化钾能与二氧化碳反应生成氧气(4KO2+2CO2=2K2CO3+3O2),在医院、矿井、潜水、高空飞行中用作供养剂。要得到320克氧气,参加反应的超氧化钾的质量是多少?
(6分)某炼铁厂用含Fe2O3的铁矿石冶炼10 t含杂质2%的生铁,至少需要一氧化碳的质量是多少?标准状况下,一氧化碳的体积是多少?(标准状况下,一氧化碳的密度为1.25 kg/m3)