用"侯氏联合制碱法"制取的纯碱(
)中常含有少量的氯化钠。化学实验小组同学为测定某厂生产的纯碱中碳酸钠的含量,称取12
样品放入烧杯中并滴加稀盐酸,当盐酸滴加至73
时,气泡不再冒出,此时称得烧杯内溶液的总质量为80.6
。
试计算:
⑴产生二氧化碳气体的质量是
。
⑵该厂生产的纯碱中碳酸钠的质量分数。(计算结果精确到0.1%)
一瓶氢氧化钠固体,因不慎敞口放置了一段时间,已经部分变质。化学课外兴趣小组的同学决定测定该瓶试剂变质的程度,他们在知识回顾的基础上,依次进行了如下的实验操作:
知识回顾:氢氧化钠必须密封保存;氢氧化钠与二氧化碳反应生成Na2CO3和H2O;CaCO3不溶于水。
第一步:取该瓶中的试剂20g加水配制成溶液;
第二步:向上述溶液中加入足量的澄清石灰水;
第三步:过滤、干燥、称量,生成沉淀为5g。
⑴若该瓶试剂中的Na2CO3的质量分数为A,则氢氧化钠的质量分数 (填大于、等于或小于),原因是 。
⑵计算该20g试剂中含有杂质Na2CO3的质量分数(结果精确到0.1%)。
(6分)实验室有一瓶氯化钠和碳酸钠的混合物,某同学为了确定它的组成做了如下实验:首先取l 6 g混合物放入烧杯中,然后向烧杯中滴加稀盐酸,直到不再产生气泡为止,共加入稀盐酸159.4 g,测得反应后剩余物质的总质量为171 g。求:
(1)此瓶混合物中所含碳酸钠的质量分数。
(2)反应后所得溶液中溶质的质量分数。
某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,取该溶液20g,加入二氧化锰0.5g,完全反应后,称得烧杯内剩余物质的总质量为19.7g。请回答下列问题:
(1)上述过程中生成氧气质量是。
(2)计算该过氧化氢溶液中溶质的质量分数。
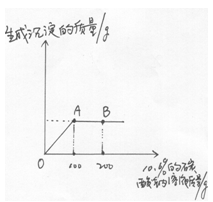
用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠。为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品12.4g,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7(填>、=、<)。
(2)从坐标上C点的数值为 g。
(3)求该纯碱样品中碳酸钠的质量分数。(计算结果保留一位小数)
将104g由氯化钠和氯化钡
组成的固体混合物溶解于足量水中,向所得溶液中滴加10.6%的碳酸钠溶液,所加碳酸钠溶液的质量与生成沉淀质量关系见右图
①图中表示恰好完全反应的点是,此时溶液中的溶质为。(写化学式)
②求生成沉淀的质量。
③求原混合物中氯化钠的质量分数。
已部分变质的Ca(OH)2固体试样10g,与足量稀盐酸反应,产生2.2gCO2,则该固体试样中Ca(OH)2的质量分数为
| A.30% | B.40% | C.50% | D.60% |
某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
| 反应时间/min |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
3.5 |
| 剩余固体质量/g |
2.55 |
2.25 |
2.10 |
2.04 |
M |
2.04 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为_______________g;
(2)根据表中数据分析M的值是 _g
(3)原混合物中氯酸钾的质量分数是多少?(请写出计算过程)
将一定质量的碳酸钠粉末溶于
克水中配制成溶液,取一半该溶液,向其中加入
的盐酸若干克,恰好反应完全,放出气体的质量为
克。试计算:
(1)碳酸钠溶液的总质量;
(2)反应后所得溶液中溶质的质量分数。
已知CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl。将15 g CaCl2溶液逐滴加入到20 g Na2CO3溶液中,并测得生成沉淀的质量与滴入CaCl2溶液的质量关系如右图所示。若将反应后的物质过滤,蒸干滤液后得到固体的质量是多少。
工业上用电解法冶炼铝的化学方程为2Al2O3 4Al+3O2。要电解得到54吨铝,需要多少吨氧化铝?
4Al+3O2。要电解得到54吨铝,需要多少吨氧化铝?
取某碳酸钠样品50g(含氯化钠和13%的不溶性杂质,杂质不参加化学反应),放入质量为200g的烧杯中,加137.7g水充分溶解,再向烧杯中加入300g稀盐酸恰好完全反应,测得反应后烧杯与烧杯内物质的总质量为674.5g。求所得溶液中溶质的质量分数。
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如右图所示。试计算:
(1)样品中铜的质量分数;
(2)反应所消耗的硫酸溶液质量;
(3)反应后所得溶液中溶质的质量分数。
为测定混有少量氯化钠的碳酸钠(Na2CO3)固体中碳酸钠的质量分数,向盛有12g该混合物的烧杯中加入过量稀盐酸至碳酸钠完全反应。
发生反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O
反应过程用精密仪器测得烧杯和药品的质量与反应时间的数据记录如下:
| 反应时间 |
t0 |
t1 |
t2 |
t3 |
t4 |
t5 |
| 烧杯和药品质量/g |
210.0 |
206.7 |
205.9 |
205.6 |
205.6 |
205.6 |
(1)则完全反应后,生成二氧化碳的质量。
(2)请计算混合物中碳酸钠的质量分数(精确到0.1%)。
(3)假如称量准确,通过计算得到的碳酸钠的质量分数比实际数值偏小,其原因是 ▲ 。