某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入92.0g稀硫酸,恰好完全反应后,过滤,所得滤液质量为100.0g。
(1)所取样品中铜的质量为 。
(2)从反应后所得的100.0g滤液中取出10.0g溶液,将其稀释为10%的溶液,需要加水多少克?
钙是人体中的常量元素,因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片。某补钙药剂说明书的部分信息如图1所示。现将100g盐酸分成五等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如图2.请根据有关信息回答问题。
| 实验次数 |
第一次 |
第三次 |
第四次 |
| 加入盐酸的质量(g) |
20 |
20 |
20 |
| 剩余固体的质量(g) |
35 |
a |
20 |
(1)该品牌补钙药剂中CaCO 3的质量分数是 ,a的数值为 。
(2)该盐酸中溶质的质量分数是多少?(写出计算过程,计算结果精确至0.1%)
向10g大理石样品(杂质不溶于水,也不与盐酸反应)分两次加入一定溶质质量分数的稀盐酸,充分反应后烧杯内物质总质量变化如图所示。
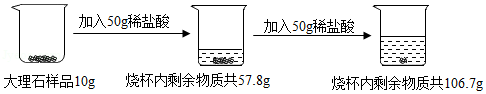
请计算:
(1)该大理石样品中碳酸钙的质量分数是 ;
(2)计算所用稀盐酸的溶质质量分数。
工业上电解氧化铝制取金属铝的化学方程式2Al 2O 3  4Al+3O 2↑ 电解20t氧化铝最多可生产多少吨铝?(写出必要的计算过程,计算结果精确到0.1t)
4Al+3O 2↑ 电解20t氧化铝最多可生产多少吨铝?(写出必要的计算过程,计算结果精确到0.1t)
胃酸过多的病人,通常需每天服用含碳酸氢钠的药物9片,能消耗胃酸中的氯化氢2.19g.某病人有胃溃疡症状,这种药物会加剧胃部疼痛.医生建议改用含氢氧化铝(其他成分不与胃酸反应)的胃舒平,药物标签如图.请计算中和相同质量的胃酸,每天需要服用胃舒平多少片?

为测定一标签破损(如图)的钙片中碳酸钙的含量,某同学做如图实验:取10片钙片,放入干燥、洁净的烧杯中,然后逐滴滴加稀盐酸,当加入50g盐酸后,恰好完全反应,此时称量烧杯内剩余物质的总质量为65.6g(钙片中其他成分不和稀盐酸反应,反应中产生的气体全部放出).
(1)反应中生成 g二氧化碳,该钙片中碳酸钙的质量分数为 ;
(2)试计算所用稀盐酸中HCl的质量分数.

某化学课外活动小组测定长期放置的铁粉中铁单质的百分含量.他们准确称量两份质量各为10.0g的铁粉样品,分别进行如下操作:
(1)如图所示甲同学记录天平砝码和游码的数据为54.0g.将气球中的10.0g铁粉样品加入到盛有过量的稀硫酸的锥形瓶中,反应停止后,天平是否平衡(不考虑空气浮力) (填"是"或"否");要想获取实验的相关数据,后面必须的操作是 (假设气球不破裂且能恢复原状).
| A. |
打开弹簧夹a放出气体 |
B. |
取下砝码 |
| C. |
向右拨动游码至天平平衡 |
D. |
向左拨动游码至天平平衡 |
(2)乙同学把10.0g铁粉样品加入到足量的硫酸铜溶液中,充分反应后过滤、洗涤、干燥、称量,得到固体10.8g,计算该样品中铁单质的百分含量.(写出计算过程)

某校化学兴趣小组在参加社会实践活动时,环保组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保组的同学进行了以下实验:取废水300g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,请分析计算:
(1)实验中生成氢氧化铜的质量为 g;
(2)300g该废水中硫酸铜的质量;
(3)该废水中硫酸的溶质质量分数。(计算结果精确到0.1%)

向53g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为5%的稀盐酸,生成二氧化碳的质量随加入盐酸质量的变化关系如图所示。(不考虑CO 2的溶解)
已知:
OB段反应的化学方程式为Na 2CO 3+HCl═NaCl+NaHCO 3
BD段(不含B点)反应的化学方程式为NaH CO 3+HCl═NaCl+H 2O+CO 2↑
请回答:
(1)53g质量分数为10%的碳酸钠溶液中溶质质量为 g。
(2)A点对应溶液中溶质有 (填化学式)。
(3)B点横坐标为 (计算结果保留1位小数,下同)
(4)假设C点横坐标为54.75,计算C点对应的二氧化碳质量。(写出计算过程)

某化学小组为了探究一瓶久置在空气中的氢氧化钠样品(不含有水分)的变质程度,进行了如下实验:取该氢氧化钠样品13.3g于烧杯中,加水完全溶解,然后向烧杯中逐渐加入一定溶质质量分数的氯化钡溶液,反应过程中对加入氯化钡溶液的质量与烧杯中产生沉淀的质量进行了记录,部分数据见表.
| 加入氯化钡溶液的质量/g |
20 |
40 |
80 |
| 生成沉淀的质量/g |
1.97 |
3.94 |
5.91 |
试分析计算:
(1)13.3g氢氧化钠样品中碳酸钠的质量.
(2)13.3g氢氧化钠样品变质前的质量.(已知:Ba的相对原子质量为137)
小苏打是发酵粉的主要成分之一,可用于制作发面食品。一化学兴趣小组对某小苏打样品中各成分的含量做了如下测定:将一定质量的该样品(已知杂质只含NaCl)加水全部溶解后,得到104.4g溶液,向该溶液中逐渐加入稀盐酸,产生的气体与加入稀盐酸的质量关系如图所示。试计算:
(1)m的值为 。
(2)当恰好完全反应时,所得溶液的溶质质量分数为3%,求原小苏打样品中NaHCO 3与NaCl的质量比 。

某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下

请回答下列问题:
(1)滤液可作化肥使用,你认为它属于 肥;
(2)该同学制得氧气的质量 g;
(3)计算滤液中溶质质量分数。
某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下

请回答下列问题:
(1)滤液可作化肥使用,你认为它属于 肥;
(2)该同学制得氧气的质量 g;
(3)计算滤液中溶质质量分数。
如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到2g气体时,停止实验(所需相对原子质量:H﹣1、O﹣16).计算:
(1)停止实验时,电解消耗水的质量是多少?
(2)停止实验后,剩余溶液中Na2SO4的质量分数是多少?

海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水.粗盐中常含有多种杂质,必须对其分离和提纯,才能用于生产和生活;卤水经常用作工业制镁的原料.
(1)实验室除去粗盐中不溶性杂质的实验步骤为:溶解、过滤、蒸发结晶.在三步中都要用到的一种玻璃仪器是 .
(2)若要除去食盐固体中含有的少量CaCl2杂质,得到较为纯净的食盐晶体.请简述实验操作步骤: .
(3)在一烧杯中盛有Mg(OH)2和MgCl2的混合粉末6g,向其中加入20g水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸.烧杯中溶液的溶液的总质量与加入稀盐酸的质量关系如图所示,请回答下列问题:
①当滴入稀盐酸30g时(即图中A点时),烧杯内溶液中的溶质是 (填写化学式).
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求此温度时所得不饱和溶液中溶质的质量(计算结果精确至0.1g).
