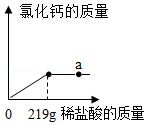
实验室模拟高温煅烧石灰石的方法制取二氧化碳,取35g石灰石样品(假设杂质受热不分解且不与酸反应),煅烧一段时间恢复到室温,测得生成11g二氧化碳。向剩余固体中逐滴加入某盐酸至不再反应为止,又生成2.2g二氧化碳,加入盐酸的质量与生成的氯化钙质量关系如图:
(1)石灰石样品的质量分数是 (结果保留一位小数,下同);
(2)a点溶液的pH 7(填“<”“>”或“=”);
(3)求所加盐酸的溶质质量分数(写出计算过程)。
实验测成分
小伟同学在实验室中对某品牌除锈剂的有效成分及含量进行探究。
(1)定性检验:
小伟同学使用 、 分别与除锈剂反应,通过实验现象确定除锈剂的主要成分是硫酸。
(2)定量测定:
小伟同学利用碳酸钠溶液测定除锈剂中硫酸的质量分数,实验过程如下:
①向烧杯中加入50g除锈剂;
②向除锈剂中滴加碳酸钠溶液,边滴加边搅拌,至不再有气泡放出,共消耗碳酸钠溶液40g;
③反应后,烧杯中剩余物质的总质量为87.8g(除锈剂中其他成分不与碳酸钠反应,反应中产生的气体全部逸出)
根据上述实验数据计算除锈剂中硫酸的质量分数。
长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢中CaCO3的含量,将6g水垢粉碎放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:
反应时间/min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
烧杯内所盛物 质的总质量/g |
46.0 |
45.2 |
44.8 |
45.1 |
44.1 |
43.9 |
43.8 |
43.8 |
43.8 |
试计算:
(1)表中有一数据是不合理的,该数据的测得时间是第 min;
(2)水垢中CaCO3的质量分数(计算结果精确至0.1%)。
某化学拓展课堂的主题是:探秘氯化钠样品。
主题Ⅰ:探究氯化钠样品中杂质的成分
已知所提供的氯化钠样品中,可能含有硫酸钠、氯化镁、氯化钙中的一种或几种杂质。甲同学的实验探究过程记录如下: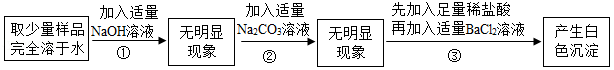
根据以上实验信息,甲同学得出结论:此氯化钠样品中含有的杂质是硫酸钠。
[实验分析]
(1)步骤①中加入适量NaOH溶液的目的是 。
(2)乙同学认为步骤③中不需要加入足量稀盐酸,你是否同意他的观点? (选填“同意”或“不同意”),请说明原因 。
主题Ⅱ:测定氯化钠样品中氯化钠的质量分数
确定了氯化钠样品中杂质的成分后,甲同学对样品中氯化钠的质量分数进行测定。称取20.0g氯化钠样品于烧杯中,加足量的水充分溶解,再向其中加入氯化钡溶液至不再产生沉淀为止,沉淀经过滤、洗涤、干燥后称量,其质量为2.33g。请计算该样品中氯化钠的质量分数。(写出计算步骤,计算结果精确到0.1%)
某纯碱样品中含有少量氯化钠杂质。称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。试回答:
(1)生成CO2的质量 。
(2)22.8g样品中氯化钠的质量为 。
(3)计算所得溶液中溶质的质量分数。(写岀解题过程,计算结果精确到0.1%)

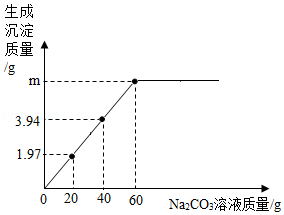
向200g NaCl和BaCl2的混合溶液中加入Na2CO3溶液。反应过程中滴加Na2CO3溶液的质量与生成沉淀的质量关系如图所示。请计算:
(1)m的值是 g;
(2)原混合溶液中BaCl2的质量分数是多少?
向200g NaCl和BaCl2的混合溶液中加入Na2CO3溶液。反应过程中滴加Na2CO3溶液的质量与生成沉淀的质量关系如图所示。请计算:
(1)m的值是 g;
(2)原混合溶液中BaCl2的质量分数是多少?

课外活动小组为测定某未知稀硫酸的质量分数,进行了下面实验:
①取10g稀硫酸于烧杯中,逐滴滴加BaCl2溶液,至不再产生白色沉淀止,经过滤、洗涤,干燥后,称得沉淀物的质量为4.71g
②为保障测定结果的精确性,按实验①操作又连续进行了四次相同的实验。几次实验所得数据见下表:
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
|
固体质量/g |
4.71 |
4.63 |
4.64 |
4.66 |
4.66 |
分析实验与表中数据后,回答:
(1)第一次实验测得数据明显偏高,可能的原因是 ;
(2)五次测定结果的平均值是 ;
(3)请利用(2)中数据计算:未知稀硫酸的质量分数是 。(不要求计算过程,计算结果精确到0.01)
镁元素广泛应用于火箭、导弹和飞机制造业,被称为“国防元素”。如图1所示为制取单质镁的转化过程,试回答下列问题:
如图转化过程中发生的化学反应主要有:

MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl═MgCl2+2H2O,MgCl2 Mg+Cl2↑
(1)在过程①中,所加石灰乳的主要成分是 (填写化学式)。
(2)过程②所发生的反应属于 (填“化合”“分解”“置换”或“复分解”)反应。
(3)下列有关过程③中能量转化的说法,正确的是 (填选项序号)。
A.电能转化为化学能 B.化学能转化为电能 C.潮汐能转化为化学能
(4)海水或卤水中本来就含有氯化镁,还需要过程①②的原因是 (选项序号)。
A.将氯化镁富集提纯 B.生成更多氯化镁 C.使石灰乳和稀盐酸反应
(5)某化学兴趣小组欲测定某氯化镁样品中MgCl2的含量(杂质为NaCl),称取10g该样品将其置于干净的烧杯中,加入适量水,使固体样品完全溶解。向所得溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与滴入NaOH溶液的质量关系如图所示。试回答下列问题:

①当滴入NaOH溶液120g时(即图中B点),烧杯中溶液里含有的溶质为 (写化学式)。
②当滴入10%的NaOH溶液80g时(即图中A点),恰好完全反应,试通过计算,求10g此氯化镁样品中MgCl2的质量。(计算结果精确至0.1g)
铜锌合金又叫黄铜,外观酷似黄金,极易以假乱真。某化学兴趣小组用图I所示装置测定黄铜中锌的含量。将足量的稀硫酸全部加入锥形瓶中,充分反应后天平示数的变化如图Ⅱ所示。请计算:

(1)生成氢气 g。
(2)黄铜样品中锌的质量分数。(写出计算过程)
工业盐酸中通常含少量FeCl3而呈黄色。小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸50g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表,请根据表格和图象完成下列问题:
加入NaOH溶液的质量/g |
25 |
50 |
75 |
100 |
所得溶液的质量/g |
75 |
100 |
125 |
m |
(1)开始没有产生沉淀的原因是 。
(2)求该工业盐酸中HCl的质量分数(写出计算过程)。
(3)m= (结果保留两位小数)。

在进行“实验活动1 氧气的实验室制取与性质”前,化学老师预计本次实验共需要收集45瓶氧气,通过计算得知:这些氧气的总质量约是16g。请计算要想制取足够的氧气,至少需要准备多少克高锰酸钾?
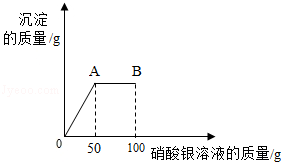
将1.17 g氯化钠固体放入烧杯中,加入51.7g水充分溶解后得到常温下氯化钠的不饱和溶液,再向所得溶液中逐滴滴入100 g一定溶质质量分数的硝酸银溶液。实验过程中生成沉淀的质量与滴入硝酸银溶液的质量关系如图所示:
(1)B点时,溶液中所含硝酸银的质量为 。
(2)A点时,所得溶液中溶质质量分数为多少?(计算结果精确到0.1%)
小苏打的主要成分是碳酸氢钠,其中往往含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌小苏打样品中碳酸氢钠的质量分数。
(1)准确称取9.0g小苏打样品放入烧杯中,逐滴加入质量分数为5%的稀盐酸至恰好不再产生气泡为止,共消耗稀盐酸73.0g,烧杯中没有残留不溶物。计算样品中碳酸氢钠的质量分数。(写出计算过程)
(2)请你设计一个与上述实验原理和操作方法均不相同的实验,测定小苏打样品中碳酸氢钠的质量分数 。