下图是甲、乙两种固体物质的溶解度曲线。下列有关叙述正确的是
| A.0℃时,甲物质的溶解度为40g |
| B.10℃时,甲、乙两种物质的溶解度相等 |
| C.30℃时,甲物质饱和溶液的质量分数为60% |
| D.除去甲物质中少量乙物质可采取蒸发的方法 |
粗盐中含有泥沙等难溶性杂质和氯化镁、氯化钙等可溶性杂质,某学习小组做粗盐的提纯实验。
【提出问题】如何才能将粗盐中的杂质除去,获得精盐?
【实验方案】该小组按以下流程进行实验。
【问题讨论】
(1)实验步骤②③④都需要进行 操作,该操作中玻璃棒的作用是 。
(2)沉淀X是 ,沉淀Y是 。
(3)有同学认为该实验方案不完善,请你说明原因并补充完善: 。
(4)将实验所得的精盐在烧杯中配制成100g 8﹪的氯化钠溶液。经检测,所配溶液溶质质量分数偏小,其可能原因有 (填序号)。
①精盐称量时,仅在左盘垫上了称量纸,而右盘没有垫上称量纸;
②溶解时所用烧杯不干燥;
③所得精盐未完全干燥。
(5)工业上用电解饱和食盐水的方法可制取氢氧化钠,同时还生成两种气体单质。写出此反应的化学方程式 。
甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:

30℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为 ;要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是 ;50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的是 [50℃时,30g乙物质加入到50g水中不断搅拌,所得溶液的质量是 .
质量分数为30%的某溶液蒸发掉10g水后,溶液的质量分数变为40%,则原溶液的质量是
| A.30g | B.40g | C.50g | D.60g |
甲、乙、丙三种固体物质的溶解度曲线如右下图所示,下列叙述中正确的是
| A.将t1℃丙的饱和溶液升温到t2℃,得到丙的不饱和溶液 |
| B.t3℃时,甲、乙两种溶液的溶质质量分数相等 |
| C.t2℃时,丙物质的饱和溶液的溶质质量分数为30% |
| D.t3℃时,30g乙物质加入50g水中,充分溶解后得到75g溶液 |
甲、乙两种固体(无结晶水)的溶解度曲线如图。
①图中a点的含义是( 11 ) ;
②40℃时,50g水中最多溶解( 12 ) g甲;
③正确的说法是( 13 )
| A.20℃时,甲、乙溶液所含溶质质量相等 |
| B.40℃时,将10%的甲溶液降温至20℃,其溶质质量分数减小 |
| C.40℃时,分别向100g水中加入35g甲、乙,所得溶液的溶质质量分数:甲>乙 |
| D.40℃时,甲、乙两杯饱和溶液所含溶质质量相同,则溶液质量的大小关系:甲<乙 |
下图是A、B、C三种物质的溶解度曲线,下列说法不正确的是
A.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
B.当A中含有少量B时,可以通过冷却热饱和溶液的方法提纯A
C.升高温度可使接近饱和的C溶液变为饱和
D.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A
在一定温度下,向不饱和的NaNO3溶液中逐渐加入NaNO3晶体,在此变化过程中,溶液里溶质质量分数(ω)与时间(t)的关系正确的是
a、b 两种物质的溶解度曲线如图所示。下列说法不正确的是
| A.15℃时,a、b 的溶解度均为20g |
| B.加水或升温均可使b的饱和溶液变为不饱和溶液 |
| C.将 30℃时a的饱和溶液降温至15℃,溶质的质量分数不变 |
| D.分别向100g 水中加入20ga和 b,升温至30℃,所得溶液均为饱和溶液 |
下图是甲、乙两种固体物质的溶解度曲线。下列说法错误的是

| A. | 时,甲、乙两物质的溶解度相等 |
| B. | 乙的饱和溶液降温时,溶质质量分数保持不变 |
| C. | 甲中混有少量乙,可采用降温结晶的方法提纯甲 |
| D. | 时,甲的饱和溶液溶质质量分数为20% |
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应。溶液质量与加入Zn的质量关系如右图所示,有关说法正确的是
| A.a点溶液中的溶质有2种 | B.b点得到的固体为Cu |
| C.c点溶液中溶质为Zn(NO3)2 | D.d点得到的固体有2种 |
同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
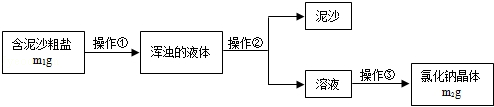
(1)操作②的名称是;
(2)操作①②③都要用到的一种玻璃仪器是,在操作③中,使用这种玻璃仪器的目的是.
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是(只写一种原因).
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是(填字母编号).
a、称量氯化钠所用天平砝码沾有杂质;b、用量筒取水时俯视读数;c、用量筒取水时仰视读数;d、配制溶液的烧杯用蒸馏水润洗过
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液ml(结果保留小数点后一位).
有一固体物质甲(不含结晶水)的溶液,在温度不变的条件下,经历如下变化: 。下列结论中,正确的是
。下列结论中,正确的是
| A.溶液Ⅰ一定是不饱和溶液 |
| B.该温度下,甲的溶解度是30g/100g水 |
| C.溶液Ⅰ和溶液Ⅱ中的溶质的质量分数可能相等 |
| D.溶液Ⅱ若再蒸发10g水,析出晶体的质量一定等于3g |
下图为甲、乙两种盐的溶解度曲线。下列说法正确的是

| A. | 甲、乙两种物质的溶解度都不相等 |
| B. | 将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法 |
| C. | 时,甲、乙两种物质的饱和溶液中,溶质质量分数均为15% |
| D. | 时,将30克乙物质放入100水中,所得溶质的质量为130克 |
下列曲线能正确表达对应的反应或过程的是()

| A. | 向一定量的水中加入生石灰 | B. | 红磷在装有空气的密闭容器中燃烧 |
| C. | 向一定量的烧碱溶液中加入盐酸 | D. | 向饱和 溶液中加入 固体 |