25℃时,向一定量不饱和KNO3溶液中逐渐加入KNO3固体,则下列图像中能正确表示此过程溶质质量变化规律的是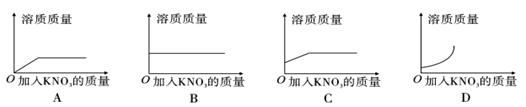
下图是A、B、C三种固体物质的溶解度曲线。(S单位:g/100g水,t单位:℃)回答以下问题:
①20℃时,A物质的溶解度 (6) (填>、=、<)B物质的溶解度。
②20℃时,将20克A物质溶于150克水,得到的溶液是 (7) (填饱和或不饱和)溶液,得到溶液的质量为 (8) 克。
③20℃时,将等质量的B和C分别加入盛有等质量水的烧杯中,充分搅拌后,其中一个烧杯中仍有少量固体未溶解,则未溶解的固体是 (9) 。
④ 用同一种方法可以使A、B、C三种物质的饱和溶液都有晶体析出,该方法是10) 。
⑤ 将30℃时120克A的饱和溶液稀释成10%,需要加水 (11) g。
甲、乙两种物质的溶解度曲线如图所示。叙述正确的是
| A.依据溶解度曲线可判断,甲的溶解度比乙的大 |
| B.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大 |
| C.将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温方法 |
| D.t1℃时,甲和乙的饱和溶液各100 g,其溶质的质量一定相等 |
K2CO3和KNO3在不同温度时的溶解度数据及对应的溶解度曲线如下:
| 温度/℃ |
20 |
30 |
50 |
60 |
80 |
|
| 溶解度 (g/100g水) |
K2CO3 |
110 |
114 |
121 |
126 |
139 |
| KNO3 |
31.6 |
45.8 |
85.5 |
110 |
169 |

①图1中表示KNO3溶解度曲线的是(24)(填“甲”或“乙”);
②曲线上M点的含义是 (25) ;
③图1中t1的温度范围为 (26) ;
④20℃时,60g K2CO3固体加入到50克水中,得到的溶液的溶质质量分数是(27) ;
⑤80℃ 时有KNO3饱和溶液(含少量K2CO3),若要得到较纯净的KNO3晶体,宜采用实验操作方法是 (28) ;
⑥40℃ 时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃ ,其结果如图2所示。有关说法中,正确的有 (29) 。(填字母)
A.烧杯Ⅱ中溶液是不饱和溶液
B.烧杯Ⅰ中溶解的是KNO3,烧杯Ⅱ中溶解的是K2CO3
C.升高温度或增加溶剂都有可能将烧杯Ⅰ中固体全部溶解
D.若将烧杯Ⅰ中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小
将20℃时某KNO3溶液均分为两份,第一份恒温蒸发掉10克水,析出a克晶体;第二份恒温蒸发掉20克水,析出晶体b克。则a与b的关系正确的是
| A.2a=b | B.2a≤b | C.2a≥b | D.2a<b |
以下是KCl的部分溶解度数据,下列说法中正确的是
| 温度(℃) |
0 |
20 |
40 |
60 |
| 溶解度(g/100g水) |
27.6 |
34.0 |
40.0 |
45.5 |
A.KCl饱和溶液中不能再溶解其他物质
B.20℃时,100 g KCl饱和溶液中含KCl 34.0 g
C.20℃的KCl溶液的浓度一定小于 40℃的KCl饱和溶液的浓度
D.60℃时,将一定质量分数KCl溶液降温到40℃,一定有晶体析出
用氯化钠固体配制一定质量分数的氯化钠溶液,必须使用的一组仪器是
| A.天平、烧杯、量筒、玻璃棒、药匙 |
| B.天平、烧杯、量筒、铁架台、药匙 |
| C.天平、烧杯、漏斗、蒸发皿、玻璃棒 |
| D.天平、集气瓶、漏斗、蒸发皿、玻璃棒 |
如图为a、b、c三种物质(均不含结晶水)的溶解度曲线。
①t1℃时c物质的溶解度是 (38) ;
②P点的含义是 (39) ;
③t2℃时,向60g的水中加入35g a物质,充分搅拌,所得溶液的质量是 (40) g;
④t1℃时,相同质量的a、b、c三种物质的饱和溶液中所含溶剂的质量最少的是 (41) (填“a”或“b”或“c”);
⑤欲将b物质的不饱和溶液变为饱和溶液,下列说法正确的是 (42) (填序号)。
Ⅰ.溶液中溶质的质量一定增加
Ⅱ.溶质b的质量分数可能增大
Ⅲ.溶液的质量可能不变
Ⅳ.可倾倒出一些水
医疗上用的生理盐水是0.9%的氯化钠溶液。要配制0.9%的氯化钠溶液100g。其中选用仪器或操作正确的是
| A.只需要托盘天平和量筒两种仪器 | B.用天平称量0.9g氯化钠 |
| C.用量筒量取100g水 | D.把食盐倒入量筒中搅拌溶解 |
2014年3月22日是第二十二个“世界水日”,它的主题是“水与能源”。关于水的知识有下列话题,请按要求填空:
①自来水生产过程中,可加 (7) (填写物质化学式)方法进行消毒杀菌。
②测定地下水的酸碱度常用 (8) 。
③水是最常用的溶剂。实验室用蔗糖配制一定溶质质量分数的溶液时,已经有以下仪器:玻璃棒、天平、烧杯、胶头滴管,还需要的仪器是 (9) 。配置好的蔗糖溶液可以保存较长时间,这体现了溶液的
(10) 性。
④保护水环境、珍爱水资源,是每个公民应尽的责任和义务。下列做法有利于保护水资源的是 (11) (填写选项编号)。
| A.大量使用化肥农药 | B.工业废水处理达标后再排放 |
| C.使用含磷洗衣粉 | D.生活污水直接排放 |
⑤科学家们在实验室中利用催化剂在光照条件下进行水的分解反应,以得到清洁能源。写出该反应化学方程式 (12) 。
下图为硝酸钾(KNO3)和氯化钠(NaCl)两种物质溶解度曲线。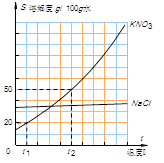
①t1℃时,两种物质溶解度的大小关系:S(NaCl) (15) S(KNO3)(填“>”、“=”或“<”)。
②t2℃时,将25g氯化钠固体投入50g水中,充分溶解后可得到的氯化钠溶液是 (16) (填“饱和溶液”或“不饱和溶液”)。
③t1℃时,硝酸钾溶解度为 (17) 。若将该温度下硝酸钾饱和溶液加水稀释后不发生改变的是 (18) (填字母)。
| A.溶剂质量 | B.溶质质量 |
| C.溶质质量分数 | D.硝酸钾的溶解度 |
④某硝酸钾溶液中含有少量氯化钠杂质,要提纯得到较纯净的硝酸钾固体的主要步骤依次是: (19) 、 (20) 、 (21) 、洗涤、烘干。
⑤t℃时,在100g25%的硝酸钾溶液中加入硝酸钾固体,所加硝酸钾固体质量(m)与溶液的溶质质量分数(C%)的关系如图所示,x= (22) (精确到0.1%);t与t1、t2的关系是 (23) 。(填编号)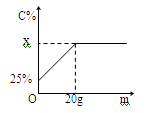
Ⅰ.t<t1 Ⅱ.t1<t<t2 Ⅲ.t>t2
室温下,将一定量生石灰加入到100g饱和的澄清石灰水中,充分搅拌后恢复到室温,滤去不溶物,所得到的溶液与原石灰水相比较,下列判断正确的是
| A.溶质质量减小 | B.溶剂质量不变 |
| C.溶质质量分数增大 | D.溶液质量增大 |
将80℃时一定质量的硝酸钾饱和溶液冷却到30℃,下列有关叙述中正确的是
①溶质的质量不变 ②溶剂的质量不变 ③溶质的质量分数不变
④有一些硝酸钾晶体析出 ⑤30℃时所得硝酸钾溶液仍是饱和溶液
| A.①③ | B.②③ | C.②④⑤ | D.①③⑤ |
溶液的相关叙述正确的是
| A.溶液就是均一、稳定的液体 |
| B.某物质的饱和溶液的溶质质量分数一定比不饱和溶液大 |
| C.溶液中溶质的质量分数可以表示每100g溶液中溶质的质量 |
| D.溶液的溶质质量分数越大,溶质的质量越大 |