下图是甲、乙两种固体物质的溶解度曲线。下列说法错误的是

| A. | 时,甲、乙两物质的溶解度相等 |
| B. | 乙的饱和溶液降温时,溶质质量分数保持不变 |
| C. | 甲中混有少量乙,可采用降温结晶的方法提纯甲 |
| D. | 时,甲的饱和溶液溶质质量分数为20% |
关于溶液的说法正确的是
| A. | 溶液都是无色透明的 | B. | 水可以溶解任何物质 |
| C. | 均一,稳定的液体都是溶液 | D. | 饱和溶液不一定是浓溶液 |
下列是"一定溶质质量分数的氯化钠溶液的配制"的实验操作示意图,其中错误的是
| A. |
取用氯化钠固体 |
B. |
.称量氯化钠固体 |
C. |
量取水的体积 |
D. |
溶解 |
要配制100 5%的 溶液,除了需要托盘天平和量筒外,还需要用到的一组仪器是
| A. | 烧杯、试管、玻璃棒 | B. | 烧杯、胶头滴管、玻璃棒 |
| C. | 烧杯、胶头滴管、漏斗 | D. | 烧杯、酒精灯、玻璃棒 |
下图是恒温下模拟海水晒盐过程的示意图,与丙烧杯溶液的溶质质量分数一定相同的是()

| A. | 甲 | B. | 甲和乙 | C. | 乙和丁 | D. | 丁 |
将60℃的硝酸钾溶液降温至20℃,有晶体析出。有关该过程的说法错误的是()
| A. | 60℃时的溶液一定是硝酸钾饱和溶液 |
| B. | 20 摄氏度时的溶液一定是硝酸钾的饱和溶液 |
| C. | 硝酸钾的溶解度随温度降低而减小 |
| D. | 硝酸钾的晶体可采用降温结晶的方法得到 |
下列曲线能正确表达对应的反应或过程的是()

| A. | 向一定量的水中加入生石灰 | B. | 红磷在装有空气的密闭容器中燃烧 |
| C. | 向一定量的烧碱溶液中加入盐酸 | D. | 向饱和 溶液中加入 固体 |
下列有关溶液的说法正确的是
| A. | 配制好6%的 溶液,装瓶时不小心撒漏一部分,瓶中 溶液浓度仍为6% |
| B. | 长期放置后不会分层的液体一定是溶液 |
| C. | 饱和溶液一定比不饱和溶液溶质质量分数大 |
| D. | 降低饱和溶液的温度,一定有晶体析出 |
用固体氯化钠配制50g溶质质量分数为6%的氯化钠溶液。下列有关做法正确的是
| A.将3.0g氯化钠直接放在托盘天平左盘上称量 |
| B.用10mL量筒量取所需水的体积 |
| C.选择的玻璃仪器是:烧杯、量筒、玻璃棒、胶头滴管、试剂瓶 |
| D.可选用内壁附有水珠的烧杯来配制溶液 |
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示。下列说法正确的是()

| A. | 甲物质的溶解度大于乙物质的溶解度 |
| B. | 时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g |
| C. | 时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 |
| D. | 时甲、乙的饱和溶液降温到 时,析出晶体的质量甲一定大于乙 |
下图为M、N两种固体饱和溶液溶质的质量分数(C%)随温度(t)变化的曲线,下列说法正确的是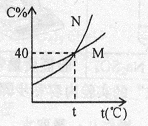
| A.50gM放入150g水中形成不饱和溶液 |
| B.t℃时,M的饱和溶液中溶质与溶剂的质量比为2:5 |
| C.80gN放入150g水中全部溶解,此时溶液的温度一定低于t℃ |
| D.100gN的溶液,蒸发15g水、冷却至t℃后得到10g晶体,原溶液溶质的质量分数为40% |
a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是
| A.15℃时,60g a、b 的饱和溶液中均含有10g溶质 |
| B.加水或升温均可使b的饱和溶液变为不饱和溶液 |
| C.将 30℃时a的饱和溶液降温至15℃,溶质的质量分数变大 |
| D.向100g 水中加入20g a,升温至30℃,所得溶液为饱和溶液 |
某溶液溶质的质量分数为20%,加入50g水后变为10%,则稀释后溶液中溶质的质量是
| A.5g | B.10g | C.20g | D.50g |
配制50g溶质质量分数为15%的氯化钠溶液的实验过程中不需要用到的仪器是