将氢氧化钠和氯化钠的混合物19.3g,放入80.7g水中使其完全溶解,再加入100g溶质质量分数为7.3%的稀盐酸,恰好完全反应。试计算:
(1)将上述浓度的稀盐酸100克稀释为溶质质量分数为4%的稀盐酸,需要加入水的质量;
(2)原混合物中氢氧化钠的质量;
(3)反应后所得溶液中溶质的质量。
小明在老师的指导下粗略测量一瓶稀盐酸的溶质质量分数,具体步骤如下:
步骤一:配制溶质质量分数约为1%的氢氧化钠溶液。
步骤二:向10克待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使
用pH计记录溶液的pH变化情况,绘制图像如图。
(1)在“步骤一”中有计算、 、溶解三个具体步骤。
(2)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,在a点的溶液中
的微粒有 。(用化学符号表示)
(3)请结合右图,计算①该稀盐酸的溶质质量分数;②b点时溶液中溶质的质量分数。(结果精确到0.1%)(写出计算过程)
(4分)某校化学兴趣小组的同学为了制取氢氧化镁,他们取9.5g氯化镁固体全部溶解在40.5g水中制成不饱和溶液,然后向其中加入55.8g某溶质质量分数的氢氧化钠溶液恰好完全反应。请计算:
(1)制得的氢氧化镁的质量。
(2)反应后所得溶液中溶质的质量分数。
在实验考试前夕,小东同学在实验操作练习中,发现用完全相同的两份稀盐酸和相同质量的大块大理石、小块大理石分别反应,大块的反应速率要慢,原因是什么? _________ .
小东又发现盛放氢氧化钠的试剂瓶口有白色粉末.为了确定白色粉末的成分,他进行了如下的探究:
(1)小毛猜测白色粉末中含有碳酸钠,请指出他的理由: _________ (用化学方程式表示).
(2)为了确定自己的猜测,小东设计了如下的方案:取少量白色粉末于试管中,加水溶解配成溶液,再用 _________ 检验,看到溶液中有 _________ 产生,从而使自己的猜想得到了证实.
(3)玻璃中的SiO2可以和氢氧化钠发生类似的CO2的反应,则SiO2与氢氧化钠反应生成盐的化学式为 _________ .
(4)为了进一步确定白色粉末中碳酸钠的质量分数,小东取了2g白色粉末,加入足量的水充分溶解,再滴加澄清石灰水,充分反应后,过滤,得到了白色沉淀1g.
①在过滤时,需用到玻璃棒,它的作用是 _________ ;
②请你帮小东计算:白色粉末中碳酸钠的质量分数.
某化学兴趣小组使用下图所示装置,对某种锌铜合金的成分进行测量。先取足量稀硫酸于烧杯中,再向其中加入15.0g合金样品开始计时,并将电子天平的读数记录在下表中,完成下列计算:
(1)反应完全后产生氢气的质量是多少?
(2)锌铜合金中铜的质量是多少?
(3)反应完全后溶液中溶质的质量分数是多少?
| |
空烧杯 |
加入硫酸后 |
加入合金后 5分钟 |
加入合金后 10分钟 |
加入合金后 30分钟 |
| 读数(g) |
21.3 |
169.7 |
184.6 |
184.3 |
184.3 |
28.7g的氯化钠和硝酸钠的混合物,溶于100g水中,向所得溶液中加入134g的硝酸银溶液,恰好完全反应,得到溶液的质量是234g。计算:原混合物中钠元素的质量分数。(已知:AgNO3 + NaCl = AgCl↓+ NaNO3;计算结果精确到1%)
我们的日常生活离不开食盐,食盐的主要成分是氯化钠,某同学想测定配制的氯化钠溶液的溶质质量分数。取100g氯化钠溶液,加入足量的硝酸银溶液,生成14.35g沉淀。试计算硝酸银溶液中溶质质量分数。
硅(Si)是太阳能电池和电脑芯片中不可缺少的材料。硅生产过程中的一个重要化学反应为SiO2 + 2C 高温 Si + 2CO↑。若生产5.6 g硅,理论上需要二氧化硅(SiO2)多少克?
金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2===2Na2CO3+O2↑。为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图所示的实验。
(1)A装置中所发生反应的化学方程式为 ;实验室确定气体发生装置时应考虑的因素是 ;检查A装置的气密性的方法是:将A装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到 现象,即可证明装置不漏气。
(2)表明二氧化碳没有被过氧化钠完全吸收的现象是 。
(3)用带火星的木条放在集气瓶口检验氧气是否收集满,这是利用了氧气性质中的 ;
(4)如果用脱脂棉包裹一定量的Na2O2固体,然后向其中通入CO2,脱脂棉很快就燃烧此现象说明该反应为 反应(填“吸热”或“放热”);
(5)常温下水也能与Na2O2反应生成氧气和氢氧化钠,该反应的化学方程式为2Na2O2+2H2O===4NaOH+O2↑,若要检验干燥的二氧化碳能否与过氧化钠反应生成氧气,对以上实验装置的改进为
(6)实验室中的过氧化钠如果保存不当,容易与空气中的CO2和水蒸汽发生反应变质。今称取10g过氧化钠样品(杂质不参加反应)放人烧杯中,向其中加入10g水,二者完全反应后。称量烧杯中剩余物质的总质量为18.4g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算过氧化钠样品中杂质的质量分数(要写出计算过程)。
实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数。现取10g稀硫酸样品,将5%的NaOH溶液逐滴加到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示。试回答: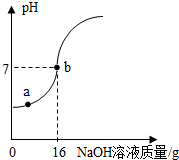
(1)a点溶液中含有的离子有 。
(2)计算稀H2SO4的溶质质量分数。
鸡蛋壳的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验: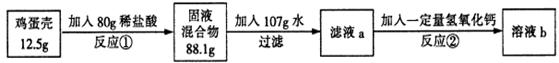
反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。请回答下列问题(可以选下列任意两个问题回答,并写出计算过程):
(1)反应①产生的CO2的质量为___________________;
(2)该鸡蛋壳中碳酸钙的质量分数为________________;
(3)所加氢氧化钙的质量为__________________;
(4)溶液b中溶质的质量分数为_________________;
计算过程:
为了测定碳酸钠样品(内含有氯化钠)的纯度,现将10克样品加入重为5克的烧杯中,再往烧杯中加入40克水搅拌至固体完全溶解,再向烧杯中加入50克稀盐酸,恰好不再产生气泡,称得烧杯总质量为102.8克。
请完成下列计算:
(1)反应产生的气体的质量是多少?
(2)碳酸钠样品中碳酸钠的质量分数是多少?
(3)盐酸溶液中溶质的质量分数是多少?
实验室中有一瓶部分变质了的NaOH溶液,小丽为了测定溶液中溶质的Na2CO3的质量分数,现取20g待测溶液,向其中逐滴加入CaCl2溶液,产生沉淀质量与所加CaCl2质量的关系如图所示。
(1)B点处所得溶液中溶质有 。
(2)若加入的CaCl2溶液的质量分数为11.1%则需该溶液的质量为________
(3)求待测溶液中Na2CO3的质量分数。(写出计算过程)
电镀厂的废水中含有H2SO4和CuSO4,为了回收Cu(OH)2并得到化肥,工厂化验室取来200g废水,逐滴加入KOH溶液,反应情况如下图所示。请回答:
(1)K2SO4属于 肥;
(2)求所用的KOH溶液的溶质质量分数;
(3)若每天处理200吨废水,可制得 吨K2SO4。