铁、铝、铜是日常生活中使用最广泛的金属。
(1)上述三种金属中,人类最早大规模冶炼和使用的是____
(2)常温下一些金属的物理性质数据如下:
| 金属单质 |
铜 |
铝 |
锌 |
铁 |
铅 |
| 导电性(以银的导电性为100作标准) |
99 |
61 |
27 |
17 |
7.9 |
| 密度/(g·cm-3) |
8.92 |
2.70 |
7.14 |
7.86 |
11.3 |
| 熔点/℃ |
1083 |
660 |
419 |
1535 |
328 |
| 硬度(以金刚石的硬度为10作标准) |
2.5~3 |
2~2.9 |
2.5 |
4~5 |
1.5 |
分析上述数据,碎石用的大锤常用铁制而不用铝制,原因是_____________________。
(3)金属铝与氧化铁在高温条件下能发生置换反应,其化学方程式为 。
(4)炼铁的原理是利用一氧化碳与氧化铁反应。在实验室里,可用下图所示装置进行实验:实验中玻璃管内的粉末由红色变为 色,该反应的化学方程式为 。
2010年12月22日,沉没在苍茫海水中800多年的中国古沉船“南海一号”的“惊艳一浮”,让无数国人为之自豪,它既为海上丝绸之路提供了实证,又推动了中国水下考古学科的建设。据保守估计,其上载有6万至8万件文物,在已发掘出的文物中发现了大量瓷器、宋代铜钱、铁锅、梳篦等物品。
(1)中国的陶瓷举世闻名,陶瓷材料属于 材料;
(2)中国的铁锅源远流长,受到联合国卫生组织的推崇,原因之一是由于铁锅能为人体补充铁元素。若人体缺乏铁元素,容易引起 症;
(3)被发掘出的宋代铜钱已经锈迹斑斑,这是因为铜能与空气中的氧气、水以及二氧化碳发生化合反应生成铜绿[Cu2(OH)2CO3],请写出该反应的化学方程式: .
根据铜绿的组成判断,若要除去铜钱表面的铜绿,可选用的试剂为 (填化学式);
炼铁厂以赤铁矿石(主要成分为Fe2O3)、焦炭、石灰石、空气等为主要原料炼铁,主要反应过程如题图所示:
请根据题图和所学知识回答相关问题:
(1)生铁属于 (填“纯净物”或“混合物”)。
(2)炼铁厂用来炼铁的主要设备是 。
(3)反应过程①②③中,属于化合反应的有 (填序号)。
(4)原料中焦炭的作用有 、
有下列实验,试管中的药品如图所示: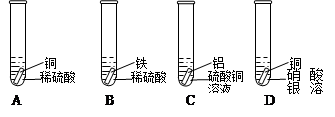
(1)上面四支试管中有气泡产生的是(填序号) ;银白色金属表面有红色物质生成的反应的化学方程式为 。
(2)从上述的实验现象中,对于铁、铜、银、铝的金属活动性强弱关系不能确定的是
(填金属的化学式)
人类对金属的开发和利用是循序渐进的。
(1)青铜器是人类较早使用的金属制品。西汉时期,人们主要采用“湿法冶金”。如将铁浸入硫酸铜溶液中,该反应的化学方程式为 。
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来。例如,
高炉炼铁所涉及的物质转化过程如下:
其中,物质A为 (填化学式),A与赤铁矿中的氧化铁反应的化学方程式为 。
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多
种方法防止金属腐蚀。例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原
因是 。
(4)铝的金属活动性比铁 (填“强”或“弱”),但铝制品却具有比较好的抗腐
蚀性能,其原因是 (用化学方程式说明)。
人类发展的历史进程中人们不断研制出各种不同的用具,制造用具的材料也在不断地发生变化,金属制品因其美观、耐用、轻便易成型而被人们广泛利用,请根据所学知识及生活知识参与有关金属制品探究.
(1)以下工具的制作过程中没有发生化学变化的是 .
A.原始人制作石刀 B.冶炼青铜 C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序 (填序号).
A.铁 B.青铜 C.铝
从以上顺序可以看出,金属制品的出现顺序与 有关,
(3)金属区别于非金属的主要物理性质是,金属具有 ,金属区别于非金属的主要化学特征是 .写出实验室最常用来制取氢气的化学方程式: .
(4)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗? .
(5)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理: .
(6)大量有关钢铁的成语与民间谚语中.“百炼成钢”是指铁在高温条件下反复敲打的目的是降低其中 .从而了解钢与铁的机械性能不同是因为两者 .
人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.
(1)金属大规模被使用的先后顺序跟 (填序号)选项关系最大.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性.
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中(反应中Mn显+2价),请回答:
| 金属 |
铁 |
锰 |
| 与盐酸反应现象 |
放出气泡速率缓慢 |
放出气泡速率较快 |
| 结论 |
活动性铁 < (填“>”“<”)锰 |
除了比较与酸反应产生气体速率的快慢,请你再举出一种可比较这二种金属活动性强弱的方法(写出所需药品即可): .
(3)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是 ;
②若天平失去平衡,则指针一定偏向放 的一边.
月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。我国四川省有大型钒钛磁铁矿,由钒钛磁铁矿提取金属钛的主要工艺过程如下:
① 钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价为 价。
②TiCl4在高温下与足量Mg反应生成金属Ti的化学方程式 ,该反应属于 (填基本反应类型)。
③ 上述生产过程中得到的金属钛中混有少量金属杂质,若在实验室提纯上述金属钛,可将其先加入 (填试剂名称)中,再 (填操作名称)。
将3枚洁净的铁钉同时置于下图所示的试管中,3天后观察到I、Ⅲ中铁钉不生锈,Ⅱ中铁钉明显生锈。对照实验I、Ⅱ,可知铁锈蚀的条件之一为 ;防止铁锈蚀的一种方法是 。
铁是生产生活中应用最广泛的一种金属。
(1)在酱油中加入铁强化剂,是我国为解决________(填“甲状腺肿大”、“贫血”或“骨质疏松”)而实施的项目。
(2)铁元素与地壳中含量最多的元素组成的化合物的化学式为________(写出一种即可)。高铁酸钠(Na2FeO4)是一种新型高效的净水剂,高铁酸钠中铁元素的化合价为________。
(3)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。请将下列脱氧中的主要反应的化学方程式补充完整:4Fe(OH)2+O2+2________===4Fe(OH)3;此反应的基本类型是____________。
依据所学的化学知识解答:
(1)将墨汁滴入一杯清水中,清水很快变黑,说明________________________;
(2)铁在空气中容易生锈,这是因为________________________________(用化学方程式表示),防止铁制品锈蚀的方法有________(写一种即可);
(3)若装白磷的储罐起火,可以用水灭火,也可以用沙土填埋灭火。其中用沙土填埋灭火的原理是________________________________。
生活离不开金属。
(1)右图“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠和水等,其发热原理是利用铁生锈时放热。
发热剂需与空气中 接触才会发热。
(2)已知下列各组物质间均能发生置换反应。
A.Fe 和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe 和CuSO4溶液反应的化学方程式 。
②Mn、Fe、Mg 、Cu四种金属的活动性由强到弱的顺序 。
(3)化学小组在实验结束后,进行了如下废液处理:
①Ⅰ中的操作名称是___________。
②写出Ⅱ中一定发生反应的化学方程式 ___ _________ 。
③滤液的组成可能是 。
生活处处皆化学。
(1)生活中的燃烧
①着火点比较:蜂窝煤 小木条(填“>”、“<”或“=”)。生煤炉过程中,不断扇入空气目的是 ,煤不完全燃烧产生一种有毒气体的化学式是 ;
②用水灭火的原理是 ,新型水成膜泡沫灭火剂扑灭油类火灾时,析出的液体和泡沫在油面上铺展形成一层水膜,进而灭火,原理是 。
(2)金属在生活中用途广泛
①下列生活用品,主要是由金属材料制成的是 ;
②用铁锅烹饪食物时,会有少量铁屑在胃部转化为可被吸收的Fe2+,反应的化学方程式为 ,是 反应(填基本反应类型)。
③用铝箔包装药物,主要利用了铝的 性;
④铜具有很好的 性,故可作导线。近代湿法冶金的先驱是指 (填化学方程式),铜和空气中的O2、H2O及 会生成铜锈[Cu2(OH)2CO3],反应的化学方程式是 。
(3)生活中的水和溶液
①处理自然水时,常用的混凝剂是 (填名称)。二氧化氯是一种新型的消毒剂,其化学式为 ;
②欲配制500mL 0.9%的生理盐水(密度为1.0 g/mL),需要NaCl的质量为 g;配制过程中,玻璃棒的作用是 ,称量NaCl时,若将砝码放在左盘(1 g以下用游码),其他操作均正确,则所配溶液中溶质质量分数将 0.9%(填“>”、“<”或“=”)
③右图是净化河水的简易装置,下列说法正确的是 ;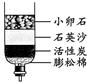
| A.净化后的水是纯净物 | B.此装置能对水杀菌消毒 |
| C.此装置能把硬水变为软水 | D.活性炭能吸附水中的色素及异味 |
④KNO3可用作配制无土栽培营养液,下表提供了KNO3在不同温度时的溶解度:
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
| 溶解度/g |
13.3 |
31.6 |
63.9 |
110 |
169 |
a.从上表可总结出KNO3的溶解度随温度变化的趋势是 ;
b.20℃时,将20gKNO3加入50g水中充分溶解,所得溶液的质量为 g;
c.现有60℃时的KNO3饱和溶液210 g,降温至20℃,会析出KNO3 g;
(4)食品包装学问大
①我区特产——嘶马羊耳采用真空包装,延长了食品的保质期,原理是 ;
②将N2充入包装袋内做保护气,是因为N2的化学性质 (填“活泼”或“稳定”);
③右图是“504双吸剂”的标签,请问答下列问题:
a.其中至少含有 种单质;
b.取少量双吸剂加入蒸馏水中,振荡后静置,测得上层清液的pH=9,若用pH试纸测定,具体操作是 。通入CO2后,上层清液变浑浊,写出上述变化的化学方程式 、 ;
c.为测定此双吸剂的使用效果,取足量双吸剂做了如右图所示的实验,一段时间后,进入试管中水的体积 21%(填“>”、“<”或“=”),理由是 ;
d.部分失效的双吸剂中,有红棕色固体,其主要是 ;
e.此双吸剂中,NaCl的作用可能是 。
金属在日常生活中随处可见,研究金属的性质可以更好地利用金属。
(1)铝、铁、铜是常见金属。下列生活用品中,主要利用金属导热性的是______(填序号)。
(2)“淬火”是金属热处理常用的方法。宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为 ,该反应属于基本反应类型中的 反应。
(3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有 。
(4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等。下列做法与此结果相符的是 (填序号)。
| A.相同质量的三种金属与足量的稀盐酸反应 |
| B.2.4 g镁、6.5 g锌、5.6 g铁与足量的稀盐酸反应 |
| C.向足量的镁、锌、铁中加入稀盐酸的质量比为2︰3︰2 |
| D.足量的三种金属与等量的稀盐酸反应 |