已知Fe2O3在氢气流中加热时,在不同的温度条件下
可生成Fe3O4、FeO或Fe,上述反应利用了氢气的 性。为了探究某次实验中氢气与氧
化铁反应的产物,某科学兴趣小组将反应生成的固体称量后放入硫酸铜溶液中(已知铁的氧
化物不与硫酸铜反应,且不溶于水)。一段时间后过滤,将得到的固体干燥并再次称量,若
发现固体质量 (填“增加”、“减少”或“不变”),则可认为产物中有Fe。
铁质水龙头长期使用容易生锈,小明从自家水龙头上取下一些铁锈样品,用下图所示的装置进行实验。
(1)B处澄清石灰水变浑浊,反应方程式为 ,C处酒精灯的作用是
(2)实验结束,小明将所得的黑色固体物质放入足量的稀硫酸中,发现没有气泡,这说明生成物中 (有或没有)铁。
为解释这个现象,小明查阅下列资料:
Ⅰ。已知铁的氧化物有FeO、Fe3O4、Fe2O3,,在一定条件下,均能逐步失去其中的氧,最终被还原为铁。
Ⅱ。某炼铁厂对氧化铁和一氧化碳进行热反应分析,获得相关数据并绘制成下图。
通过分析资料确定:
①700℃时氧化铁和一氧化碳进行反应的产物是 (填FeO或Fe3O4或Fe).
②小明实验失败的主要原因是 。
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的应用
(1)下列铁制品的利用与金属导热性有关的是________________(填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的________________。
Ⅱ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:___________________________;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能_____________________;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的_________(填装置编号);
(2)图中装置C、D的作用分别是 ____________、_______________;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的_____________(填试剂名称),反应的化学方程式为 ______________________;
(4)该装置设计有一个明显缺陷,你认为是______________________________。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下: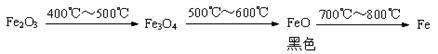
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;②_________ ③____________。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质量 |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,纯净的Fe2O3固体质量为_____________g,请选择有效的数据,推断出反应后黑色固体的成分(写出计算过程)__________________________。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:__________________________。
某研究性小组在实验室中模拟炼铁化学原理的实验。实验前查阅有关资料,获得以下信息:一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁粉,三种物质均为黑色,其中四氧化三铁、铁粉能被磁铁吸引。
在一定温度下,该小组同学用下图所示的实验装置进行一氧化碳还原纯净的氧化铁的实验。
(1)在上述实验装置(已检查气密性)中加好药品、连接好仪器后进行的第一步操是 。
(2)实验开始时,右侧试管中发生反应的化学方程式为 。
(3)从环保角度看,该小组设计的实验装置有不足之处,你认为该如何改进? 。
(4)实验中观察到玻璃管内固体由红棕色全部变为黑色。将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体全部能被吸引,则该黑色固体中不可能含有 (填化学式)。
(5)取上述研磨后的黑色固体20g,设计如下实验:
根据上述实验结果,判断20g黑色固体的成分是 (填化学式)。
(6)若要从以上探究所得FeSO4、CuSO4的混合溶液中回收铜和硫酸亚铁晶体,可设计如下实验方案:
步骤①中,金属X是 ,发生反应的化学方程式为 ;步骤②中,加入过量稀硫酸的目的是 。
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的应用
(1)下列铁制品的利用与金属导热性有关的是 (填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的 。
Ⅱ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式: ;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的 (填试剂名称),反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下:
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质量 |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,纯净的Fe2O3固体质量为 g,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) 。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
(2)某钢铁厂每天消耗5000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁98%的
生铁的质量是多少?
Ⅱ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的澄清石灰水,该反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑
后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现
固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下: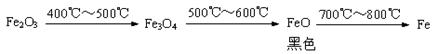
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质量] |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g] |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) 。
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
(2)某钢铁厂每天消耗5000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?
II.实验探究炼铁原理某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4 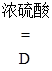 CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的澄清石灰水,该反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解。
b.Fe2O3与CO反应的固体生成物可能情况如下:
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质 |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程)
科学兴趣小组用以下装置探究炼铁的原理。
(1)方框中连接的是装置C和D,目的是进行尾气处理,则导管接口的连接顺序为a→ 。(用箭头和接口字母表示)
(2)玻璃管A中发生反应的化学方程式为 。
关注物质变化的过程,探究物质变化的条件是化学学习的重要内容之一。以下是初中化学进行的部分探究实验,请回答有关问题:
(1)实验A探究的是物质燃烧的条件,由此实验得出的结论是:在通常情况下物质燃烧需要满足以下条件: 。
(2)写出A实验中白磷燃烧的化学方程式 。
(3)根据你所掌握的知识,实验B中左、中、右三支试管中,哪支试管中的铁钉易生锈 (填“左边”或“中间”或“右边”)
(4)请总结出铁制品发生锈蚀的基本条件是 。
(5)写一种防止铁制品锈蚀的方法 。
含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途
I.以含锌废渣(主要成分为
,杂质为
﹑
)为原料制备七水硫酸锌(
)的流程如下。

(1)粉碎的目的是。
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管﹑玻璃棒﹑和,此处玻璃棒的作用是。
(3)物质X是,滤渣中含有的金属单质有,除铜时发生的反应属于反应(填基本反应类型)。
(4)流程中获得七水硫酸锌前省略的操作是﹑冷却结晶﹑洗涤和低温烘干。
(5)某温度下,
分解得到一种铁﹑氧质量比21:8的氧化物,该氧化物的化学式。
(6)除铁过程中,温度pH对除铁效果的影响分别对如图所示。由图可知,除铁时温度应控制在℃为宜,pH应控制在为宜。

II.以某菱锌矿(
含量为62.5%)为原料制备锌的原理如下(假设杂质不参加反应):
则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)
生物浸出技术在金属冶炼中应用广泛。嗜热细菌在65-80℃酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分
)产生硫酸盐,进而生产铜和绿矾,主要流程如下:

(1)分离出矿渣的操作是。
(2)若试剂b为
粉,反应①的化学方程式为。
(3)氢氧化铁与试剂a发生中和反应,反应②的化学方程式为。
下图所示的是一氧化碳还原氧化铁的实验。请回答下列问题:

(1)一氧化碳还原氧化铁的化学方程式为。
(2)A处的现象是。B处的现象是。
(3)C处酒精灯的作用是。
"2014青岛世园会"于4月25日正式开园,主题是"让生活走进自然",倡导人与自然和谐相处的绿色发展理念。
(1)下列做法不符合人与自然和谐相处的绿色发展理念的是。
| A. | 通过风力和太阳能发电来驱动空气取水装置从潮湿的空气中得到水,用于浇灌植物 |
| B. | 在大型场馆的房顶设"光线导入"装置,减少场馆白天开灯的数量 |
| C. | 景区鲜花大道覆盖用秸秆等废弃物再生的无土草皮,进行防尘、保湿 |
| D. | 园区餐厅使用一次性木筷,以确保饮食卫生 |
(2)海洋植物馆门口,一棵会光闪闪的人造植物"黄余奇葩--金耐冬"格外引人沣目。它是以优质木材雕刻而成,外贴纯度为99.7%的黄金箔。
黄金制成金箔是利用了黄金良好的性,"金耐冬"长久不褪色,总是金光闪闪是因为。

(3)世园会植物馆号称亚洲第一大钢结构馆,拼装钢材杆件达到14000 多根,所有杆件均为现场拼装焊接。

①焊接钢材杆件要先除锈。用稀盐酸除锈(
)的化学方程式为;
②用氧气乙炔焊机焊接钢件时,要先调整乙炔(
)和氧气的比例,氧气不能过量,如果氧气过量,将导致焊接不牢。写出乙炔充分燃烧的化学方程式;请分析氧气过量会导致焊接不牢的原因;
③植物馆内温热潮湿,为防止钢件生锈,请你写出一种可行的方法。
“对比实验”是化学学习中行之有效的思维方法。某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题。
(1)通过实验A,可以说明燃烧的条件之一是 ,实验中使用铜片,是利用了铜的 性(填一条物理性质)
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与水
和 直接接触。写一种除去铁锈的方法 。
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 。
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的。烧杯②中是酚酞溶液,当烧杯①中液体由浓氨水换成浓盐酸时②中溶液的颜色的变化是 其中盐酸与NaOH的反应属于 反应(填基本反应类型)
人类生产和生活都离不开金属.早在春秋战国时期,我国就开始生产和使用金属.
Ⅰ.随着贵(阳)→广(州)高铁的开通.贵阳已进入高铁时代.高铁建设需要大量的钢铁.那钢铁是怎样炼成的呢?
[原料]赤铁矿(主要成分是氧化铁)、焦炭、空气等.
[流程]主要反应过程如图。

[原理](1)反应的化学方程式:① ,②,③ .
(2)反应①中空气要过量,目的是 .
Ⅱ.锰钢是一种合金,可用于高铁建设.若金属活动性:锰〉铁.请设计实验加以验证.
实验方案是(不用描述实验现象).
Ⅲ.铝合金不但用于日常生活,还用于火箭、飞机的制造.某铝合金只含铝和另一种金属X.为确定其成分,在实验室将mg该铝合金投入稀硫酸中,发现合金完全溶解,并生成ng氢气,铝与稀硫酸反应的化学方程式为.若要确定该合金中金属X的相对原子质量还需要的条件是.