2015年初中毕业升学考试(北京卷)化学
下图为空气成分示意图(按体积计算),其中"a"代表的是()

| A. | 氧气 | B. | 氮气 |
| C. | 二氧化碳 | D. | 稀有气体 |
下列酒精灯的使用方法正确的是
下列物质的用途中,利用其化学性质的是
| A. | 干冰用于人工降雨 | B. | 天然气用作燃料 |
| C. | 液氮用作冷冻剂 | D. | 银用于制作导线 |
下列实验方法一定能达到实验目的的是
| 选项 |
实验目的 |
实验方法 |
| A |
检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
| B |
鉴别 和 | 分别点燃,在火焰上方罩一干冷烧杯 |
| C |
鉴别石灰水和
溶液 |
加入适量的稀盐酸 |
| D |
比较
的金属活动性 |
将
和
分别放入
溶液中 |
a,b两种物质的溶解度曲线如下图所示.下列说法不正确的是()

| A. | 将 ℃时b的饱和溶液加水可变为不饱和溶液 |
| B. | 将 ℃时a的饱和溶液降温至 ℃,溶液质量不变 |
| C. |
℃时,两种物质的饱和溶液中溶质质量分数a
 b b
|
| D. | 将 ℃时a、b的饱和溶液分别降温至 ℃,两溶液的溶质质量分数相等 |
下图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明
密度大于空气且能与水反应的现象是()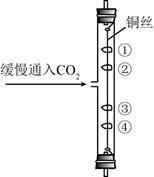
| A. | ①变红,③不变红 |
| B. | ④变红,③不变红 |
| C. | ①、④变红,②、③不变红 |
| D. | ④比①先变红,②、③不变红 |
纳米材料具有特殊的性质和功能.纳米二氧化钛( )参与的光催化反应可使吸附在其表面的甲醛等物质被氧化,降低空气中有害物质的浓度.正钛酸 在一定条件下分解失水可制得纳米 .下列说法不正确的是()
| A. | 甲醛对人体健康有害 |
| B. | 纳米 添加到墙面涂料中,可消除甲醛 |
| C. | 纳米 与普通的 的性质、功能完全相同 |
| D. | 制备纳米 的反应: |
已知: ,下图表示一定质量的 和 固体混合物受热过程中,某变量 随时间的变化趋势,纵坐标表示的是()

| A. | 固体中氧元素的质量 | B. | 生成 的质量 |
| C. | 固体中 的质量 | D. | 固体中钾元素的质量分数 |
下面连环画记录了雯雯参观中国地质博物馆的一天.

(1)早餐食物中有花卷、牛奶、鸡蛋和苹果,其中富含蛋白质的是.
(2)陶瓷餐盘的主要成分之一是硅酸钙
,其中硅元素的化合价是.
她出发了.
(1)她携带的物品中,主要材料属于有机合成材料的是(填字母序号)
A.水壶 B.帽子 C.背包
(2)如图③所示,乘坐地铁禁止携带的物品中,属于易燃易爆品的是.
她和同学们进入博物馆.
她看到了许多矿石标本,其中的4种矿石及其主要成分如下:

(1)上述矿石标本的主要成分中,所含元素种类最多的是(填字母序号).
(2)她根据辉铜矿的主要成分,推测以辉铜矿为原料,可制得含铜元素或含硫元素的产品,她的依据是化学反应前后不变.
(3)她依据化学式计算出
的相对分子质量为222,计算式为.
参观结束时,老师进行了小结,并就金属冶炼和金属回收再利用提出了两个问题,请同学们用化学方程式作答.
(1)工业上用一氧化碳和赤铁矿炼铁的原理是.
(2)废旧钢铁表面的铁锈可用盐酸除去,其原理是.
人们的生产生活离不开能源。
(1)目前人们使用的燃料大多来自化石燃料,如、石油、天然气等。
(2)开发和利用新能源是解决能源问题的重要途径。下列利用了新能源的是(填字母序号)。

水是一种重要的资源。
(1)电解水实验揭示了水的组成。下图实验中得到氧气的试管是(填"1"或"2")。

(2)自来水厂净水过程中用到活性炭,其作用是。
(3)海水淡化可缓解淡水资源匮乏的问题。下图为太阳能海水淡化装置示意图。

①水变成水蒸气的过程中,不发生变化的是(填字母序号)。
A.分子质量 B.分子种类 C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数会(填"变大"、"变小"或"不变")
亮亮做家务时接触到下列用品。
| 用品 |
脱氧剂 |
洁厕灵 |
炉灶清洁剂 |
| 有效成分 |
还原铁粉 |
盐酸 |
氢氧化钠 |
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是
(4)做完家务,他用
泡腾片冲了一杯饮料。下列
泡腾片的主要成分中,属于有机物的是
A.维生素C( )
)
B.柠檬酸( )
)
C.碳酸氢钠( )
)
阅读下面科普短文(原文作者:段翰英等)。
我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐[如亚硝酸钠(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)和氯化物(如
)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?含量有多少?含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。

用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素
,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由
(2)亚硝酸钠能与盐酸反应,该反应属于基本反应类型中的
(3)室温下,用芹菜制作的泡菜,最佳食用时间是
A.泡制2-3天 B.泡制5-6天 C.泡制12天后
(4)下列关于制作泡菜的说法中,合理的是
A.最好加入一些姜汁
B.最好在较低温度下泡制
C.最好加入一些富含维生素
的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(5)请你为喜欢吃泡菜的人提一条食用泡菜的建议:
生物浸出技术在金属冶炼中应用广泛。嗜热细菌在65-80℃酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分
)产生硫酸盐,进而生产铜和绿矾,主要流程如下:

(1)分离出矿渣的操作是。
(2)若试剂b为
粉,反应①的化学方程式为。
(3)氢氧化铁与试剂a发生中和反应,反应②的化学方程式为。
某烟气脱硫的工艺不仅能消除 ,还能将其转化为石膏(
,还能将其转化为石膏( )等产品,实现"变废为宝"。主要物质转化关系如下:
)等产品,实现"变废为宝"。主要物质转化关系如下:

(1)设备1中,通过喷淋水脱去烟气中的 ,该反应的化学方程式为。
,该反应的化学方程式为。
(2)设备2中,加入 的目的是将
的目的是将 转化为。
转化为。
(3)设备3中,反应前后化合价发生改变的元素是。
甲、乙、丙、丁4种常见物质,由氢、碳、氧、钠、钙5种元素中的2-3种组成。
(1)甲俗称纯碱,其化学式为。
(2)乙是一种氧化物,遇水放出大量的热,乙的名称是。
(3)丙与氧气在点燃条件下反应,其微观示意图如下,请在方框中补全相应微粒的图示。

(4)如图所示(夹持仪器略去, 、
、 均关闭),打开
均关闭),打开 ,待液体全部流下,立即关闭
,待液体全部流下,立即关闭 ,观察到产生大量气泡,且烧杯中丁的溶液变浑浊。充分反应后,打开
,观察到产生大量气泡,且烧杯中丁的溶液变浑浊。充分反应后,打开 和
和 ,使液体全部流入锥形瓶,瓶中无明显现象。
,使液体全部流入锥形瓶,瓶中无明显现象。

①用化学方程式表示烧杯中溶液变浑浊的原因。
②取反应后锥形瓶中的溶液,测得 ,则该溶液中含有的溶质除HCl外,还有。
,则该溶液中含有的溶质除HCl外,还有。
实验小组同学做了如下实验。

(1)
中反应的化学方程式为
(2)
中现象是声带涌出柱状的泡沫,可形象地称为"大象牙膏",其原理主要是
在某些催化剂作用下迅速分解产生水和氧气。反应的化学方程式为
依据下图进行实验(夹持仪器略去)。实验过程:
①通入
,点燃酒精灯,一段时间后,
、
中均无明显现象;
②熄灭酒精灯,立即改通
,
中无明显现象,
中红磷燃烧。

(1)实验过程②中,红磷燃烧的化学方程式为。
(2)实验过程②中,对比
、
中的实验现象,可知可燃物燃烧的条件之一是。
(3)实验过程中,能说明可燃物燃烧需要氧气的实验是。
的硼酸溶液可用于清洗皮肤的小面积创伤。现配制
质量分数为
的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数。

(2)量取水的体积:用量筒取 水( )。
(3)溶解:用到的玻璃仪器是。
(4)装瓶、贴标签:在下图的标签中填上相应的内容。

利用下图装置进行实验。实验前
、
、
均已关闭。
| 内容 装置 |
【实验1】制备气体 |
【实验2】测定气体含量 |
 |
Ⅰ.打开
,用注射器向盛有锌粒的A中注入稀硫酸,直至液面浸没下端导管口 Ⅱ.在 上方导管口收集气体 |
Ⅰ.A(容积
)中为用排空气法收集的
,B中装满水。用注射器向A中注入15mL
溶液(足量),充分反应 Ⅱ.打开 和 |
(1)检查装置气密性:保持
关闭,打开
、
,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,说明装置在左侧气密性良好的现象是
(2)实验1中,锌与稀硫酸反应的化学方程式为
(3)实验2中,当B中液面不再变化时,测得B中减少了160mL水,则A中
的体积分数约为
众所周知,酚酞溶液遇
溶液变红。但是,在分组实验中(如图所示),出现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物。

【提出问题】分组实验中,出现意想不到的现象的原因是什么呢?
【查阅资料】酚酞溶液由酚酞固体溶于酒精配制而成。
【猜想与假设】
Ⅰ.红色褪去,与
溶液和空气中的
反应有关。
Ⅱ.红色褪去,与
溶液的浓度有关。
Ⅲ.出现白色浑浊物,与酚酞溶液的浓度有关。
【进行实验】
| 实验 |
实验操作 |
实验现象 |
|
| 1 |
向盛有2 mL =
溶液的试管中滴加5滴0.5%的酚酞溶液 |
溶液变红 |
|
| 2 |
 |
1号试管0.1min红色褪去 2号试管5min红色褪去 3号试管30min红色明显变浅 4号试管120min红色无明显变化 |
|
| 3 |
取3支试管,分别加入2 mL水,…… |
酚酞溶液浓度/% |
浑浊程度 |
| 5 |
大量浑浊物 |
||
| 2 |
少量浑浊物 |
||
| 0.5 | 无浑浊物 |
【解释与结论】
(1)
与
反应的化学方程式为
(2)实验1的现象表明,猜想与假设1
(3)由实验2得出结论:出现"溶液变红后褪色"现象的原因是
(4)实验3的操作步骤:取3支试管,分别加入2ml水,
【反思与评价】
(5)依据现有实验,为了确保红色不变,若酚酞溶液浓度为0.5%,建议选用
溶液的浓度为
(6)有同学认为,仅通过实验3得出"猜想与假设Ⅲ成立"证据不足,理由是




 粤公网安备 44130202000953号
粤公网安备 44130202000953号