配制100g质量分数为15%的KNO3溶液,需要水 毫升(水的密度为1g/cm3)。在配制过程中量取水的体积时仰视读数,则所配制溶液的溶质质量分数 (选填“偏大”、“不变”、“偏小)。
防范新冠疫情,需要我们"戴口罩,勤洗手,勤消毒,勤通风"。
(1)医用口罩的核心材料是聚丙烯制成的熔喷布,聚丙烯属于 (填"金属材料"或"有机合成材料");
(2)请从微现角度解释:教室进行消杀后室内充满消毒液气味的原因 ;
(3)某消毒液稀释后pH=6,则稀释前其pH (填">"、"="或"<")6;
(4)在疫情期间要学会正确的洗手方法,沾有油污的手,可使用洗洁精清洗,洗洁精的作用是 ;
(5)"84消毒液"的主要成分是次氯酸钠(NaClO)。其中氯元素的化合价是 ,制取NaClO的原理是2NaOH+Cl 2═NaClO+X+H 2O,其中X的化学式是 ;
(6)某校要配制100kg溶质质量分数为0.2%的过氧乙酸消毒液,需要10%的过氧乙酸溶液 kg,所需水的质量为 kg。
某化学课外兴趣小组欲配制80g质量分数为12%的氢氧化钠溶液来制作“叶脉书签”。
(1)需要氢氧化钠固体的质量为 g。
(2)称量时,氢氧化钠固体应放在 (填“滤纸”或“烧杯”)中。
(3)下列说法或操作正确的是 (填字母序号)。
A、配制该溶液时所需的玻璃仪器中不包括玻璃棒
B、用量程为100mL的量筒量取所需要的水
C、将称量好的固体倒入装有水的量筒中溶解
(4)在量取水的体积时,若采用仰视的方法读数,则所配制的氢氧化钠溶液中溶质的质量分数将 (填“偏大”或“偏小”)。
(5)某同学用蒸馏水润湿了的pH试纸来测定配制好的溶液的pH值时,他测得的结果会 (填“偏大”、偏小”或“不变”)。
(6)该兴趣小组的同学提出还可以用配制好的氢氧化钠溶液和稀盐酸进行中和反应实验,具体操作如图:

在烧杯中加入10mL的氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液呈 色。接着加入一定量的稀盐酸,用玻璃棒搅拌后发现溶液为无色,此时 (填“能”或“不能”)得出两者恰好中和的结论。以下操作及实验现象能证明加入的盐酸为过量的是 (填字母序号)。
A、加入少量铁粉,无明显现象
B、滴加紫色石蕊溶液,搅拌后溶液变蓝
C、加入碳酸钠溶液,产生气泡
实验是学习化学的重要手段,请结合下列实验回答相应问题。
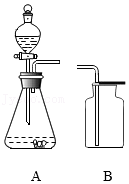
(1)实验室利用如图装置A制氧气,化学方程式为 。用装置B收集气体,气体应该具有的性质是 。
(2)如图是配制一定溶质质量分数的氯化钠溶液的操作步骤,其正确操作顺序是 ;指出图中错误的操作步骤并加以改正: 。
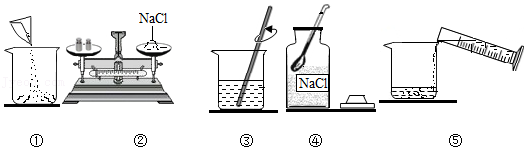
(3)配制过程中,假设其他步骤都正确,用量筒量取水的体积时仰视读数,所配溶液溶质质量分数会 (填“偏大”、“偏小”或“不变”)。
某同学配制25g 3%的NaCl溶液,整个操作过程如图所示。

回答下列问题:
(1)配制溶液的正确操作顺序为 (填序号),其中操作错误的是 (填序号)
(2)用量筒量取液体时,读数时视线要与量筒内 保持水平。
(3)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是 。
配制50g质量分数为6%的氯化钠溶液,不需要用到的仪器是( )
A.烧杯B.量筒C.铁架台D.玻璃棒
规范操作是实验成功的前提。请按要求回答下列问题:
(1)“粗盐中难溶性杂质的去除”实验中,玻璃棒的作用有:转移、 。
(2)“一定溶质质量分数溶液的配制”实验的基本步骤包括:计算、 、装瓶保存。
(3)利用pH试纸检验溶液的酸碱性,正确的操作应是 。
农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如图所示。下列说法不正确的是( )

| A. |
实验操作顺序为④②①⑤③ |
| B. |
②中需称量NaCl的质量为16.0g |
| C. |
选用100mL量筒量取所需水的体积 |
| D. |
用量筒量取水时仰视读数所得溶液的溶质质量分数偏大 |
在“一定溶质质量分数的氯化钠溶液配制”实验活动中,下列操作正确的是( )
A. 取药B.
取药B. 称量
称量
C. 量取D.
量取D. 溶解
溶解
请回答下列问题:
(1)现提供下列实验仪器和装置:

①实验室用高锰酸钾制氧气,反应的化学方程式为 ;该实验可选用F和 (填序号)组装成排水法收集氧气的装置;还可用 方法收集氧气。
②实验室用锌粒和稀硫酸制氢气,反应的化学方程式为 ;为达到控制反应生和停止的目的,发生装置应选择A和 (填序号);为除去氢气中的水分,用B、C组装成一套装置,向B中加入液体试剂 ,气体通过此装置达到目的。
(2)实验室用氯化钠固体配制50g溶质质量分数为15%的氯化钠溶液。
①量取水,应选择 (填“10mL”或“50mL”)量筒。
②下列操作导致氯化钠溶液的溶质质量分数偏大的是 (填序号)。
a.取用潮湿的氯化钠
b.称量时,所用砝码表面已生锈
c.量取水时仰视读数
d.转移溶液后,烧杯内还有少量氯化钠固体
2021年“世界水日”的主题为“珍惜水、爱护水”。
(1)2021年5月10日,“南水北调东线北延应急供水工程”启动向天津等地供水,以缓解我市可利用淡水资源 的现状。
(2)下列有关保护水资源的说法正确的是 (填序号)。
A.生活污水可直接排放
B.工业上对污染的水体作处理使之符合排放标准后再排放
C.农药、化肥的施用会造成水体污染,应该禁止施用
(3)如图是利用海水提取粗盐的过程。

根据海水晒盐的原理,下列说法正确的是 (填序号)。
A.进入贮水池中的海水,氯化钠的质量逐渐减少
B.在蒸发池中,海水中氯化钠的质量逐渐增加
C.析出晶体后,母液中的氯化钠溶液达到饱和
(4)某同学配制50g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为 g。
②配制过程有以下步骤:a.称量及量取b.计算c.溶解d.装瓶贴标签,正确顺序是
(填序号)。
A.bcad
B.bacd
③将50g溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水 g。
(5)为研究水的组成,某同学进行了电解水实验。
①电解水的化学方程式为 ;
②电解水的实验证明水是由 元素组成的。
氯化钠是生产、生活中的一种重要化合物,应用很广泛。
Ⅰ.图甲和图乙分别是钠原子和氯原子的原子结构示意图。

(1)图甲中的x= 。
(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有 个电子的相对稳定的氯离子,氯离子用化学符号表示为 。
Ⅱ.如表是氯化钠在不同温度下的溶解度数据。
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
(1)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于
(填“饱和”或“不饱和”)溶液。
(2)医用盐水(溶质为NaCl)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其中含NaCl的质量为 g。
(3)学生化学实验活动之一:配制50g质量分数为6%的氯化钠溶液,该实验需要的仪器有药匙、托盘天平、玻璃棒、胶头滴管、 (从下列图中选择写出名称)。

Ⅲ.工业上常用电解饱和食盐水的方法来制取氢氧化钠、氯气和氢气,其化学反应方程式可表示为:xNaCl+yH2O zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
(填数字)。
某同学配制100g质量分数为11%的葡萄糖溶液,下列操作会导致所配溶液浓度偏高的是( )
A.用托盘天平称葡萄糖时,砝码放在左盘
B.转移葡萄糖时,纸上有少量残留
C.用量筒量取水时,俯视液面
D.配好溶液装入试剂瓶时,有少量洒出
配制100g质量分数为16%的Na2CO3溶液,用于演示灭火器原理。回答下列问题。
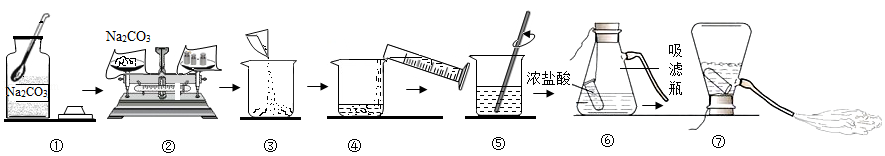
(1)计算Na2CO3的质量为 g,称量Na2CO3的仪器名称是 。
(2)20℃时,Na2CO3的溶解度为21.5g,⑤中的溶液 (填“是”或“不是”)该物质的饱和溶液。
(3)将烧杯中溶液倒入吸滤瓶的操作是 ,从橡胶管喷出大量液体的原因是 。
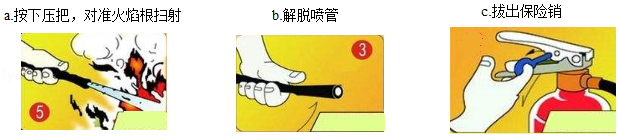
(4)酒精(C2H5OH)可作燃料,在空气中完全燃烧的化学方程式是 。酒精燃烧失火,可用干粉灭火器灭火。NaHCO3是干粉的主要成分,俗称是 。用干粉灭火器灭火的正确操作顺序是 → → (填序号)。