农业废弃物是指农业生产过程中废弃的有机物,如秸秆、蔗渣等.
(1)农业废弃物经发酵处理可获得沼气(主要成分为甲烷).甲烷完全燃烧的化学方程式为 .
(2)闽籍科学家张俐娜发明了一种快速溶解农业废弃物的“神奇溶剂”.该“神奇溶剂”中氢氧化钠、尿素和水的质量比为7:12:81.
①“神奇溶剂”是一种溶液,其溶质有 .
②某次生产需用到100kg“神奇溶剂”.现仅用氢氧化钠溶液和尿素来配制,所用的氢氧化钠溶液的溶质质量分数为 (列出计算式即可).
③利用该“神奇溶剂”溶解农业废弃物生产的新型纤维素膜,在土壤中能完全降解.利用此膜替代普通塑料,可缓解的环境问题是 (写一点)
化学兴趣小组在老师的帮助下围绕燃烧实验开展相关研究。
探究一:氢气的燃烧实验

(1)用锌和稀硫酸制取氢气,从图1中选择仪器组装一套随开随停的发生装置,所需仪器为 (填编号);仪器B的名称是 。
(2)按图2操作研究氢气的燃烧实验,需用试管收集不同体积比的氢气与空气的混合物,现用(1)中组装的正确装置制取氢气,如何用试管(假设试管容积为10mL)收集氢气与空气体积比为4:1的混合气体,写出其操作方法: 。
(3)用不同体积比的混合气体做氢气的燃烧实验,结果如表:
| 序号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
| 氢气与空气体积比 |
9:1 |
8:2 |
7:3 |
5:5 |
3:7 |
1:9 |
0.5:9.5 |
| 点燃现象 |
安静 燃烧 |
安静 燃烧 |
弱的 爆鸣声 |
强的 爆鸣声 |
强的 爆鸣声 |
弱的 爆鸣声 |
不燃烧 不爆鸣 |
分析上表信息,你对燃烧或燃烧条件的新认识是 。
探究二:可燃性粉尘燃烧剧烈程度的影响因素
(4)用如图3装置研究某可燃性粉尘颗粒大小对燃烧剧烈程度的影响,燃烧剧烈程度用燃烧产生的最大压力衡量,容器内壁的传感器可测出燃烧产生的最大压力。
①实验过程中需改变的实验条件是 ,不能改变的是 、 、 (仅列三种);
②实验测得可燃性粉尘颗粒大小与燃烧产生的最大压力的关系如图4所示,其原因是 。

(5)兴趣小组另测得可燃性粉尘浓度与燃烧产生的最大压力的关系如图5所示,结合图5信息,提出防止可燃性粉尘发生燃烧的合理建议:①禁止烟火;② 。
实验室常用无水醋酸钠(CH 3COONa)固体和碱石灰混合加热的方法制取甲烷。

(1)写出图A中标有序号的仪器名称:① ,② 。
(2)甲烷属于 (填"有机"或"无机")化合物。
(3)实验室制取甲烷应选择的发生装置是 (填字母)。用C装置收集甲烷,发生装置的导管口应与 (填"a"或"b")端相连。
(4)点燃甲烷前需先检验 甲烷完全燃烧的化学方程式是 。
(5)用上述方法收集8g甲烷CH 3COONa+NaOH Na 2CO 3+CH 4↑)理论上至少需要无水醋酸钠的质量是多少?
如图是硫在氧气中燃烧的实验改装装置:
(1)写出分解过氧化氢制取氧气的化学方程式: 。
(2)硫在氧气中燃烧的现象是: 。
(3)本实验中电烙铁的作用是: 。
(4)配制50g溶质质量分数为5%的氢氧化钠溶液,需要氢氧化钠的质量 。
(5)本实验具有的优点是: 。(写一点即可)

化学是一门以实验为基础的学科
[实验一]常见气体的制取

(1)仪器a的名称 。
(2)实验室制取二氧化碳气体,发生和收集装置分别选用 和 (填字母),反应的化学方程式为 。
(3)实验室用A装置制取氧气,从燃烧条件分析,加热过程中试管内的棉花没有燃烧的原因是 。
[实验二]对比归纳是学习化学的重要方法

(4)实验A:观察到图2②中反应更剧烈,可知影响硫燃烧剧烈程度的因素是 。
(5)实验B:观察到图3 ④中固体消失,③中固体几乎不溶,可知影响物质溶解性的因素是 。
化学与生产、生活息息相关。
(1)水稻生长初期需要施氮肥,下列属于氮肥的是 。
A.K 2CO 3 B.(NH 4) 2SO 4 C.Ca 3(PO 4) 2 D.CO(NH 2) 2
(2)农业上常用溶质质量分数为16%的氯化钠溶液选种,现要配制100Kg这种溶液,需要 Kg氯化钠,配制该溶液的主要步骤有:①计算 ②称量 ③量取 ④ 。
(3)自行车是"绿色出行"的交通工具,为防止其链条生锈常采用的方法是 ;自行车支架使用的铝合金是 材料(填"金属"或"合成"),铝离子结构示意图如图 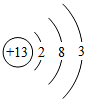 ,铝在化学反应中易 (填"得"或"失")电子,她的离子符号为 。
,铝在化学反应中易 (填"得"或"失")电子,她的离子符号为 。
泡菜是常见的腌制食品,因含亚硝酸盐(如NaNO2)而引发人们的关注。根据要求回答问题:
Ⅰ.腌制泡菜时,蔬菜中的NaNO3转化为NaNO2.食用泡菜时,NaNO2与胃酸反应生成HNO2.HNO2不稳定,转化为某氮氧化物(常温下为红棕色气体)进入血液而中毒。
(1)NaNO2与胃酸(主要成分为盐酸)发生复分解反应,该反应的化学方程式为 。
(2)图1为泡菜生产和食用时涉及的四种含氮物质的类别及氮元素化合价关系图。其中,L的化学式为 。
(3)为检验某无色溶液是NaNO2还是NaCl,完成实验方案。
选取的试剂 |
实验现象 |
实验结论 |
|
|
该溶液为NaNO2溶液 |
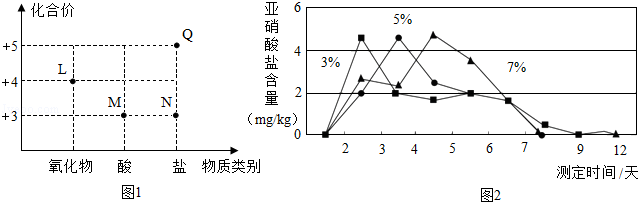
Ⅱ.室温下,用3%、5%和7%的食盐水浸泡蔬菜,浸泡不同时间获得的泡菜中亚硝酸盐的含量如图2所示。若往食盐水中添加少量维生素C,泡菜中亚硝酸盐含量明显降低。
(4)配制3%的NaCl溶液2000.0g,需用托盘天平称取 g的NaCl。
(5)食盐水的溶质质量分数越大,泡菜中亚硝酸盐含量最大值出现得 (填“越早”、“越迟”或“无影响”)。
Ⅲ.实际上,只要合理制作、食用泡菜,将有效避免(或降低)对人体的危害。
(6)列举一条避免(或降低)食用泡菜对人体危害的措施。
答: 。
小明用锌粒和稀硫酸制取氢气,选用右图部分装置开展实验.根据要求回答问题:
(1)写出标号仪器的名称:
a ;b .
(2)实验过程中,制取、收集氢气的装置是 和 .
(3)制取氢气的化学方程式是 .
(4)实验时产生氢气很慢.小明根据老师建议,往制H2装置中滴入蓝色硫酸铜溶液,果然快速放出氢气.硫酸铜是否作催化剂?探究如下:往小烧杯中加入约20mL稀硫酸和约1mL硫酸铜溶液,再加入黄豆粒大的锌粒.反应停止时,溶液褪至无色、有红色物质生成.
①产生红色物质的原因 (填化学方程式);
②由上述实验可知,硫酸铜不是催化剂.理由是 .

豆腐是客家美食之一.豆腐制作过程如下:
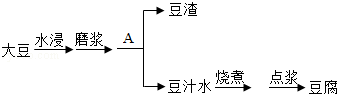
根据要求回答问题:
(1)豆浆 (填"是"或者"不是")溶液.
(2)"点浆"是使用MgCl 2、CaSO 4等凝固剂使豆浆凝固的过程.这些凝固剂的水溶液能导电,说明它们在水中溶解时能生成 .
(3)操作A为 .在实验室进行此操作,用到的玻璃仪器有烧杯、玻璃棒和 .
(4)食用豆腐有益于补充人体所需的蛋白质、预防骨质疏松症等.
①蛋白质对生命活动的重要意义是 ;
②豆腐能够预防骨质疏松症,说明豆腐含较丰富的 (填元素名称).
(5)豆腐中某成分会促进人体内碘的排泄.因此,食用豆腐时,可和 (填一种食物)搭配,解决食用豆腐可能引发的碘流失.
根据下列实验要求回答问题。

(1)写出图中仪器①、②的名称:① ,② 。
(2)实验室制取二氧化碳的化学方程式为 ,制取装置为 (填标号,下同)和 组合。检验二氧化碳的原理为 (用化学方程式表示)。
(3)实验室用高锰酸钾制取氧气的化学方程式为 ,可选用的发生装置为 (填标号)。
(4)若用水将图2所示的氧气从瓶内排出,水须从 (填"a"或"b")端导管口通入。
(5)实验室用碘化氢溶液测定过氧化氢溶液中溶质的质量分数,反应原理:H 2O 2+HI═2H 2O+I 2↓.取25.0g过氧化氢溶液,加入足量的碘化氢溶液,充分反应后生成12.7g碘。根据化学方程式计算该过氧化氢溶液中溶质的质量分数。
实验室用如图装置制取CO2。
(1)反应的化学方程式为 。
(2)用向上排空气法收集CO2的原因是 。

请从A或B两题中任选一个作答,若两题均作答,按35﹣A计分.
| A用浓硫酸配制100g 9.8%的稀硫酸 |
B粗盐中难溶性杂质的去除 |
| (1)实验需要5.4mL浓硫酸和90mL水.量取两种液体用到的仪器有 (填序号). (2)稀释时,需将浓硫酸缓慢倒入水中,并不断进行搅拌,其原因是 . |
(1)过滤需要用到的仪器有 (填序号). (2)蒸发过程中,需不断进行搅拌,其原因是 . |
| 可供选择的主要仪器: ①试管 ②烧杯 ③蒸发皿 ④托盘天平 ⑤10mL量筒 ⑥100mL量筒 ⑦药匙 ⑧胶头滴管 ⑨漏斗 ⑩酒精灯⑪铁架台⑫玻璃棒 |
|
| |
|
Ba(NO 3) 2可用于生产信号弹、炸药等。利用钡泥(主要含有BaCO 3、BaSO 3、Fe 2O 3)可制取Ba(NO 3) 2,其部分流程如图:
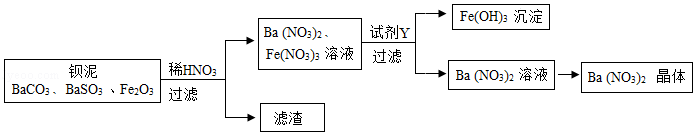
(1)Ba(NO 3) 2中钡元素的化合价为 ;流程中所涉及的氧化物是 (填1种即可)。
(2)BaCO 3与稀HNO 3反应的反应类型是 ;写出Fe 2O 3与稀HNO 3反应的化学方程式: 。
(3)试剂Y为 (填序号)。
①BaCl 2溶液 ②Ba(OH) 2溶液 ③NaOH溶液
(4)从Ba(NO 3) 2溶液中析出Ba(NO 3) 2晶体的方法是 。
如图是实验室中常见装置,回答下列问题。

(1)仪器a的名称是 。
(2)用装置A进行实验时,首先应 (填序号)。
①加药品
②加热
③检查装置气密性
(3)用A装置制取气体的不足之处是 。
(4)若要收集干燥的CO 2,可将含有水蒸气的CO 2从装置B的 (填"m"或"n")端导入,试剂X是 ;再用装置 (填"C"或"D"或"E")收集。
(5)向集满CO 2的集气瓶中加入澄清石灰水,反应的化学方程式为 。