(本题共12分)维生素B6(Vitamin B6)可用于防治妊娠呕吐和放射病呕吐。维生素B6又称吡哆素,包括吡哆醇、吡哆醛及吡哆胺(分别是下图中X、Y、Z中的某一种)。

47.PLP是由 (填:吡哆醇、吡哆醛、吡哆胺)与某无机物W发生酯化而制得。制备PMP时也使用了无机物W,则该无机物的名称是 。
反应条件:Z→X: (不考虑其他官能团的副反应)。
已知:乙基(-C2H5)常简写为-Et。Z的盐酸盐G的合成路线如下图,回答48-51题:
48.结构简式:D 、F 。
49.步骤①的目的是: ;
步骤④中碳酸钠的作用是: 。
50.写出一种满足下列条件的E的同分异构体K的结构简式: 。
条件:①K分子中氮原子与苯环直接相连且直接连接3个碳原子;
②1mol K能与4mol Na2CO3反应。
51.写出R转化为B和C的化学方程式: 。
(本题共10分)碳碳双键的性质较为活泼,在一定条件下会发生特殊的反应,例如: 。根据下列转化流程,回答43-46题:
。根据下列转化流程,回答43-46题:
43.反应条件:② ,③ 。
44.反应类型:① ,⑤ 。
45.结构简式:X 。
46.写出实验室由B的芳香烃的同分异构体的同系物制备 的合成路线: 。
的合成路线: 。
(合成路线常用的表示方式为: )。
)。
【化学选修5-有机化学基础】化合物G是一种医药中间体,常用于制备抗凝血药.可以通过下图所示的路线合成:
请回答下列问题:
(1)B→C的转化所加的试剂可能是_______C+E→F的反应类型是________。
(2)有关G的下列说法正确的是___________。
a.属于芳香烃
b.可以发生水解、加成、氧化、酯化等反应
c.能与FeCl3溶液发生显色反应
d.1molG最多可以跟4molH2反应
(3)E的结构简式:___________________。
(4)F与足量NaOH浴液充分反应的化学方程式为 。
(5)E的同分异构体中,既能发生水解反应,又能与FeCl3溶液能发生显色反应的还有____种,其中苯环上有两种不同化学环境的氢原子的是 (写出其中一种的结构简式)。
(6)已经氯苯用10%到15%的氢氧化钠溶液在360到390℃、28-30MPa条件下水解再酸化,
可制取苯酚,而酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯( )是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。
)是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。
注:合成路线的书写格式参加如下示例流程图:
【化学---有机化学基础】化合物G是一种医药中间体,常用于制备抗凝血药。可以通过下图所示的路线合成:
已知:RCOOH RCOCl;D与FeCl3溶液能发生显色。
RCOCl;D与FeCl3溶液能发生显色。
(1)B→C的转化所加的试剂可能是 ,C+E→F的反应类型是 。
(2)有关G的下列说法正确的是 。
| A.属于芳香烃 |
| B.能与FeCl3溶液发生显色反应 |
| C.可以发生水解、加成、氧化、酯化等反应 |
| D.1mol G最多可以跟4 mol H2反应 |
(3)E的结构简式为 。
(4)F与足量NaOH溶液充分反应的化学方程式为 。
(5)写出同时满足下列条件的E的同分异构体的结构简式 。
①发生水解反应
②与FeCl3溶液能发生显色反应
③苯环上有两种不同化学环境的氢原子
A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如图所示的转化关系:
(1)若A为非金属单质,C、D的相对分子质量相差16。0.05 mol·L—1 E溶液中只有3种离子,且在25℃时,溶液中的c(H+)/c(OH—)=1012。
①写出E→C的一个化学方程式___________________________;
②在A→C的反应中,每转移1 mol e— 就会放热 143.5 kJ,该反应的热化学方程式为_________。
(2)若A为金属单质,B、C均属于盐类,D是一种白色沉淀。
①若B水溶液呈酸性,C水溶液呈碱性,则B溶液呈酸性的原因是______________(用离子方程式表示);
②若B溶液呈黄色,与硫氰化钾溶液混合后显红色,E是一种不溶性碱。B→C的离子方程式为___________。D→E的化学方程式为______________________。选用氢碘酸与可E反应实现E→C的转化,该反应的离子方程式为________________。
(3)若A~E均为含有Y元素的化合物,A是淡黄色固体,等物质的量浓度B、C两溶液,其中C溶液的pH较小。电解D的水溶液是最重要的工业生产之一,D→E→C是工业侯氏制碱中的主要过程。则等浓度、等体积混合的C、E两溶液中所有离子浓度的大小关系为________________。
化合物H可用以下路线合成:
已知:
请回答下列问题:
(1)标准状况下11.2L烃A在氧气中充分燃烧可以生成88gCO2和45gH2O,且A分子结构中有3个甲基,则A的结构简式为 ;
(2)B和C均为一氯代烃,D的名称(系统命名)为 ;
(3)在催化剂存在下1molF与2molH2反应,生成3—苯基—1—丙醇。F的结构简式是 ;
(4)反应①的反应类型是 ;
(5)反应②的化学方程式为 ;
(6)写出所有与G具有相同官能团的芳香类同分异构体的结构简式 。
已知:①R— —
—
②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
以下是用苯作原料制备一系列化合物的转化关系图:
(1)A转化为B的化学方程式是_______________________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①、②物质的结构简式:
①________________________,②____________________________。
(3)B在苯环上的二氯代物有 种同分异构体。
(4)有机物 的所有原子 (填“是”或“不是”)在同一平面上。
的所有原子 (填“是”或“不是”)在同一平面上。
下图是由短周期元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。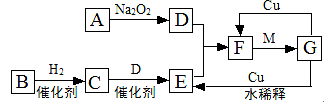
(1)物质G的化学式为 ;物质F的名称是 。
(2)①A→D的化学方程式为 ;
②C→E的化学方程式为 。
(3)G→E的离子方程式为 。
各物质的转换关系如图,其中A为不饱和烃:
(1)A、E、F2的结构简式分别为:
(2)图中②、④、⑤的反应类型为: 、 、
(3)写出图中⑤、⑧的反应方程式:
A、B、C、D为为中学常见单质。通常状况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间转化关系如下图所示(其中某些反应条件和部分反应物已略去)。
请回答下列问题:
(1)写出下列物质的化学式:A______、X______。
(2)在反应;①~⑦中,属于氧化还原反应的有____个;反应⑥说明D溶液中含有___离子。
(3)反应④的离子方程式是__________。
(4)反应⑦的化学方程式是__________。
(5)检验D的溶液中是否含有G离子的方法是_________。
(6)除去D溶液中混有的少量G的方法是_____________。
【原创】(10分)如图1所示是某些物质的转化关系图(个别小分子产物可能没有标出)。

已知:
Ⅰ.A、B、C是三种常见的气态含碳化合物,A、B的相对分子质量均为28,C的相对分子质量略小于A。
Ⅱ.化合物D的比例模型如图2所示;D完全燃烧时,消耗的氧气与生成的CO2的体积比为1:1。
Ⅲ.硫酸氢乙酯水解得E与硫酸,从A经硫酸氢乙酯至E的反应中,硫酸实际起到了催化剂的作用。
Ⅳ.E与F反应,得一种有浓郁香味的油状液体G,E与D反应得无色液体H,在反应②、③中,参与反应的官能团完全相同。
请按要求回答下列问题:
(1)化合物D所含官能团的名称是 ,化合物C的结构简式为 。
(2)反应①的反应类型是 ,化合物A与F在一定条件下也可发生类似①的反应,其化学方程式为 。
(3)化合物H可进一步聚合成某种柔软且透明的高分子化合物,写出其化学反应方程式 。
【原创】(10分)化合物I是一种药物合成中间体,与I相关的反应如下:

根据以上信息回答下列问题。
(1)写出A中所含官能团的名称 ;B→C的反应类型是 。
(2)写出D→E的化学方程式 。
(3)工业上用B与O2在催化剂条件下生产环氧乙烷,化学反应方程式为 。
(4)实验室取1.96g G完全燃烧,将燃烧产物通过碱石灰,碱石灰质量增加4.68g;若将燃烧产物通过浓硫酸,浓硫酸的质量增加0.72g。G的分子式是 。
(5)已知化合物I分子式中碳原子数为13,则化合物H的结构简式是 。
【命题立意】考查学生对有机化学基础知识的掌握情况,重点考查有机物结构(官能团)与性质的关系、各类衍生物间的转化关系及有机反应类型、化学方程式、有机物分子式的确定。
【改编】(10分)醇酸树脂是一种成膜性很好的树脂,下面是一种醇酸树脂的合成线路:

(1)B中含有的官能团的名称是_________________________。
(2)反应①、③的有机反应类型分别是 、 。
(3)下列说法正确的是__________(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2mol Ag
b.F能与NaHCO3反应产生CO2
c.检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液
(4)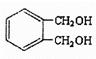 的同分异构体中同时符合下列条件的芳香族化合物共有 种。
的同分异构体中同时符合下列条件的芳香族化合物共有 种。
a.能发生消去反应
b.能与过量浓溴水反应生成白色沉淀
(5)写出反应⑤的化学方程式________________________________________________。
【原创】(18分)甲、乙、丙是常见的三种物质,它们之间有如图所示的转化关系。根据要求回答下列问题:
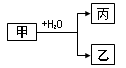
I.已知:甲是由两种短周期元素组成的化合物,丙的水溶液显碱性。
(1)若构成甲的阴、阳离子个数比为2:3,丙是气体。则构成甲的阴、阳离子半径大小关系为 (用具体的微粒表示)。
(2)若乙是O2,则甲的一种重要用途是 ;产物丙与Cl2按2:1(物质的量)反应得到丁溶液,丁溶液中阴离子浓度从大到小的顺序是 。
Ⅱ.一种灰白色固体粉末X是由两种常见元素组成的化合物,其中金属元素与另一元素的质量比为14:l。在一定条件下X可发生如下图的转化关系,有的反应标出全部产物,有的反应标出部分产物。已知P为混合气体,R是无色无味能使澄清石灰水变浑浊的气体,C为红褐色物质,M为常见金属单质,Q为常见非金属单质。请回答下列问题:

(1)X的化学式为______________;R的电子式为_________________。
(2)写出气体P的组成 。
(3)写出D→G的离子反应方程式 。
(4)M与钛构成的合金是一种常用的不锈钢材料,某同学在探究该合金的性质时,往含有TiO2+、M3+溶液中加入M至溶液显紫色,该过程中发生的反应有:
①2TiO2+(无色)+Fe+4H+==2Ti3+(紫色)+Fe2++2H2O
②Ti3+(紫色)+Fe3++H2O ="=" TiO2+(无色)+Fe2++2H+
③ 。
请写出③可能的反应方程式 。
(5)人们对X的结构研究后发现其金属元素有0价、+2价两种化合价,写出X与稀硫酸反应的化学方程式 。
(6)聚合硫酸M是一种常见的净水剂,化学式为:[M2(OH)n (SO4)3- ]m (n>2,m≤10),其制备可由硫酸M经水解后再聚合得到,其中聚合反应的原理为m[M2(OH)n(SO4)3-
]m (n>2,m≤10),其制备可由硫酸M经水解后再聚合得到,其中聚合反应的原理为m[M2(OH)n(SO4)3- ]
]  [M2(OH)n(SO4)3-
[M2(OH)n(SO4)3- ]m,则写出硫酸M水解的化学方程式为 。
]m,则写出硫酸M水解的化学方程式为 。
【命题立意】本题综合考查元素及其化合物的知识,融入信息型化学方程式的书写,旨在考查考生知识迁移能力以及应用化学原理解决实际问题的能力。
(10分)某科研小组利用石油分馏产品经下列路线,合成一种新型香料。

已知X分子中碳氢质量比为24∶5,A、E都是X的裂解产物,且二者互为同系物,D与饱和NaHCO3溶液反应产生气体。
信息提示:卤代烃在强碱水溶液中发生水解(取代)反应生成醇。如:
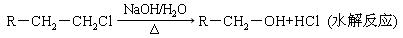
(1)X分子为直链结构,X的名称为 ;C中官能团的名称为 。
(2)①~⑥的反应中,下列反应类型存在且数目由多到少的是 。(用字母和“>”写出)
A.加成反应 B.加聚反应 C.取代反应 D.氧化反应
(3)B与D在浓硫酸作用下,生成甲,则与甲同类别的同分异构体的有 种(不包括甲)
(4)写出⑥的化学反应方程式 。
(5)E可能发生下列选项中的某种反应,写出能反应的化学方程式 。
A.皂化反应 B.与乙酸的酯化反应
C.加聚反应 D.与银氨溶液的银镜反应