陕西省西安地区八校高三下学期联考三理综化学试卷
有两组物质:①组CH4、聚乙烯、邻二甲苯 ②组2-丁烯、乙炔、苯乙烯下列有关上述有机物说法正确的是
| A.①组物质都不能使酸性高锰酸钾褪色,②组物质都能使酸性高锰酸钾褪色 |
| B.①组物质都不能使溴的四氯化碳褪色,②组物质都能使溴的四氯化碳褪色 |
| C.②组物质所有原子可以在同一平面内 |
| D.邻二甲苯的一氯代物只有两种 |
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是
| A.该图体现出原子核外电子层呈现周期性变化 |
| B.简单离子半径: W->R2->X+>S3+ |
| C.R、Z形成的化合物中可能含有共价键 |
| D.由酸性: HWO4>H2RO3可证明非金属性:W>R |
下列陈述I、II正确并且有因果关系的是
| 选项 |
表述一 |
表述二 |
| A |
浓硝酸在光照下颜色变黄 |
浓硝酸具有不稳定性 |
| B |
Cl2和SO2有漂白性 |
Cl2和SO2均可使含有酚酞的NaOH溶液褪色 |
| C |
常温下铁与浓硫酸不反应 |
可用铁槽车密封运送浓硫酸 |
| D |
SiO2有导电性 |
SiO2可用于制备光导纤维 |
实验室从含溴化氢的废液中提取溴单质,下列说法中能达到实验目的的是
| A.用装置甲氧化废液中的溴化氢 |
| B.用装置乙分离CCl4层和水层 |
| C.用装置丙分离CCl4和液溴 |
| D.用仪器丁长期贮存液溴 |
下列表示对应化学反应的离子方程式.其中正确的是
| A.向NaAlO2溶液中通入足量CO2:2AlO2-+CO2+3H2O==2Al(OH)3↓+CO32- |
| B.(NH4)2Fe(SO4)2溶液中加入少量的氢氧化钡溶液:NH4++SO42-+Ba2++2OH-=BaSO4↓+H2O |
| C.工业上用氨水吸收二氧化硫:2NH3.H2O+SO2=SO32-+2NH4+ |
| D.磁性氧化铁溶于稀硝酸:3Fe2+ +4H+ +NO3-=3Fe3+ +NO+2H2O |
25℃时,醋酸、次氯酸、亚硝酸的电离常数如下表,下列叙述不正确的是
| 酸 |
醋酸 |
次氯酸 |
亚硝酸 |
| 电离常数 |
1.7×10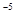 |
3.0×10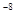 |
7.1×10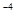 |
A.PH相同的氯水和亚硝酸溶液,水电离出的C(H+)相同
B.往氯水滴加NaOH溶液呈中性:C(Na+)=2C(ClO-)+C(HClO)
C.浓度相等的CH3COONa和NaNO2两份溶液中:C(CH3COO-)>C(NO2-)
D.向pH=a的醋酸溶液中加一定量水,所得溶液的pH>a、pH<a、pH=a均有可能
用酸性氢氧燃料电池(甲池)为电源进行电解的实验装置(乙池,一定条件下可实现有机物的电化学储氢)如下图所示.甲池中C为含苯的物质的量分数为10%的混合气体,D为l0mol混合气体其中苯的物质的量分数为24%(杂质不参与反应),E为标准状况下2. 8mol气体(忽略水蒸汽),下列说法正确的是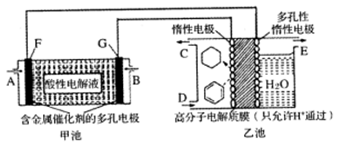
| A.甲池中A处通入H2,E处有O2放出 |
| B.甲池中H+由F极移向G极 |
| C.乙池中阴极区只有苯被还原 |
| D.导线中共传导11.2mol电子 |
乙酰苯胺可用作止痛剂、退热剂、防腐剂和染料中间体,实验室制备乙酰苯胺反应原理和有关数据如下:
| 名称 |
相对分子质量 |
性状 |
密度(g/cm3) |
沸点/℃ |
溶解度 |
|
| 苯胺 |
93 |
无色油状液体具有还原性 |
1.02 |
184 |
微溶于水 |
均易溶于乙醇、乙醚 |
| 乙酸 |
60 |
无色液体 |
1.05 |
118 |
易溶于水 |
|
| 乙酰苯胺 |
135 |
白色晶体 |
1.22 |
304 |
微溶于冷水、溶于热水 |
实验步骤:
在50ml圆底烧瓶中加入无水苯胺5ml.,冰醋酸7.5mL,锌粉0.lg,按下图安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,调节加热温度,使柱顶温度控制在105℃左右,反应约60~ 80nun,当反应基本完成时,停止加热.
在搅拌下,趁热将烧瓶中的物料倒人盛有l00mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品.将粗品重结晶,抽滤,晾干,称重,计算产率,注:D为刺形分馏柱,用于沸点差别不太大的混合物的分离.
请回答下列问题:
(1)仪器B的名称 。
(2)装置图中加热可用 (填“水浴”或“油浴”)。
(3)实验中加入锌粉的目的是 。
(4)为何要控制分馏柱上端的温度在105℃左右 。
(5)通过观察到 ,现象可判断反应基本完成,反应结束后须立即倒入事先准备好的冰水中的原因 。
(6)洗涤乙酰苯胺粗品最合适的试剂是 。
a.用少量冷水洗
b.用少量热水洗
c.先用冷水洗,再用热水洗
d.用酒精洗
(7)该实验最终得到纯品1.8 g,则乙酰苯胺的产率是 。
将废旧锌锰电池处理得到含锰混合物,现以含锰混合物为原料制备锰锌铁氧体的主要流程如图l所示:
请回答下列问题:
(1)MnOOH中,锰元素的化合价为____。
(2)碱性锌锰干电池的电解质为KOH,Mn02参与的电板反应方程式为 。
(3)酸浸时,MnO2与H2SO4、H2O2反应的离子方程式为 。
(4)在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图2所示:
①pH对Hg吸收率的影响规律是 。
②在强酸性环境下Hg的吸收率高的原因可能是 。
(5)锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O
①当1molMnO2参加反应时,共有_____mol电子发生转移。
②MnOOH与浓盐酸在加热条件下也可发生反应,试写出其反应的化学方程式:_________________。
③已知:Ksp(MnCO3)=2.3×10-11、Ksp(Mn(OH)2))=2.1×10-13,欲制备MnCO3,选用的加料方式是______(填字母),原因是___________________________________。
a.将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将MnSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
d.以上三种方法都无法制得MnCO3
SiCl4在室温下为无色液体,易挥发,有强烈的刺激性.把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅.
(1)高温条件下,SiHCl3与氢气反应的方程式为: 。
(2)已知:
(ⅰ)Si(S)+4HCl(g)=SiCl4(g)+2H2(g) △H=-241KJ.mol-1
(ⅱ)Si(S)+3HCl(g)=SiHCl3(g)+H2(g) △H=-210KJ.mol-1
则SiCl4转化为SiHCl3的反应(ⅲ):3SiCl4(g)+2H2(g)+Si(S)==4SiHCl3(g) △H=______。
(3)力研究反应(iii)的最适宜反应温度,下图为四氯化碳的转化率随温度的变化曲线:由图可知该反应最适宜的温度为 ,四氯化碳的转化率随温度升高而增大的原因为____。
(4)一定条件下,在2L恒容密闭容器中发生反应(ⅲ),6h后达到平衡,H2与SiHCl3的物质的量浓度分别为1mol.L-1和0.2 mol.L-1
①从反应开始到平衡,v(SiCl4)=___________。
②该反应的平衡常数表达式为K= ,温度升高,K值 (填“”增大”、“减小”或“不变”)。
③原容器中,通入H2的体积(标准状况下)为 。
④若平衡后再向容器中充人与起始时等量的SiCl4和H2(假设Si足量),当反应再次达到平衡时,与原平衡相比较,H2的体积分数将 (填“增大”、“减小”或“不变”).
⑤平衡后,将容器的体积压缩为1L,再次达到平衡时,H2的物质的量浓度范围为 。
【化学选修2一化学与技术】下图是某企业设计的硫酸一磷肥一水泥联产、海水一淡水多用、盐一热一电联产的三大生态产业链流程图.
根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:① 、②____、③__ 、④ 、⑤
(2)沸腾炉发生反应的化学方程式: ,磷肥厂的主要产艄是普钙(磷酸二氢钙和硫酸钙),写出由磷矿石和硫酸反应制普钙的化学方程式 .
(3)用1吨硫铁矿(FeS2的质量分数为36%)接触法制硫酸,制硫酸的产率为65%,则最后能生产出质量分数为98%的硫酸____吨.
(4)热电厂的冷却水是____,该流程中浓缔盐水除提取盐以外还可提取的物质有 (写出一种即可).
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气和废渣的利用设想. (写出两点即可).
【化学选修3-物质结构与性质】X、Y、Z、W、Q五种前四周期元素,原子序数依次增大.已知X、Y、Z、W均为非金属元素,XW2分子与Y3为等电子体,元素W的原子序数等于元素Z的原子序数加8,Q的最外层电子数为2,次外层电子数等于Y和W2 -最外层电子数之和,根据以上信息回答下列问题:
(1)上述五种元素中电负性最大的是____(填元素符号,下同),Y的第一电离能大于Z的第一电离能原因 。
(2)XW2的电子式为 。Y3的分子构型为 。
(3)Q的价电子排布式为 。
(4)下列关于WZ2结构的说法正确的是 。
a.WZ2直线形非极性分子
c.WZ2中w为sp3杂化
b.WZ2直线形极性分子
d.WZ2中W为sp2杂化
(5)d-QW的晶胞是立方体,用X射线衍射法测得该晶体晶胞边长a=520.0pm,26℃测得该晶体的密度为4.1g/cm3,请列式计算一个晶胞中含有的Q、W离子数。(5.23=140.6)
(6)d-QW的晶胞的一个侧面的投影图如图所示,与Q离子距离最近且距离相等的W离子构成的几何图形是________________
【化学选修5-有机化学基础】化合物G是一种医药中间体,常用于制备抗凝血药.可以通过下图所示的路线合成:
请回答下列问题:
(1)B→C的转化所加的试剂可能是_______C+E→F的反应类型是________。
(2)有关G的下列说法正确的是___________。
a.属于芳香烃
b.可以发生水解、加成、氧化、酯化等反应
c.能与FeCl3溶液发生显色反应
d.1molG最多可以跟4molH2反应
(3)E的结构简式:___________________。
(4)F与足量NaOH浴液充分反应的化学方程式为 。
(5)E的同分异构体中,既能发生水解反应,又能与FeCl3溶液能发生显色反应的还有____种,其中苯环上有两种不同化学环境的氢原子的是 (写出其中一种的结构简式)。
(6)已经氯苯用10%到15%的氢氧化钠溶液在360到390℃、28-30MPa条件下水解再酸化,
可制取苯酚,而酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯( )是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。
)是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。
注:合成路线的书写格式参加如下示例流程图:
 粤公网安备 44130202000953号
粤公网安备 44130202000953号