SiCl4在室温下为无色液体,易挥发,有强烈的刺激性.把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅.
(1)高温条件下,SiHCl3与氢气反应的方程式为: 。
(2)已知:
(ⅰ)Si(S)+4HCl(g)=SiCl4(g)+2H2(g) △H=-241KJ.mol-1
(ⅱ)Si(S)+3HCl(g)=SiHCl3(g)+H2(g) △H=-210KJ.mol-1
则SiCl4转化为SiHCl3的反应(ⅲ):3SiCl4(g)+2H2(g)+Si(S)==4SiHCl3(g) △H=______。
(3)力研究反应(iii)的最适宜反应温度,下图为四氯化碳的转化率随温度的变化曲线:由图可知该反应最适宜的温度为 ,四氯化碳的转化率随温度升高而增大的原因为____。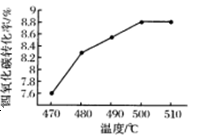
(4)一定条件下,在2L恒容密闭容器中发生反应(ⅲ),6h后达到平衡,H2与SiHCl3的物质的量浓度分别为1mol.L-1和0.2 mol.L-1
①从反应开始到平衡,v(SiCl4)=___________。
②该反应的平衡常数表达式为K= ,温度升高,K值 (填“”增大”、“减小”或“不变”)。
③原容器中,通入H2的体积(标准状况下)为 。
④若平衡后再向容器中充人与起始时等量的SiCl4和H2(假设Si足量),当反应再次达到平衡时,与原平衡相比较,H2的体积分数将 (填“增大”、“减小”或“不变”).
⑤平衡后,将容器的体积压缩为1L,再次达到平衡时,H2的物质的量浓度范围为 。
 CO(g)+H2(g),此反应是吸热反应
CO(g)+H2(g),此反应是吸热反应 (2)合成气合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g)△H=-90.8kJ· mol-1
(2)合成气合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g)△H=-90.8kJ· mol-1


 设计的原电池如图所示。
设计的原电池如图所示。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号