金属的腐蚀是指金属与周围接触到的气体或液体物质发生________而引起损耗的现象。金属腐蚀的本质是________________,发生________反应。一般可分为________腐蚀和________腐蚀。
(1)在下列物质中是同系物的有___________;互为同分异构体的有___________,是同一种物质的有___________。
(11)2,2-二甲基丁烷
(2)具有复合官能团的复杂有机物,其官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论。
如 具有三种官能团:__________、__________和__________(填官能团的名称),所以这个化合物可看作__________类、__________类和__________类。
具有三种官能团:__________、__________和__________(填官能团的名称),所以这个化合物可看作__________类、__________类和__________类。
在①CH2==CH2,② ,③CH3CH2OH,④CH3COOH,⑤聚乙烯五种物质中:
,③CH3CH2OH,④CH3COOH,⑤聚乙烯五种物质中:
(1)能使Br2的CCl4溶液褪色的是___________;
(2)属于高分子化合物的是___________;
(3)能与Na2CO3溶液反应的是___________;
(4)能发生酯化反应的是___________;
(5)既能发生取代反应又能发生加成反应的是________________。
下表是摘自国家环境监测中心公布的某时间我国部分大城市空气的监测周报.
| 城市 |
污染 指数 |
首要 污染物 |
空气质 量级别 |
城市 |
污染 指数 |
首要 污染物 |
空气质 量级别 |
| 北京 |
92 |
TSP |
Ⅱ |
济南 |
76 |
TSP |
Ⅱ |
| 天津 |
82 |
TSP |
Ⅱ |
武汉 |
83 |
NO x |
Ⅱ |
| 长春 |
103 |
TSP |
Ⅲ |
深圳 |
77 |
NO x |
Ⅱ |
| 上海 |
74 |
NO x |
Ⅱ |
汕头 |
54 |
|
Ⅱ |
| 杭州 |
67 |
TSP |
Ⅱ |
成都 |
87 |
TSP |
Ⅱ |
| 福州 |
42 |
|
Ⅰ |
重庆 |
98 |
SO 2 |
Ⅱ |
| 厦门 |
25 |
|
Ⅰ |
贵阳 |
69 |
TSP |
Ⅱ |
注:TSP:空气中飘尘;NO x :含氮氧化物.
阅读分析上表,回答下列问题:
(1)经济特区中,空气质量最好的城市是_____________,直辖市中空气质量最差的城市是_____________.
(2)最容易出现酸雨的城市是_____________.为防止城市出现酸雨,降低煤燃烧时向大气排放的SO 2 ,工业上将生石灰或石灰石和含硫煤混合使用.请写出燃烧时,有关“固硫”(不使含硫化合物进入大气)反应的化学方程式 ___________________________.
空气污染监测仪是根据SO 2 与Br 2 的定量反应测定空气中SO 2 的含量:SO 2 +Br 2 + 2H 2 O="=H" 2 SO 4 +2HBr,上述反应的溴,来自一个装满酸性KBr溶液的电解槽阳极上的氧化反应。电解槽的阴、阳极室是隔开的。当测空气中SO 2 的含量时,空气(经过除尘)以1.5×10 - 4 m 3·min - 1 的流速进入电解槽的阳极室,电流计显示每秒通过的电子是8.56×10 - 1 1mol时,此条件下能保持溴浓度恒定,并恰与SO 2 完全反应(设被测空气中不含与溴反应的物质)。
(1)写出监测过程中主要发生的化学反应方程式;_______________________。
(2)计算空气中SO 2 的含量(g·m - 3 空气)。
按下面的实验过程填空: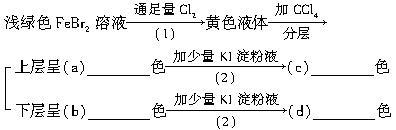
写出上述反应的化学方程式:
(1)______________________________________________;
(2)______________________________________________;
(3)______________________________________________。
填空:
(1)图Ⅰ表示10 mL量筒中液面的位置,A与B、B与C刻度间相差1 mL。如果刻度A为4,量筒中液体的体积是______________mL。

图Ⅰ 图Ⅱ
(2)图Ⅱ表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_______________。
A.是a mL B.是(50-a) mL
C.一定大于a mL D.一定大于(50-a) mL
试样X由氧化亚铁和氧化铜组成,取质量相等的两份试样按图所示进行实验: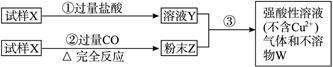
(1)请写出步骤③中所发生的全部反应的离子方程式。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中氧化铜的质量为______________(用m表示)。
“探险队员”——盐酸,不小心走进了化学迷宫,迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
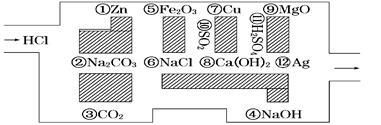
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)_____________。
(2)在不能“吃掉”盐酸的物质中,属于非电解质的是________(填写物质序号),在能“吃掉”盐酸的物质中,属于电解质的是 (填写物质序号)。
(3)如果将盐酸换成碳酸镁,它能沿着盐酸走出的路线“走出”这个迷宫吗?填“能”或“不能”_____,写出离子方程式说明其原因: 。
(4)写出氧化铝与④反应的化学方程式 ,氧化铝属于 ____________氧化物(填“酸性”“碱性”或“两性”)。
现有盐酸、铁、氢气、碳酸氢钠、氢氧化钡。根据要求回答下列问题:
(1)下图为常见物质的树状分类图:
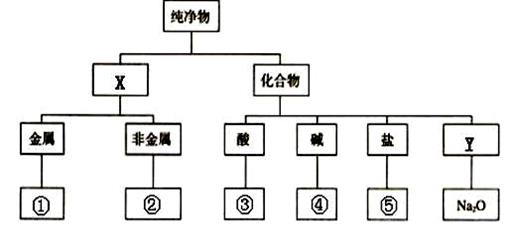
X属于_________(填物质类属);若图中①—⑤分别代表上述五种物质,则④对应的化学式是 。
(2)上述五种物质中,有一种物质能与其他三种物质发生反应。该物质是__________。
(3)上述五种物质间发生置换反应的离子方程式____________________
(4)写出过量的③与④反应的离子方程式 ____________________
Ⅰ、实验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
(1)该反应中的氧化剂是__________,被氧化的元素是__________.
(2)该反应中氧化剂和氧化产物的物质的量之比为___________.
(3)氧化性:KMnO4__________Cl2(填“>”、“<”或“=”)
(4)用双线桥法表示该反应中电子转移的方向和数目:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为__________.
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
(1)把氯气通入紫色石蕊试液中,可以观察到的现象是: ,请你解释其中的原因_____________________
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。
①写出反应的化学方程式 ;
②当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2 mol·L—1的NaOH溶液的体积至少应为 L
研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2<0(Ⅱ)
2ClNO(g) K2 ΔH2<0(Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=__________(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=__________(用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________mol,NO的转化率α1=_______。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2_____α1(填“>”“<”或“=”),平衡常数K2__________(填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是______________。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH===NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 molL的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为_________________。(已知HNO2电离常数Ka=7.1×10-4 mol·L-1,CH3COOH的电离常数Ka=1.7×10-5 mol·L-1)
可使溶液A和溶液B的pH相等的方法是____________。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式______________________ _。
(2)若溶液M由10mL 2 mol·L-1NaHA溶液与2mol·L-1NaOH溶液等体积混合而得,则溶液M的pH ________7 (填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为
(3)若溶液M由下列三种情况:①0.01mol·L-1的H2A溶液②0.01mol·L-1的NaHA溶液③0.02mol·L-1的HCl与0.04mol·L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为_ _ _ _ __;pH由大到小的顺序为 。
综合利用CO2、CO对构建低碳社会有重要意义。
(1)固体氧化物电解池(SOEC)用于高温电解CO2和H2O的混合气体,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如图。

①b为电源的 (填“正极”或“负极”)
②写出电极c发生的电极反应式 、 。
(2)电解生成的合成气在催化剂作用下发生如下反应:CO(g) +2H2(g) CH3OH(g)。对此反应进行如下研究:某温度下在一恒压容器中分别充入1.2mol CO和1mol H2,达到平衡时容器体积为2L,且含有0.4mol CH3OH(g),则该反应平衡常数值为 ,此时向容器中再通入0.35molCO气体,则此平衡将 移动(填“向正反应方向”、“不”或“逆反应方向”)。
CH3OH(g)。对此反应进行如下研究:某温度下在一恒压容器中分别充入1.2mol CO和1mol H2,达到平衡时容器体积为2L,且含有0.4mol CH3OH(g),则该反应平衡常数值为 ,此时向容器中再通入0.35molCO气体,则此平衡将 移动(填“向正反应方向”、“不”或“逆反应方向”)。