周期表前四周期的元素Q、R、X、Y、Z原子序数依次增大,Q元素的原子形成的离子就是一个质子;R基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;X基态原子s能级的总电子数比p能级的总电子数多1;Y原子的核外成对电子数是未成对电子数的3倍;Z原子的价电子排布为3d74S2。
回答下列问题:
(1)R、X、Y中第一电离能最大的是 (填元素符号),其中Y原子的电子排布式为 。
(2)Q、R元素形成的某分子中共有14个电子,该分子中R原子采取 杂化,该分子的立体构型为 。
(3)RY可以和很多过渡金属形成配合物,如Fe( RY)5、Ni(RY)4。其中Fe(RY)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe (RY)5晶体属于 (填晶体类型)。RY与N2互为等电子体,与RY互为等电子体的离子有 (任写一种)。
(4)向含Z2+的溶液中加入过量的氨水,并通入适量的Y2气体,生成有[Z(NH3)6]3+离子,则该反应的离子方程式为 。
A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图①所示:
(1)写出B的结构简式 ;A中官能团的名称为 。
(2)写出下列反应的化学方程式反应① ;反应④ ;
(3)实验室利用反应③制取C,常用上图②装置:
①a试管中的主要化学反应的方程为: 。
②在实验中球形干燥管除起冷凝作用外,另一个重要作用是 。
③试管b中观察到的现象是 。
(1)下列有关硅单质及其化合物的说法正确的是 。
A.高纯度的硅单质广泛用于制作光导纤维
B.水泥、玻璃、陶瓷都是硅酸盐产品
C.自然界中的硅元素储量丰富,并存在大量的硅单质
D.SiO2属于酸性氧化物,故只与碱溶液发生化学反应,不与任何酸反应
(2)某些化学反应可用下式表示(未配平):A+B→C+D+H2O,请回答下列问题:
①若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,D具漂白性。
A. 写出该反应的离子方程式: 。
B. Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备: MgCl2+2NaClO3=Mg(ClO3)2+2NaCl
MgCl2+2NaClO3=Mg(ClO3)2+2NaCl ,已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:
,已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:



将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2。简述可制备Mg(ClO3)2的原因: 。
②若A与B加热生成的产物C、D均为无色气体,且C、D两分子中组成元素的原子个数比都为1:2,则符合上式的化学方程式是: 。
③若A为过氧化钠,B为硫酸,则C、D的化学式为 、 。
胃酸过多是常见的胃病之一,下面是甲、乙两种常见胃药的性质摘要。
甲:①白色结晶状粉末,受热可缓慢分解,焰色反应为黄色。 ②能溶于水,水溶液呈弱碱性,但是属于盐类。③遇酸及酸性药物则产生CO2。④胃酸过多患者服用多见胃胀气,甚至有引起胃溃疡穿孔的危险。
乙:①与胃酸发生中和作用缓慢而持久,可维持3到4小时。②凝胶本身覆盖于溃疡面上具有保护作用。③可溶于稀酸或氢氧化钠溶液中。④其中含有的金属元素是地壳中含量最多的金属元素。
(1)请你推测甲中含有的主要化学成分是 (填化学式),其俗名为________________。
(2)写出甲中主要成分引起胃胀气(生成CO2 )的反应的离子方程式 。
(3)乙中含有的主要化学成分是 (填化学式),加热时,可以分
解为水和________________________(填化学式)。写出乙中的主要成分与氢氧化钠溶液反应的化学方程式 。
(4)等质量的两份铝分别与足量等物质的量浓度的盐酸和氢氧化钠溶液反应,消耗盐酸和氢氧
化钠溶液的体积之比为 ,生成氢气的物质的量之比为 。
高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如下方案制备高铁酸钾:
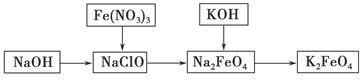
(1)高铁酸钾中铁元素的化合价为________,推测它具有的化学性质是__________________。
(2)已知Fe2O3与KNO3和KOH的混合物加热共融也可制得高铁酸钾。完成并配平下列化学方程式:
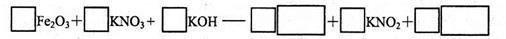
(3)将KOH加入含Na2FeO4的溶液中搅拌半小时,静置,过滤粗产品,该过程发生的反应为2KOH+Na2FeO4===K2FeO4+2NaOH,根据复分解反应原理,高铁酸钠的溶解度________(填“大于”、“小于”或“等于”)高铁酸钾的溶解度。
(4)为测定含铁溶液中铁元素的总含量,实验操作:
①准确量取20.00mL含铁溶液于带塞锥形瓶中,加入足量H2O2,待充分反应后,加热除去过量H2O2;
②加入过量KI充分反应后,再用0.1000 mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00 ml。已知:
①写出滴定选用的指示剂 ,滴定终点观察到的现象 。
②溶液Ⅰ中铁元素的总含量为 g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会 (填“偏高”“偏低”“不变”)。
将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g)  xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:
n(A)=n(B)=________mol。
(2)B的平均反应速率v(B)=________mol/(L·min)。
(3)x的值为________。
“8·12”天津港危化仓库爆炸,造成生命、财产的特大损失。据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN)。请回答下列问题:
(1)钠、钾着火,下列可用来灭火的是 。
A. 水 B.泡沫灭火器 C.干粉灭火器 D.细沙盖灭
(2)NH4NO3为爆炸物,在不同温度下加热分解,可能发生非氧化还原反应,可能发生氧化还原反应,下列反应可能发生的是 。
A. NH4NO3 → N2 + O2 + H2O
B. NH4NO3 → NH3 + HNO3
C. NH4NO3 → O2 + HNO3 + H2O
D. NH4NO3→ N2 + HNO3 +H2O
E. NH4NO3→N2+ NH3+ H2O
F. NH4NO3 →N2O + H2O
(3)NaCN属于剧毒物质,有多种无害化处理方法
① H2O2处理法:NaCN + H2O2 —— N2↑+ X + H2O,推测X的化学式为 ,双氧水的电子式为 。
② NaClO处理法:aCN-+bClO-+2cOH-= dCNO-+eN2↑+fCO32-+bCl-+cH2O。 方程式中e : f的值为
(填选项标号)。
A.1 B.1/2 C.2 D.不能确定
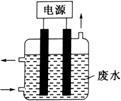
③用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,某电极上产生的ClO-将CN-氧化为两种无污染的气体,则电解过程中,阳极的电极反应式为 。
(4)以TiO2为催化剂用NaClO将CN-离子氧化成CNO-,CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol·L—1)进行实验。
①写出CNO-在酸性条件下被NaClO氧化的离子方程式:_______ _______;
②若结果测得CO2的质量为1.408g,则该实验中测得CN-被处理的百分率为 。
(1)将标况下的2.24LCO2通入150mL 1mol•L-1NaOH溶液中,溶液中离子浓度由大到小的顺序为
(2)0.02mol/L的醋酸溶液与0.01mol/L的氢氧化钠溶液等体积混合,混合后溶液的pH=6,则溶液中除水分子外粒子浓度(含CH3COOH)由大到小的顺序为 ,溶液中c(CH3COO—)-c(Na+)= (写出精确计算结果)
已知25℃时Ksp[Mg(OH)2]=1.0×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(3)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式)。
(4)室温时,Mg(OH)2(S) Mg2+(aq)+2OH-(aq) 当Mg2+沉淀完全(离子浓度小于10-5mol/L)时,溶液的pH=_______。
Mg2+(aq)+2OH-(aq) 当Mg2+沉淀完全(离子浓度小于10-5mol/L)时,溶液的pH=_______。
在氮的单质和化合物中,遇到HCl会产生白烟的是 (用字母填空);与氢氧化钙加热发生反应产生刺激性气味气体的是 (用字母填空)。
| A.氮气 | B.氨气 | C.硝酸钠 | D.氯化铵 |
将过量的铜置入一定量的浓硝酸中,充分反应后放出11.2 L气体(标准状况下),试回答下列问题:
(1)反应放出的气体中,含有 (写化学式);
(2)写出反应过程中的的化学方程式: ;
(3)若有19.2g铜溶解,则参加反应的HNO3的物质的量 被还原HNO3的质量为
完成下列各题
(1)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是 __(填“CaCl2”或“Ca(ClO)2”)。
(2)某些合成染发剂含有对苯二胺(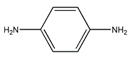 ),有一定的致癌作用。对苯二胺属
),有一定的致癌作用。对苯二胺属
于 (填“有机物”或“无机物” )。
中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
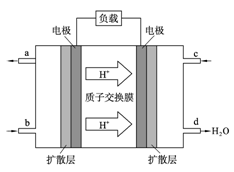
(1)该电池工作时,b口通入的物质为____________,c口通入的物质为__________。
(2)该电池负极的电极反应式为_________________。
(3)工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有__________NA个电子转移。
(4)若将a口排放出的1.12L气体,通入到5L0.015mol·L-1NaOH溶液中完全反应。反应后的溶液中离子浓度由大到小的顺序为 。
0.1 mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6 mol,则该烃的分子式为 。若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2.2—二甲基丁烷,则此烃属于 烃,结构简式为 ,名称是 。
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。例如二乙醚的结构简式为:CH3—CH2—O—CH2—CH3,其核磁共振谱中给出的峰值(信号)有两个,如图所示:
(1) 下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是 。
| A.CH3CH3 | B.CH3COOH |
| C.CH3COOCH3 | D.CH3OCH3 |
(2) 化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如右图所示,则A的结构简式为: ,请预测B的核磁共振氢谱上有 个峰(信号)。
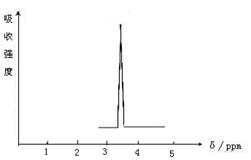
(3)用核磁共振氢谱的方法来研究C2H6O的结构,简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是 。