(1)在下列物质中是同系物的有___________;互为同分异构体的有___________,是同一种物质的有___________。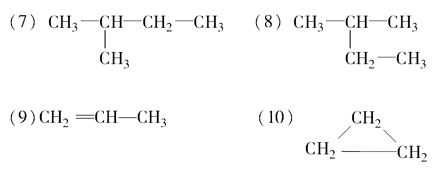
(11)2,2-二甲基丁烷
(2)具有复合官能团的复杂有机物,其官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论。
如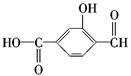 具有三种官能团:__________、__________和__________(填官能团的名称),所以这个化合物可看作__________类、__________类和__________类。
具有三种官能团:__________、__________和__________(填官能团的名称),所以这个化合物可看作__________类、__________类和__________类。
(1)在下列物质中是同系物的有___________;互为同分异构体的有___________,是同一种物质的有___________。
(11)2,2-二甲基丁烷
(2)具有复合官能团的复杂有机物,其官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论。
如 具有三种官能团:__________、__________和__________(填官能团的名称),所以这个化合物可看作__________类、__________类和__________类。
具有三种官能团:__________、__________和__________(填官能团的名称),所以这个化合物可看作__________类、__________类和__________类。