燃烧法是测定有机化合物化学式的一种重要方法。已知完全燃烧0.2 mol某烃后,测得生成CO2 17.92 L(STP),生成水18 g。据此推断该烃的化学式。
为了测定某铜银合金的组成,将30.0 g合金溶于80 mL 13.5 mol·L-1的浓硝酸中,待合金完全溶解后,收集到气体6.72 L(标准状况),并测得溶液中H+的物质的量浓度为1 mol·L-1,假设反应后溶液的体积仍为80 mL,计算:
(1)被还原的硝酸的物质的量。
(2)合金中银的质量分数。
使250 mL密度为1.1 g·cm-3、质量分数为24.5%的硫酸跟铁屑充分反应。计算:
(1)此硫酸中H2SO4的物质的量浓度。
(2)生成H2的体积(标准状况)。
(3)将生成的硫酸亚铁配制成400 mL溶液,此溶液中硫酸亚铁的物质的量浓度是多少?
取碳酸钠和碳酸氢钠混合物27.4 g,加热到质量不再减少为止,剩余固体物质的质量为21.2 g,试计算原混合物中碳酸钠和碳酸氢钠各为多少克。
在2KMnO4+16HBr====5Br2+2MnBr2+2KBr+8H2O反应中,若消耗1 mol氧化剂,则被氧化的还原剂的物质的量是_______________mol。
已知2.00% CuSO4溶液的密度为1.02 g·mL-1,欲配制500 mL这种溶液需用胆矾多少克?所得溶液的物质的量浓度是多少?
.实验室欲配制6 mol·L-1的硫酸溶液,现有三种不同浓度的硫酸:①240 mL、1 mol·L-1的硫酸 ②150 mL 25%(ρ="1.18" g·cm-3)的硫酸 ③18 mol·L-1的H2SO4足量。还有三种规格的容量瓶:250 mL、500 mL、1 000 mL。配制要求:①②两种H2SO4全部用完,不足部分由③补充。问需选用哪种容量瓶?需用18 mol·L-1浓H2SO4多少毫升?
通常情况下,CO与O2的混合气体m L,用电火花引燃后体积变为n L(在相同条件下测定)。
(1)试确定原混合气体中CO与O2的体积。
(2)若反应后的气体密度在相同条件下为氢气的15倍时,试确定反应气体的组成及体积之比。
已知某浓度氨水中氨气的物质的量浓度为18.4 mol·L-1,溶液的密度为0.900 g·mL-1,则该溶液中溶质的质量分数是多少?
下面是一个四肽,它可以看作是4个氨基酸缩合生成3个水分子而得。
 式中,R、R′、R″、
式中,R、R′、R″、 可能是相同的或不同的烃基,或有取代基的烃基,
可能是相同的或不同的烃基,或有取代基的烃基, 称为肽键。今有一个“多肽”,分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸:
称为肽键。今有一个“多肽”,分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸:
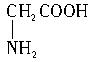

甘氨酸(C2H5NO2) 丙氨酸(C3H7NO2)

苯丙氨酸(C9H11NO2) 谷氨酸(C5H9NO4)
问:(1)这个“多肽”是几肽?
(2)该多肽水解后,有几个谷氨酸?
(3)该多肽水解后,有几个苯丙氨酸?
盖尔达法分解蛋白质的过程可表示为:蛋白质 硫酸铵
硫酸铵 氨
氨
现对牛奶中的蛋白质进行下列实验。取30.0 mL牛奶用盖尔达法分解蛋白质,把氮完全转化成氨,用0.5 mol·L-1 H2SO4 50.0 mL吸收后,剩余的酸用1 mol·L-1 NaOH溶液中和,需38.0 mL。求:
(1)30.0 mL牛奶中共含有多少克氮?
(2)如果蛋白质中含氮16%(质量分数),则牛奶中含蛋白质的质量分数是多少?(已知牛奶的密度是1.03 g·mL-1)
在一定温度下,气态烃CnHm与氢气在催化剂存在下反应生成CnHm+x。现将烃与氢气以不同比例混合,分别取出60 mL进行反应,混合气体中氢气的体积分数与反应后气体总体积之间的关系如图5-15所示。
图5-15
试完成下列问题:
(1)A点氢气的体积分数等于________。
(2)x=________。
(3)CnHm是既有双键又有三键的链烃,已知 的碳键结构是很少见的,则n值最小应等于__________。
的碳键结构是很少见的,则n值最小应等于__________。