对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、洗气、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有块状CaCO3。可用 的方法除去Ca(OH)2溶液中悬浮的CaCO3。
②除去H2中的CO2,可用 的方法除去。
③除去乙醇中溶解的微量食盐可采用 的方法。
④粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再 ;然后将滤液调成中性并 就可以得到纯净的氯化钠。
⑤除去氧化钙中的碳酸钙可用 的方法。
为下列混合物的分离或提纯提供正确的方法:
(1)除去食盐水中的泥沙 ;
(2)分离水和汽油的混合物 ;
(3)分离四氯化碳(沸点为76.75℃)和甲苯(有机溶剂,与CCl4互溶。沸点为110.6℃)的混合物 ;
(4) 从食盐水中提取氯化钠 。
除去下列物质中所含少量杂质(括号内为杂质)的方法是(前两个用化学方程式表示;后两个用离子方程式表示)
(1)Na2O2(Na2O)______________________________________
⑵Na2CO3固体(NaHCO3固体)___________________________
⑶KCl溶液(K2CO3)________________________________
⑷NaHCO3溶液(Na2CO3)______________________________
I.下列实验中仪器的下端必须插入反应物液面下的是: 。(填写序号)
①制备氢气的简易装置中的长颈漏斗;②制备氯气装置中的分液漏斗; ③制备硝基苯时的温度计;④用乙醇制取乙烯时的温度计; ⑤分馏石油时的温度计。
II.完成以下实验:①
用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验。在试管I中依次加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。试回答下列问题: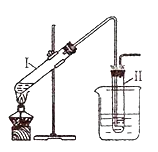
(1)试管I中反应的化学方程式 __________________。
(2)反应结束后,U形管中粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的_______________(填字母)
| A.NaOH溶液 | B.H2O | C.Na2SO3溶液 | D.CCl4 |
(3)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后__________________(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
(4)在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过下图所示的装置。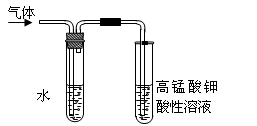
用上图装置进行实验的目的是 _;上图中右边试管中的现象是 ;水的作用是 。
(5)溴乙烷(C2H5Br)多一个碳的同系物在氢氧化钠的醇溶液中能发生反应,生成的产物为_________________
7分)某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下:(写出最佳答案)
(1)写出沉淀的化学式:沉淀1 ,白色沉淀2 ,
沉淀3 ;
(2)写出混合液加入A的离子方程式
(3)溶液加入B的离子方程式
已知:
| 溶解度 |
 |
C1- |
OH- |
| Ba2+ |
不溶 |
可溶 |
可溶 |
| Cu2+ |
可溶 |
可溶 |
不溶 |
| Ag+ |
微溶 |
不溶 |
不存在 |
常温下,某未知酸性溶液中,可能含有大量的Cl-、OH-、CO32-、H+、Ag+、Fe3+ 等离子。你认为其中一定含有的离子是 ,一定不含有的离子是 ,还需进一步检验的离子是 ,为了进一步确认是否含该离子,需要的试剂和现象为 。
(6分)如图为实验室分离水和乙醇的装置图,根据图示回答下列问题。

(1) 图中的两处明显的错误是:
_________________________________,
_________________________________。
(2) A仪器的名称是____________,B仪器 
的名称是_______________。
(3) 实验时向A中加入少量碎瓷片的作用是:
____________________________________________________。
(4)实验后锥形瓶中所收集到的物质为____________。
(7分) 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):


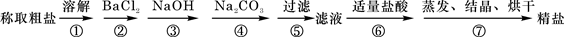
(1)判断BaCl2已过量的方法是_________________________________。
(2)第④步中,有关的离子方程式是_____________________________。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
_____________________________ 。
(4)为检验精盐纯度,需配制1000mL.0.2 mol/L NaCl(精盐)溶液,若定容时观察液面仰视(如右图所示),会造成所配制的溶液浓度(填偏高或偏低 )________________。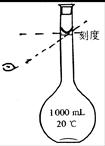
在锥形分液漏斗中加入10 mL 色碘水,然后再注入4 mL CCl4,盖好玻璃塞,按操作规则反复振荡后静置观察到的现象是:
操作完毕后,油层(即CCl4层)应从锥形分液漏斗的 口(填“上”或“下”)放出或倒出,为得到碘并回收CCl4可用 法。
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO以及泥沙等杂质,一位同学设计了一种制备精盐的实验方案,步骤如下(用于生成沉淀的试剂均稍过量):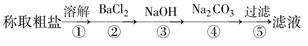
(1) 判断BaCl2已过量的方法是______________________________ 。
(2) 第④步中,相关的离子方程式是_________________________________ 。
(3)蒸发、结晶时,当 中剩余 时停止加热。
四只失去标签的试剂瓶中分别盛有NaCl溶液、NaNO3溶液、Na2CO3溶液和Na2SO4溶液,就如何检验这四种溶液做如下实验:先用四只试管分别取四种溶液各1mL, ① 在四只试管中分别滴入过量的同一种试剂,根据反应现象检验出一种物质;② 在剩余的三只试管中分别滴入第二种试剂,又检验出一种物质;③ 在剩余的两只试管中分别滴入第三种试剂,检验出第三种物质;④在三次实验中都没有明显现象的是第四种物质。请回答:
(1)①中加入的试剂的名称是 ;
(2)②中检验出的物质是 (写化学式);
(3)③中反应的现象是 。
有一固体粉末,可能由Na2CO3、CuSO4、CaCl2、Na2SO4、KCl中的一种
或几种,做了如下实验:
①将固体混合物溶于水,搅拌后得无色透明溶液;
②往此溶液中滴加BaCl2溶液,有白色沉淀生成;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀部分溶解。
试判断:
(1)固体粉末中肯定有 ,肯定没有 ,
可能有 。
(2)如要检验其是否存在,将如何操作 。
(1).现有以下物质①NaCl溶液 ②干冰 ③硫酸 ④铜 ⑤BaSO4固体 ⑥蔗糖 ⑦酒精 ⑧熔融状态的KNO3,其中属于电解质的是: ;属于非电解质的是: ;能导电的是: 。(均填序号)
(2).选择下列实验方法分离物质,将分离方法的字母填在横线上。
| A.萃取分液 | B.升华 | C.结晶 | D.分液 E.蒸馏 F.过滤 |
①分离粗盐中混有的泥沙______。 ②分离碘和水的混合物______。
③分离水和汽油的混合物______。 ④分离酒精和水的混合物______。
(3).离子方程式BaCO3+2H+ ="=" CO2↑+H2O+Ba2+中的H+不能代表的物质是_____________(填序号)①HCl ②H2SO4 ③HNO3 ④NaHSO4 ⑤CH3COOH
(4)取少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液先出现红褐色浑浊,接着红褐色浑浊逐渐变浅,最终又得到黄色的FeCl3溶液,先出现红褐色浑浊的原因: ,又得到黄色的FeCl3溶液的化学方程式为: 。
(9分) 选用一种试剂除去下列各物质中的杂质(括号内为杂质),把所选试剂的化学式填在横线上,并写出离子方程式。
(1)BaCl2(HCl)试剂 ;离子方程式为
(2)CO(CO2)试剂 ;离子方程式为
(3)Fe SO4 (Cu SO4) ;离子方程式为
(1)请指出下列做法中分别应用了哪些分离方法?(过滤、蒸发、蒸馏 、萃取、结晶)
a、熬煮中药__________________ b、分离豆浆和豆渣__________________
c、用海水晒盐____________________ d、海水淡化__________________
(2)写出离子反应方程式H+ + OH- =H2O所对应的两个不同类型化学方程式
①
②
(3).在下列反应中:
| A.2F2+2H2O=4HF+O2 | B.2Na+2H2O=2NaOH+H2↑ |
| C.CaO+H2O=Ca(OH)2 | D.2H2O=2H2↑+O2↑ |
水只作氧化剂的是 ,水只作还原剂的是 ,水既作氧化剂又作还原剂的是 ,水既不作氧化剂又不作还原剂的是 。请用线桥表示B反应的电子转移方向和数目。
2Na+2H2O=2NaOH+H2↑