选择下列实验方法分离物质,将分离方法的序号填在横线上。
A、萃取分液法 B、加热分解C、结晶法D、分液法E、蒸馏法F、过滤法
(1) 分离饱和食盐水和沙子的混合物;
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(3) 分离水和苯的混合物;
(4) 分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),已知四氯化碳和甲苯互溶。
(2分)下列实验操作或对实验事实的描述中正确的说法有 。
① 分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
② 除去甲烷中混有的少量乙烯,可以让混合物通过盛有酸性KMnO4溶液的洗气装置
③将无水乙醇和3mol·L-1 H2SO4混合加热到170℃,可制得乙烯
④只用溴水就可将苯、四氯化碳、乙醇、己烯四种液体区别开来
⑤用分液法分离苯和硝基苯的混合物
提纯下列物质(括号内为杂质),填写所选用的除杂试剂和除杂方法
| |
括号内为杂质 |
除杂试剂 |
操作 |
| 1 |
乙烷(乙烯) |
|
|
| 2 |
乙酸乙酯(乙酸) |
|
|
| 3 |
苯(苯酚) |
|
|
| 4 |
乙醇(水) |
|
|
某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下步骤进行:
Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 ,(填仪器名称)
(2)请写出加入溴水发生的离子反应方程式 ,
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是
若蒸发皿质量是W1 g,蒸发皿与加热后固体总质量是W2 g,则样品中铁元素的质量
分数是
Ⅱ.有同学提出,还可以采用以下方法来测定: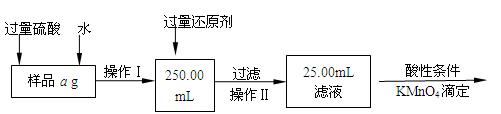
(1)溶解样品改用了硫酸,而不在用盐酸,为什么
(2)选择的还原剂是否能用铁 (填“是”或“否”),原因是:
(3)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是 。
若要除去下列各物质中的杂质,写出所用试剂:
(1)除去MgCl2中混有的少量MgCO3,可选用  溶液
溶液
(2)除去FeCl2中混有的少量Cu2+,可选用
(3)除去Fe粉中混有的少量Al粉,可选用 溶液
离子推断题
某待测液中可能含有Mg2+、NH4+、Ba2+、CO32-、SO42-、AlO2-等离子,各取少量进行如下实验:
(1)加足量NaOH溶液并加热,过程中无沉淀也无气体生成,可排除
离子大量存在;
(2)加入过量的稀盐酸,先出现白色沉淀,后来沉淀逐渐溶解消失。继续加稀硫酸,又出现白色沉淀。可肯定含有 离子,并排除
离子大量存在。
某待测液中可能含有A13+、Fe3+、K+、NH4+、C1-等离子,现通过如下实验对其中的阳离子进行检验:
(1)取少量待测液,仔细观察,呈无色;
(2)向上述待测液中滴加NaOH溶液,有白色沉淀生成,NaOH溶液过量后沉淀又完全溶解,再加热还有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变蓝。
据此可以判断该待测液中一定含有的阳离子是 ▲ ,一定没有的阳离子是 ▲ 。还有一种阳离子没有检验,检验这种离子的实验方法是(填写实验名称) ▲ ,现象是 ▲ 。
下列两组混合物,括号内为杂质,填写除去杂质所需试剂或方法,并写出反应的化学方程式。(请按相应序号填在答题卷上)
| 混合物 |
试剂或方法 |
化学方程式 |
| Na2CO3固体(NaHCO3) |
① |
② |
| Fe2O3粉末(Al2O3) |
③ |
④ |
除去括号中杂质,写出所加试剂与反应的离子方程式。
(1)SO42― (CO32― ),所加试剂: ,离子方程式
(2)Cl―― (SO42― ),所加试剂: ,离子方程式
(3)Fe2+ (Cu2+),所加试剂: ,离子方程式
(4)BaCl2 (HCl ),所加试剂: ,离子方程式
利用下图装置,写出除去下列气体中的杂质的方法,并写出化学方程式(括号内的气体为杂质)。
(1)CO2(SO2):
化学方程式: _。
(2)SO2(SO3)(假设SO3为气体): 化学方程式:______________________________________________________
(3)NO(NO2):__________________________________________________。
化学方程式:_____________________________________________________。
某氯化钠样品中含有少量的硫酸钠和碳酸钠杂质,按下列流程进行净化,回答下列问题。
(1)分散系A、B都属于 (选填“溶液”“胶体”或“浊液”)。
(2)写出以下步骤所需的试剂(用化学式表示)
② ③ ⑤
(3)写出以下步骤的实验操作名称① ④ ⑥
(4)第④步中要用到的玻璃仪器有烧杯、 、
(5)写出第②步有关反应的离子方程式
用一种试剂除去下列物质中的杂质(括号内物质为杂质,所用试剂均为适量),写出所加的试剂及有关反应的离子方程式。
(1) FeSO 4溶液(CuSO 4):试剂
离子方程式
(2) Mg(Al):试剂
离子方程式
(3) CO(CO 2):试剂
离子方程式
实验室有一瓶混有少量NaCl杂质的NaOH固体试剂,为准确测其纯度,采用盐酸滴定法进行测定 。
。
①称取Wg NaOH固体试剂配制成100.00 mL水溶液备用;
②将浓度为c mol/L的标 准盐酸装在用标准盐酸润洗过的25.00 mL酸式滴定管中,调节液面位置
准盐酸装在用标准盐酸润洗过的25.00 mL酸式滴定管中,调节液面位置 在零刻度以下,并记下刻度;
在零刻度以下,并记下刻度;
③取V1 mL NaOH待测溶液置于洁净的锥形瓶中,加入2~3滴甲基橙指示剂充分振荡,然后用浓度为c mol/L的标准盐酸滴定,重复测定3次,平均用去盐酸V2 mL。
试回答:
(1)配制标准盐酸溶液时,必须使用的最主要玻璃仪器是____________。
(2)如有1 mol/L和0.1 mol/L的标准盐酸应选用_____mol/L盐酸,原因是______________
________________________________ _____________________________。
_____________________________。
(3)滴定时,滴定过程中两眼应该注视_____________________。滴定终点时溶液颜色由_____色突变为____色。在盛放待测溶液的锥形瓶下方放一张白纸的作用是 。
(4)下列操作会使实验测得结果偏大的是(填选项的序号) ;
| A.用湿润的pH试纸测定某NaOH溶液的pH |
| B.中和滴定实验中用蒸馏水洗净的锥形瓶直接装待测液 |
| C.若滴定前酸式滴定管尖嘴气泡未排出,滴定结束后气泡消失 |
D.装标准盐酸的 酸式滴定管没有进行润洗 酸式滴定管没有进行润洗 |
E.读数时,若滴定前仰视,滴定后俯视
(5)固体试剂NaOH的质量分数的表达式为 。
选择下列实验方法分离物质,请将分离方法的序号填在横线上
| A.萃取法 | B.结晶法 | C.分液法 | D.蒸馏法 E.过滤法 |
①____________分离饱和食盐水与沙子的混合物。
②____________分离水和汽油的混合物。
③____________分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
④____________从碘水里提取碘。
⑤____________从硝酸钾和氯化钠的混合液中获得硝酸钾。